ТЕПЛОВАЯ ТЕОРЕМА НЕРНСТА
Полученные ранее уравнения Q = f (Т), ln К = f (T) и А'max = φ (Т), являющиеся основными уравнениями химической термодинамики, позволяют рассчитывать тепловые эффекты реакции, определять условия химического равновесия и меру химического сродства. Однако для этого в зависимостях кроме теплового эффекта и теплоемкостей (Q0 и μ c) необходимо знать постоянную интегрирования С. Эту величину теоретически с помощью первых двух законов термодинамики определить не представляется возможным.
Константа интегрирования может быть вычислена только в том случае, если экспериментально для соответствующей температуры можно определить константу равновесия данной реакции. Необходимость предварительного нахождения константы равновесия для заданной температуры (что часто связано с большими затруднениями) осложняло изучение равновесия химических реакций. Поэтому естественным было стремление исследователей найти способ определения константы интегрирования теоретическим путем.
Если графически построить в координатах Qp—A'maxp = AG0 и Т кривые функций
Q = f (Т) и —A'maxp = ΔG = φ(T) по ранее приведенным уравнениям (56) и (223), получим
Qp = Q0 + αT + βT2 + γT3
и
-A'maxp = ΔG = Q0 - αT ln Т - βT2 - γТ3/2 - RTC,
то легко заметить, что при Т = 0 Qp и —Аmах р = ΔG равны между собой, т. е. обе кривые будут выходить из одной точки К (рис. 45). Зависимость Qp = f (T) изображается определенной кривой, начало которой расположено в точке К Отрезок на оси Qp от нуля до точки К соответствует Q0. Зависимость
—A'max р — ΔG = φ(T) на графике, из-за неопределенности постоянной интегрирования С, не может быть изображена определенной кривой.

Соответственно различным значениям С имеется целое семейство l кривых, берущих свое начало также из точки К
Вальтером Нернстом (1906 г.) была высказана гипотеза о том, что для конденсированных систем не только при абсолютном нуле, но и вблизи него значения энергии Гиббса и теплоты реакции Qp
равны между собой, т. е. Qp = f (Т) и ΔG = φ (T) при Т = 0, и не только выходят из одной точки К, но и вблизи абсолютного нуля имеют общую касательную. Следовательно, первые производные в точках касания, представляющие собой тангенсы углов наклона касательных к осям координат, должны быть равны между собой:
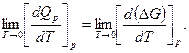
Экспериментально установлено, что при очень низких температурах свойства, конденсированных тел перестают зависеть от температуры. Поэтому общая касательная кривых функций Qp = f (T) и ΔG = φ (Т) должна идти параллельно оси температур:
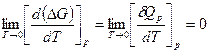
Для проверки этого предположения найдем из уравнений Гиббса— Гельмгольца (122) [ д (ΔG) д T]p при Т → 0:
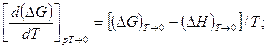 (246)
(246)
при T = 0
ΔG=ΔG0=ΔH0.
Следовательно, в правой части данного уравнения получили неопределенность.
Для раскрытия неопределенности продифференцируем по Т в правой части уравнения (246) в соответствии с правилом Лопи-таля числитель и знаменатель дроби, тогда
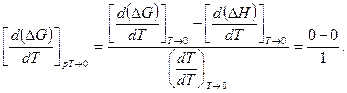
Таким образом,
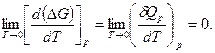 (247)
(247)
Из большого семейства кривых, представляющих функцию ΔG =φ (T), искомой кривой будет кривая, касательная к которой проведенная через точку K, параллельна оси Т.
Тепловая теорема Нернста позволяет решать уравнения для конденсированных систем вида lg Кр = f (Т) и ΔG = φ (T) по тепловым эффектам реакций и теплоемкостям веществ, участвующих в реакции. С помощью теоремы Нернста можно определить константы интегрирования, неизвестные в указанных уравнениях.
Дифференцируя уравнение зависимости теплового эффекта Qp = f{T) от температуры (56) по температуре и учитывая, что Q0 — const, получим
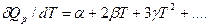
При T = 0 К α = δQp/dT. Так как {δQ/dT)T=o = 0, то и α=0, следовательно,
δQp/dT = 2βT + ЗγТ2 +….
Дифференцируя уравнение зависимости энергии Гиббса от температуры
ΔG == 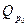 — αT ln T — βT2 — О,5γТ3 — RTC по температуре Т с учетом QP0 = const
— αT ln T — βT2 — О,5γТ3 — RTC по температуре Т с учетом QP0 = const
и α=0, получим
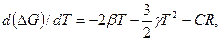
при Т=0
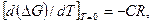
но так как 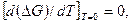 то при Т=0 и CR=0. Однако R не может быть равно нулю, поэтому С = 0. Следовательно, в уравнениях для конденсированных систем вида ΔG = φ (T) и In Kp = f (T) константы интегрирования равны нулю. Учитывая это, можно записать
то при Т=0 и CR=0. Однако R не может быть равно нулю, поэтому С = 0. Следовательно, в уравнениях для конденсированных систем вида ΔG = φ (T) и In Kp = f (T) константы интегрирования равны нулю. Учитывая это, можно записать
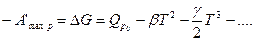 (248)
(248)
Из (248) следует, что максимальная полезная работа и энергия Гиббса могут быть вычислены при любой температуре по тепловому эффекту и теплоемкостям реагирующих веществ.
Если принять, что теплоемкость зависит от температуры по линейному закону, то уравнения зависимости энергии Гиббса и энергии Гельмгольца от температуры будет иметь вид при V = const ΔF = -RT ln Kc = QVo — βT2; при р = const ΔG = — RT ln и Kp = QPo — βT2. Так как для кон- дейсйрованных систем различие между A'maxp и A'maxv невелико То в общем виде
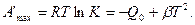 (249)
(249)
Уравнение (249) можно получить также в другом виде для этого умножим обе части уравнения работы 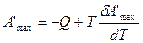 на dT и разделим на —Т2. Тогда
на dT и разделим на —Т2. Тогда
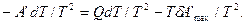
Перенесем в левую часть равенства член, содержащий 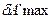 ;
;
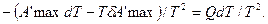 .
.
Проинтегрируем и умножим на Т обе части равенства:
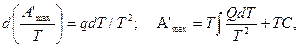
где С = 0 (согласно теореме Нернста) для конденсированной системы. Следовательно,
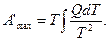
Имея в виду, что С = 0, и согласно закону Кирхгоффа,
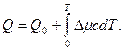
Подставив эти значения, получим
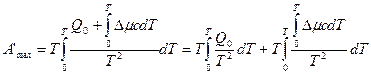
или
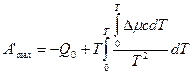 . (250)
. (250)
В такой форме удобно выражать работу, так как для многих реакций при разных температурах в таблицах приведены численные значения интегралов, входящих в уравнение (250).
ОСНОВНЫЕ СЛЕДСТВИЯ ТЕПЛОВОЙ ТЕОРЕМЫ НЕРНСТА
Из тепловой теоремы Нернста можно получить ряд важнейших следствий, имеющих большое практическое значение. Так, например, из уравнения Кирхгоффа (54) известно, что
δQ/dT = μс2 — μс1 = Δμс.
Согласно теореме Нернста (δQ/dT)T→0 = 0. Следовательно, можно сказать, что при абсолютном нуле алгебраическая сумма теплоемкостей конденсированных систем равна нулю, т. е.
 (251)
(251)
Это положение распространил Нернст и на значение самих теплоемкостей конденсированных систем. Это положение в настоящее время, как известно, подтвердилось в экспериментах: теплоемкости твердых тел при температуре, близкой к 0 К, резко падают и стремятся к нулю.
Из тепловой теоремы Нернста можно получить еще одно важное следствие, касающееся вычисления абсолютного значения энтропии.
Запишем уравнения максимальной работы (119) и (120) в дифференциальной форме:
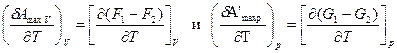
Учитывая, что 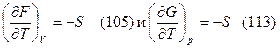 , можно записать
, можно записать

В общем случае имеем
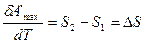 ;
;
при T=0
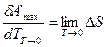 .
.
Так как
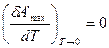 ,
,
то и
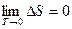 . (252)
. (252)
Следовательно, можно сказать, что при абсолютном нуле температуры изменение энтропии конденсированных тел равно нулю.
В дальнейшем это следствие из теоремы Нернста было дополнено Планком (1912 г.). Он предположил, что при температуре Т = 0 К значение энтропии конденсированных тел также можно считать, равным нулю, т. е.
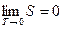 . (253)
. (253)
Это допущение носит название постулата Планка. Учитывая уравнение (253), можно вычислять абсолютные значения энтропии S конденсированных тел в зависимости от температуры.
Допустим, например, что при данной температуре необходимо определить энтропию тела, изменяющего свое состояние при р = const. Запишем известное уравнение для приращения энтропии
dS = δQ/T.
Заменив δQ = μсрdT, получим
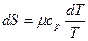 .
.
Проинтегрировав полученное уравнение, определяем приращение энтропии:
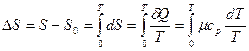 .
.
Так как согласно постулату Планка S0 = 0, то энтропия тела для данной температуры
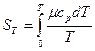 . (254)
. (254)
Таким образом, если известен закон изменения теплоемкости от температуры μср = f(T), то может быть найдено и истинное значение энтропии конденсированного тела для любой температуры.




