В течение не менее 2 ч после остановки кровотечения для избежания его рецидива больных не следует перекладывать и транспортировать.
5.2.3. Коагулопатия потребления с активацией вторичного фибринолиза (3- я сталия острого ДВС - синдрома)
Инициаторы развития. Поступление в системный кровоток инициаторов активации системы гемостаза:
• тканевого тромбопластина (преждевременная отслойка нормально расположенной плаценты, эмболия околоплодными водами, атоническое маточное кровотечение, внутриутробная гибель плода);
• фосфолипидов из разрушенных форменных элементов крови и эндотелия сосудов (тяжелые бактериальные и вирусные инфекции, кризис микроциркуляции во время шока любой природы и при им-мунокомплексных заболеваниях).
Клинические признаки. Коагулопатический и капиллярно-ге-матомный характер кровотечения:
• усиление кровотечения из родовых путей, тканей операционного поля;
• кровотечение по дренажам;
175
• изливающаяся кровь образует единичные, рыхлые, спонтанно лизирующиеся сгустки;
• диффузная кровоточивость тканей операционного поля, слизистых, мест инъекций;
• на коже и слизистых оболочках обильная геморрагическая сыпь, местами склонная к слиянию, возможно образование гематом.
• матка Кувелера.
Лабораторная диагностика.
Время свертывания крови по Ли — Уайту увеличено (12—60 мин), а в тесте спонтанного лизиса сгустка — быстрый лизис свернувшейся крови.
Снижение числа (< 100 ■ 109/л) и функции тромбоцитов.
Снижение факторов свертывания крови, преимущественно фибриногена (< 1,0 г/л).
Высокий уровень маркеров тромбинемии (F1 + 2, фибрин-мономер, комплекс тромбин + антитромбин, РКМФ) и плазминемии (плазмин-антиплазминовый комплекс, ПДФн и ПДФ, D-димер).
Гемостатическая терапия.
Ингибиторы протеаз: контрикал — 60—100 тыс. АТрЕ или гор-докс — 600—1000 тыс. Е или тразилол — 100—300 тыс. КИЕ вводят в/в шприцем.
Свежезамороженную плазму 15—20 мл/кг массы тела следует переливать через 15 мин после введения ингибиторов протеаз. Она применяется в/в, струйно. Необходимо использовать только плазму, совместимую по системе АВ0. Ее следует размораживать в течение 20 мин при температуре 37—38 °С.
Воздерживаться от переливания крови, заготовленной на гепарине, и реинфузии.
Местно с гемостатической целью в рану или в дренаж целесообразно на 20—30 мин вводить смесь, состоящую из е-аминокапроно-вой кислоты (100—400 мл 5 % раствора), сухого тромбина (125-500 ЕД) и адроксона (1—4 мл) или дицинона (250—500 мг). Эффект достигается лишь после применения ингибиторов протеаз или СЗП.
Местный гемостатик тахокомб, состоящий из коллагеновой пластины, покрытой с одной стороны высококонцентрированными тромбином, фибриногеном и апротинином, надежно склеивает за 5 мин раневую поверхность и коллагеновую пластину, даже при нарушениях биологического гемостаза.
Инфузионная терапия. Для лечения гиповолемии применять кровезаменители, не оказывающие прямого отрицательного воздействия на первичный и вторичный гемостаз (гелофузин, изотонические электролитные растворы).
176
Критерии эффективности гемостатической терапии:
1. Через 15 мин после введения ингибиторов протеаз изливаю-щаяся кровь образует единичные, рыхлые, спонтанно уже не лизи-руюшиеся сгустки.
2. После введения первых 2—3 доз СЗП (500—750 мл) наблюдаются следующие изменения:
. уменьшение кровотечения из родовых путей, тканей операционного поля, по дренажам и уменьшение повышенной кровоточивости мест инъекций;
. изливающаяся кровь образует плотные, спонтанно не лизиру-ющиеся сгустки;
• уменьшение диффузной кровоточивости тканей операционно
го поля, слизистых, мест инъекций.
3. После введения повторно 2—3 доз СЗП (500—750 мл) наблю
даются следующие изменения:
• резкое уменьшение или прекращение кровотечения из родовых путей, тканей операционного поля, по дренажам и уменьшение повышенной кровоточивости мест инъекций;
• изливающаяся кровь образует плотные, спонтанно не лизиру-ющиеся сгустки;
• уменьшение или прекращение диффузной кровоточивости тканей операционного поля, слизистых, мест инъекций.
4. Через 30 мин после введения тромбоцитов (0,5 дозы на 10 кг массы тела) прекращение диффузной кровоточивости тканей операционного поля, слизистых, мест инъекций.
5. Окончательная остановка кровотечения наблюдается через 60-90 мин от начала введения ингибиторов протеаз.
6. Если по истечении 60—90 мин уже нет клинико-лабораторных данных, подтверждающих острый ДВС-синдром, но интенсивность кровотечения сохраняется, следует предположить дефект хирургического гемостаза.
Тактика после остановки кровотечения. В течение не менее 2 ч после остановки кровотечения для избежания его рецидива больных не следует перекладывать и транспортировать.
5.2.4. Полное несвертывание крови (4- я сталия острого ДВС - синдрома)
Инициаторы развития. Поступление в системный кровоток инициаторов активации системы гемостаза:
• тканевого тромбопластина (преждевременная отслойка нор
мально расположенной плаценты, эмболия околоплодными водами,
атоническое маточное кровотечение, внутриутробная гибель плода);
177
• фосфолипидов из разрушенных форменных элементов крови и
эндотелия сосудов (тяжелые бактериальные и вирусные инфекции
кризис микроциркуляции во время шока любой природы и при при
иммунокомплексных заболеваниях).
Клинические признаки. Коагулопатический и капиллярно-ге-матомный характер кровотечения:
• профузное кровотечение из родовых путей, тканей операционного поля;
• по дренажам изливается жидкая кровь;
• изливающаяся кровь не образует сгустков;
• профузное кровотечение из неповрежденных слизистых носа, верхних дыхательных путей, желудка;
• кровоизлияния в жизненно важные органы: головной мозг, надпочечники;
• матка Кувелера.
Лабораторная диагностика.
Время свертывания крови по Ли — Уайту (более 60 мин) и тесты коагулограммы не определяются.
Снижение числа тромбоцитов (< 60 • 109/л).
Плазминемия (плазмин-антиплазминовый комплекс, ПДФн и ПДФ, D-димер).
Гемостатическая терапия.
Ингибиторы протеаз: контрикал — более 100 тыс. АТрЕ или гор-докс — более 1000 тыс. Е или тразилол — более 300 тыс. КИЕ, вводят в/в шприцем.
Свежезамороженную плазму 20—30 мл/кг массы тела следует переливать через 15 мин после введения ингибиторов протеаз. Она применяется в/в, струйно. Необходимо использовать только плазму, совместимую по системе АВ0. Ее следует размораживать в течение 20 мин при температуре 37—38 "С.
Воздерживаться от переливания крови, заготовленной на гепарине, и реинфузии.
Местно с гемостатической целью в рану или в дренаж целесообразно на 20—30 мин вводить смесь, состоящую из е-аминокапроно-вой кислоты (100—400 мл 5 % раствора), сухого тромбина (125-500 ЕД) и адроксона (1-4 мл) или дицинона (250-500 мг). Эффект достигается лишь после применения 750 мл СЗП.
Местный гемостатик тахокомб, состоящий из коллагеновой пластины, покрытой с одной стороны высококонцентрированными
178
тромбином, фибриногеном и апротинином, надежно склеивает за 5 мин раневую поверхность и коллагеновую пластину, даже при нарушениях биологического гемостаза. Инфузионная терапия. Для лечения гиповолемии применять кровезаменители, не оказывающие прямого отрицательного воздействия на первичный и вторичный гемостаз (гелофузин, изотонические электролитные растворы).
Критерии эффективности гемостатической терапии:
1. Через 15 мин после введения ингибиторов протеаз клинические признаки без динамики.
2. После введения первых 3—4 доз СЗП (750—1000 мл) наблюдаются следующие изменения:
• уменьшение кровотечения из родовых путей, тканей операционного поля, по дренажам и уменьшение повышенной кровоточивости мест инъекций;
• изливающаяся кровь образует единичные, рыхлые, спонтанно уже не лизирующиеся сгустки;
• уменьшение диффузной кровоточивости тканей операционного поля, слизистых, мест инъекций.
3. После введения повторно 2—3 доз СЗП (500—750 мл) наблю
даются следующие изменения:
• резкое уменьшение кровотечения из родовых путей, тканей операционного поля, по дренажам и уменьшение повышенной кровоточивости мест инъекций;
• изливающаяся кровь образует плотные, спонтанно не лизирующиеся сгустки;
• уменьшение диффузной кровоточивости тканей операционного поля, слизистых, мест инъекций.
4. Через 30 мин после введения тромбоцитов (1 доза на 10 кг массы тела) прекращение диффузной кровоточивости тканей операционного поля, слизистых, мест инъекций.
5. Окончательная остановка кровотечения наблюдается через 90-120 мин от начала введения ингибиторов протеаз.
6. Если по истечении 90—120 мин уже нет клинико-лаборатор-ных данных, подтверждающих острый ДВС-синдром, но интенсивность кровотечения сохраняется, следует предположить дефект хирургического гемостаза.
Тактика после остановки кровотечения. В течение не менее 2 ч после остановки кровотечения для избежания его рецидива больных не следует перекладывать и транспортировать.
179
5.3. ИНФУЗИОННЫЕ СРЕДЫ В АКУШЕРСКОЙ ПРАКТИКЕ
Инфузионные среды (кровезаменители) широко используют при выведении беременных, рожениц и родильниц из критических (экстремальных) состояний.
При неосложненном течении беременности к моменту родов во-лемические сдвиги выражаются гиперволемической гемодилюцией: прирост ОЦК на 80 % (1000-1200 мл), из которых за счет ОЦП 60 % (800-850 мл) и 20 % за счет ОЦЭ (200-350 мл); гематокрит 30—35 %. Реологические сдвиги проявляются повышением относительной вязкости крови, снижением КОД до 22 мм рт. ст., снижением осмолярности на 10 мосм/л (275—280 мосм/л), повышением агрегации эритроцитов. Повышается первичный и вторичный гемостаз. Развивается компенсированный метаболический ацидоз.
При течении беременности, осложненной гестозом, железодефи-цитной анемией, предлежанием плаценты, прирост ОЦК незначителен или отсутствует, КОД ниже 22 мм рт. ст., осмолярность ниже 275 мосм/л. Более выражено повышение относительной вязкости крови и агрегации эритроцитов. Нарушения гемостаза протекают по типу подострого или хронического ДВС-синдрома. Метаболический ацидоз уже декомпенсирован.
Выбор кровезаменителей должен основываться как на волеми-ческих, реологических и гемостатических свойствах крови и КОС беременных, так и на их свойствах.
Кровезаменители — водные растворы органических и неорганических веществ, вводимые парентерально для возмещения дефицита функций крови и коррекции патологических состояний организма человека.
Предложено несколько классификаций кровезаменителей: А. Н. Филатов (1943); А. Н. Филатов, И. Р. Петров, Л. Г. Богомолова (1958); А. А. Багдасаров, П. С. Васильев, Д. М. Гроздов (1969); А. Н. Филатов, Ф. В. Баллюзек (1972).
Наибольшее практическое значение имеет классификация кровезаменителей по механизму лечебного действия, предложенная А. А. Багдасаровым, П. С. Васильевым, Д. М. Гроздовым и дополненная О. К. Гавриловым (1973):
I. Г емодинамические кровезаменители, производные:
—декстрана;
—желатина; -ГЭК;
—полиэтиленгликоля.
180
II. Регуляторы для коррекции водно-солевого баланса и КОС:
—электролитные растворы;
—раствор глюкозы 5 %;
—электролитные растворы с 5 % глюкозой;
—полуэлектролитные растворы с 5 % глюкозой;
—осмодиуретики.
III. Растворы для «малообъемной реанимации»:
—раствор натрия хлорида 7,2 %;
—растворы натрия хлорида 7,2 % и искусственных коллоидов.
IV. Инфузионные антигипоксанты:
—растворы фумарата;
—растворы сукцината.
V. Кровезаменители с функцией переноса кислорода:
—растворы гемоглобина;
—эмульсии перфторуглеродов.
VI. Кровезаменители комплексного действия.
VII. Препараты для парентерального питания:
—смеси аминокислот;
—жировые эмульсии;
—углеводы;
— смеси «все в одном» (аминокислоты, жиры и углеводы).
Гемодинамигеские кровезаменители предназначены для нормали
зации показателей центральной и периферической гемодинамики:
• лечения и профилактики абсолютной и относительной гипо-волемии;
• нормоволемической гемодилюции.
Они созданы на основе желатины, декстрана, ГЭК и полиэти-ленгликоля. Рецептура гемодинамических кровезаменителей определяет следующие их свойства:
• максимальную гемодинамическую эффективность (волемиче-ский эффект и его продолжительность, максимальную суточную дозу);
• побочные эффекты (прямое отрицательное воздействие на первичный и вторичный гемостаз, гемодилюцию, острое гиперонко-тическое повреждение почек, частоту анафилактоидных реакций и частоту зуда кожи и слизистых).
Волемический эффект (ВЭ) — отношение прироста ОЦК к объему введенной инфузионной среды в процентах (табл. 12). Волеми-ческий эффект и его продолжительность устанавливаются опытным путем на добровольцах, которым после удаления 400 мл крови переливали в течение 15 мин 500 мл кровезаменителя.
181
Таблица 12 Гемодинамическая эффективность коллоидов
| Производные | Молекулярный вес, тыс. Да/степень замещения | Волемиче-ский эффект, % | Продолжительность ВЭ, ч | Максимальная суточная доза, мл/кг массы тела |
| Желатины: | ||||
| гелофузин | 30 | 100 | 3-4 | 200 |
| желатиноль | 20 | 60 | 1-2 | 30 |
| Декстрана: | ||||
| полиглюкин | 60 | 120 | 4-6 | 20 |
| реополиглюкин | 35 | 140 | 3-4 | 12 |
| Гидроксиэтилкрахмала (ГЭК): | ||||
| венофундин (6 %) | 130/0,42 | 100 | 4 | 50 |
| волювен (6 %) | 130/0,4 | |||
| гемохес (6 %) | 200/0 5 | 100 | 4 | 33 |
| рефортан (6 %) | ||||
| гемохес (10 %) | 200/0,5 | 145/1ч | 4 | 20 |
| рефортан плюс (10 %) | 100/3 ч | |||
| ХАЕС-стерил 10 % | ||||
| стабизол (6 %) | 450/0,7 | 100 | 6-8 | 20 |
| Полиэтиленгликоля: | ||||
| полиоксидин | 20 | - | - | 20 |
Продолжительность волемигеского эффекта (плато) — время, в течение которого волемический эффект составит не менее 100 %.
Волемический эффект и его продолжительность служат для сравнения гемодинамических кровезаменителей между собой.
Максимальная сутогная доза для всех рассматриваемых гемодинамических кровезаменителей различна. В сочетании с кристаллоидами, компонентами и препаратами крови ими можно восполнять различную по величине кровопотерю (табл. 13). Однако на практике следует обязательно учитывать выраженность прямого отрицательного влияния на гемостаз декстранов и ГЭК.
К одному из побочных эффектов ряда кровезаменителей следует отнести их прямое отрицательное воздействие на первичный и вторичный гемостаз (табл. 14).
Декстраны уменьшают адгезивность тромбоцитов, снижают активность фактора Виллебранда, оказывают дезагрегантное действие на тромбоциты, снижают активность коагуляционной части молекулы фактора VIII, блокируют молекулу фибриногена, увеличивают чувствительность фибринового сгустка к лизису плазмином, оказы-
182
Таблица 13 восполнение кровопотери гемодинамическими кровезаменителями
| Производные | Молекулярный вес, тыс. Да/степень замещения | Максимальная суточная доза, мл/кг массы тела | Максимальная суточная доза, л/70 кг массы тела | Величина кровопотери, % ОЦК |
| Желатины: | ||||
| гелофузин | 30 | 200 | 14,0 | 400 |
| желатиноль | 20 | 30 | 2,1 | 150 |
| декстрана: | ||||
| полиглюкин | 60 | 20 | 1,4 | 100 |
| реополиглюкин | 35 | 12 | 0,84 | — |
| Гидроксиэтилкрахмала (ГЭК): | ||||
| венофундин (6 %) | 130/0,42 | 50 | 3,5 | 250 |
| волювен (6 %) | 130/0,4 | |||
| гемохес 6 % | 200/0,5 | 33 | 2,2 | 150 |
| рефортан (6 %) | ||||
| гемохес (10 %) | 200/0,5 | 20 | 1,4 | 100 |
| рефортан плюс (10 %) | ||||
| ХАЕС-стерил (10 %) | ||||
| стабизол (6 %) | 450/0,7 | 20 | 1,4 | 100 |
| Полиэтиленгликоля: полиоксидин | 20 | 20 | 1,4 | 100 |
Таблица 14
Прямое отрицательное воздействие на первичный и вторичный гемостаз
| Гемостаз | Лабораторные тесты | Коллоиды на основе | |||
| Желатина (гелофу- зин) | ГЭК 130/0,42 | ГЭК 200/0,5 | ГЭК 450/0,7; декстрана | ||
| Сосудисто-тромбоци- | Активность фактора Виллеб-ранда | - | 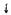
| 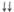
| 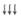
|
| тарный | Адгезия тромбоцитов | - | 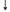
| 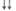
| 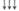
|
| Агрегация тромбоцитов | - | 
| 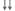
| 
| |
| Длительность кровотечения | - | 
| 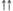
| 
| |
| Коагуля- | Строение фибринового сгустка | - | 
| 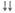
| 
|
| Ционный | Плотность тромба | - | 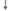
| 
| 
|
| Активность фактора VIII | - | 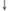
| 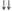
| 
| |
| Протромбиновое время | - | 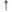
| 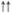
| 
| |
| АПТВ | — | 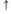
| 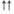
| 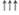
| |
Примечание: «—» — не оказывает;  — слабо выражено;
— слабо выражено; 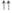 — умеренно выражено;
— умеренно выражено;  - выражено.
- выражено.
183
вают «силиконизирующий» эффект. Степень отрицательного воздействия декстранов находится в прямой зависимости от молекулярной массы и усиливается от реополиглюкина к полиглюкину.
ГЭК за счет «силиконизирующего» эффекта снижают адгезию и агрегацию тромбоцитов, активность факторов VIII и IX, антитром-бина-Ш и фибриногена. У ГЭК степень этого отрицательного воздействия находится в прямой зависимости не только от молекулярной массы, но и от степени замещения, и усиливается от 130/0,42 к 200/0,5 и 450/0,7. Согласно инструкциям, декстраны и ГЭК (200/0,5 и 450/0,7) противопоказаны при тяжелых геморрагических диатезах, а при использовании ГЭК 130/0,42 (Венофундин) следует соблюдать осторожность.
Производные желатины (гелофузин, желатиноль) и полиэти-ленгликоля (полиоксидин) не оказывают прямого отрицательного воздействия на первичный и вторичный гемостаз. В опытах in vitro при добавлении к донорской плазме от 6,7 об % до 37,5 об % гело-фузина не выявлено прямого снижения ристоцитин-кофакторной активности фактора Виллебранда, снижения обратимой и необратимой АДФ-агрегации тромбоцитов, удлинения АПТВ, снижения активности фактора VIII, удлинения протромбинового времени и снижения концентрации фибриногена. Следовательно, гелофузин является гемодинамическим кровезаменителем выбора при инфузи-онной терапии акушерских кровотечений, особенно обусловленных нарушением биологического гемостаза (ДВС-синдром, гемодилю-ционная коагулопатия, болезнь Виллебранда и др.).
Гемодилюционный эффект. Каждые в/в введенные 500 мл гемо-динамического кровезаменителя в течение 15 мин снижают гема-токрит в среднем на 4—6 %. При гемодилюционном снижении гема-токрита менее 28 % может развиться гемодилюционная коагулопатия и тромбоцитопения.
Коллоидно-осмотическое давление (КОД) создается белками плазмы крови (в основном альбумином) и является одним из регуляторов транскапиллярного обмена. Согласно закона Старлинга разница между силами фильтрации и реабсорбции на артериальном участке капилляра достигает 7 мм рт. ст. (под таким давлением жидкость из капилляров фильтруется в ткани), а на венозном -7—8 мм рт. ст. (под таким давлением жидкость из тканей поступает в сосудистое русло). Из 33 мм рт. ст. сил реабсорбции на долю КОД приходится 25 мм рт. ст. КОД в пределах нормы (16,7— 24,2 мм рт. ст.) имеют желатиноль (16,2—21,4 мм рт. ст.) и стабизол (18 мм рт. ст.). У 6 % ГЭК (130/0,42 и 200/0,5) КОД колеблется в пределах 28—36 мм рт. ст. Следовательно, при введении кровезаме-
184
«теля с КОД выше, чем у плазмы крови, создаются условия для поступления жидкости из интерстициального пространства в сосуди-стоерусло. Однако при применении гиперонкотических растворов:
декстранов, в особенности низкомолекулярного декстрана — реопо-лиглюкин (КОД составляет 90 мм рт. ст.); 10 % растворов ГЭК 200/0,5 (КОД составляет 65—80 мм рт. ст.) в большей степени характерно развитие так называемого синдрома острого гиперонкотигеско- го повреждения почек. Существует несколько гипотез патогенеза поражения почек при применении коллоидных растворов. По одной из них развитие острой почечной недостаточности (ОПН) связано с накоплением низкомолекулярных фракций в почечных канальцах и повышением осмолярности мочи, что и запускает некротические изменения в клетках канальцевого эпителия. По другой — поражение почек обусловлено дисбалансом между гидростатическим давлением (почечное перфузионное давление) и онкотическим давлением (плазмы крови) на мембране клубочков. Повышение онкотического давления плазмы связанно с применением гиперонкотических растворов вплоть до резорбции клубочковой фильтрации, что в конечном итоге приводит к ишемии и повреждению канальцевого эпителия.
При введении коллоидных кровезаменителей любого класса могут возникать анафилактоидные реакции (табл. 15). Согласно классификации Ринга и Мессмера, они делятся на легкие (1—2 степени) и угрожающие жизни, или тяжелые (3—4 степени). Частота (%) и тяжесть (1—4 степень) их возникновения должны быть указаны в инструкции по применению этих препаратов. Например, для альбумина - 0,099 %, желатиноля - 0,155 %, гелофузина - 0,0077 %, декстранов - до 7 %, ГЭК 200/0,5 - до 0,047 % и для ГЭК 450/0,7 — до 0,085 %. С целью профилактики анафилактоидных реакций следует проводить биологическую пробу.
Таблица 15 Степени анафилактоидных реакций по Рингу и Мессмеру (1977)
| Степень | Клинические проявления |
| 1 | Аллергическая реакция на коже |
| 2 | Не представляющая угрозы для жизни гемодинамическая реакция (гипотония, тахикардия), тошнота, рвота, респираторные нарушения (одышка), возбуждение, беспокойство, парестезия и боли |
| 3 | Бронхоспазм, судороги, потеря сознания, ангионевротический отек, отек гортани |
| 4 | Кардиопульмональный шок |
185
Длительное ежедневное применение ГЭК в средних (500 мл) и высоких (1000 мл) дозах (суммарная курсовая доза ГЭК более 300 г) может вызывать зуд кожи и гениталий различной интенсивности и продолжительности. Он связан с отложением молекул ГЭК по ходу нервов и проходит лишь после выведения или распада ГЭК Классические антигистаминные препараты, противозудные средства, ультрафиолетовая терапия и нейролептики оказываются бесполезными при лечении зуда данного типа.
Гидроксиэтилкрахмалы (130/0,42; 200/0,5 и 450/0,7) обладают цитопротекторными свойствами. Сильно разветвленные молекулы крахмала образуют «заклепки» в пространствах между клетками эндотелия по всей базальной мембране, эффективно устраняя транскапиллярную утечку, имеющую место при многих патологических состояниях, и защищая эндотелиоциты от повреждений различными агентами.
Основной путь выведения всех гемодинамических кровезаменителей — с мочой, только ГЭК вначале расщепляются амилазой крови до фракций. У больных с почечной недостаточностью наблюдается снижение элиминации кровезаменителей.
Показания для применения 6 %-го ГЭК и гелофузина зависят не только от уровня гиповолемии, но и от наличия у больной геморрагических диатезов (табл. 16).
Регуляторы водно-электролитного баланса и КОС предназначены для коррекции нарушений:
• водного обмена;
• электролитного обмена;
• КОС (метаболического ацидоза).
Таблица 16 Показания для применения 6 % ГЭК и гелофузина при гиповолемии
| Показания | Гелофузин | ГЭК 6 % 130/0,42 | ГЭК. 6 % 200/0,5 |
| Относительная гиповолемия | + | + | + |
| Абсолютная гиповолемия (< 30 % ОЦК) | + | + | + |
| Абсолютная гиповолемия (> 30 % ОЦК) | + | + | 1 |
| Абсолютная гиповолемия с доклинической стадией геморрагических диатезов | + | + | 1 |
| Абсолютная гиповолемия с коагулопатиче-ским кровотечением (ДВС, гемодилюция, отрицательное воздействие ГЭК и декстра-нов и др.) | + | 1 | 1 |
| Абсолютная гиповолемия с тромбоцитопе-ническим кровотечением | + | 1 | 1 |
Примечание: «+» — показано; «—» — не показано. 186
Эти растворы условно можно разделить на пять групп:
1) электролитные растворы;
2) электролитные концентраты;
3) осмодиуретики;
4) раствор глюкозы 5 %;
5) полуэлектролитные растворы.
Рецептура электролитных растворов (табл. 17, 18) определяет их свойства — осмолярность, изотоничность, ионность, резервную щелочность.
По отношению осмолярности электролитных растворов к крови они проявляют изо-, гипо- или гиперосмолярный эффект.
Изоосмолярный эффект. Вода, химически связанная с ионами, распределяется между внутрисосудистым и внесосудистым пространствами как 25 % к 75 %. Волемический эффект (прирост ОЦК к объему введенной инфузионной среды в %) составит 100 % при струйном введении и около 25 % через 30 мин после окончания введения. Эти растворы показаны при лечении гиповолемии (табл. 19).
В зависимости от содержания электролита в растворе они могут быть изотоническими (раствор натрия хлорида 0,9 %), гипотоническими (дисоль, ацесоль) и гипертоническими (раствор натрия хлорида 10 %, раствор калия хлорида 4 %, раствор натрия гидрокарбоната 4,2 и 8,4 %). Последние носят название электролитных концентратов и применяются как добавка к инфузионным растворам (раствору глюкозы 5 %, раствору Рингер-ацетата) непосредственно перед введением.
В зависимости от числа ионов в растворе различают моноионные (раствор натрия хлорида) и полиионные растворы (раствор Рингера и др.).
Введение в электролитные растворы носителей резервной щелочности позволяет проводить быструю (гидрокарбонат) и отсроченную (ацетат, лактат, малат) коррекцию метаболического ацидоза или поддерживать существующее КОС (см. табл. 17).
Изотонические электролитные растворы (см. табл. 17) в зависимости от состава применяются при:
• изотонической дегидратации внеклеточного пространства (за счет воды, химически связанной с ионами);
• нарушениях электролитного обмена (за счет ионов Na+, K+, Са2+, Mg2+, С1_);
• неизмененном КОС (за счет BE от -3 до +2,5 ммоль/л);
• метаболическом ацидозе (за счет BE более +3 ммоль/л).
187
Таблица 17 Изотонические электролитные растворы
| Показатель | Ингредиенты, ммоль/л | Осмо- лярность, мосм/л | |||||||
| Na+ | к+ | Са2+ | Mg2+ | С1- | НСО3 | Ацетат | BE | ||
| Внутриклеточное пространство | 10 | 150 | - | 30 | - | 10 | - | - | 300 |
| Внеклетогное пространство: | |||||||||
| интерстициальная жидкость | 145 | 4 | 2,5 | 1 | 116 | 29 | — | — | 298 |
| плазма крови | 136-143 | 3,5-5,0 | 2,38-2,63 | 0,75-1,1 | 96-105 | 24 + 2 | - | -3-+2.5 | 280-300 |
| натрия хлорид 0,9 % | 154 | - | - | - | 154 | - | - | -24 | 308 |
| рингер | 140 | 4 | 6 | - | 150 | - | - | -24 | 300 |
| рингер-ацетат | 131 | 4 | 2 | 1 | 111 | - | 30 | +6 | 280 |
| стерофундин | 140 | 4 | 2,5 | 1 | 127 | - | 24 + (5 малат) | 0 | 304 |
| изотонический | |||||||||
| ионостерил | 137 | 4 | 1,65 | 1,25 | 110 | - | 36,8 | +18 | 291 |
| плазмалит 148 | 140 | 5 | - | 1,5 | 98 | - | 27 + (23 глюко-нат) | +26 | 294 |
Таблица 18 Электролитные растворы (изотонические) с 5 % глюкозой
| Показатель |
| И | нгредиенты, ммоль/л | Осмо- лярность, мосм/л | ||||
| Na+ | К+ | Са2+ | Mg2+ | С1- | Глюкоза, г/л | НСО3- | ||
| Внутриклеточное пространство | 10 | 150 | - | 30 | - | - | 10 | 300 |
| Внеклетогное пространство: | ||||||||
| интерстициальная | 145 | 4 | 2,5 | 1 | 116 | - | 29 | 298 |
| жидкость | ||||||||
| плазма крови | 136-143 | 3,5-5,0 | 2,38-2,63 | 0,75-1,10 | 96-105 | - | 26-30 | 300 |
| плазмалит 148 | 140 | 5 | - | 1,5 | 98 | 50 | 27 ацетат | 564 |
| стерофундин Г-5 | 140 | 4 | 2,5 | 1 | 141 | 50 | 10 малат | 575 |
Таблица 19
Распределение воды между физиологическими пространствами организма через 30 мин после введения кровезаменителей
| Раствор | Осмолярность, мосм/л | Внеклеточное пространство | Внутриклеточное пространство | |
| Плазма, % | Интерстиций, % | |||
| Гемодинамические кровезаменители | 300 | 100 | - | - |
| Электролитный | 300 | 25 | 75 | - |
| 5 % глюкозы | 277 | 7 | 28 | 65 |
Таблица 20
Скорость введения и максимальные дозы изотонических электролитных растворов
| Наименование раствора | Скорость введения, кап./мл • мин"1 | При необходимости за 15 мин, мл | При необходимости мл/сут. |
| Натрия хлорид 0,9 % | 180/9 | До 500 | До 3000 |
| Рингер | 80/4 | - | - |
| Рингер-ацетат | 80/4 | - | — |
| Ионостерил | 60/3 | — | — |
| Плазмалит 148 | 80/4 | — | — |
| Стерофундин изотонический | 80/4 |
Изотонические электролитные растворы можно вводить как через периферические, так и через центральные вены. Скорость и максимальные суточные дозы взрослым приведены в табл. 20.
Электролитные растворы (изотонические) с 5 % глюкозой применяются при:
• изотонической или гипотонической дегидратации внеклеточного пространства;
• нарушениях электролитного обмена (за счет ионов Na+, K+, Са2+, Mg2+, C1-);
• метаболическом ацидозе (за счет ацетата, малата) и для частичного покрытия энергетической потребности.
Инфузионные антигипоксанты (мафусол, реамберин, стерофун-дин Г-5) предназначены для повышения энергетического потенциала клетки (табл. 21). Они выполняют следующие функции:
1) восстанавливают клеточный метаболизм, активируя адаптацию клетки к недостатку кислорода, за счет участия в реакциях обратимого окисления и восстановления в цикле Кребса;
Таблица 21 Инфузионные антигипоксанты
| Показатель | Ингредиенты, ммоль/л | Анти- гипоксант, ммоль/л | Осмо- ляр- ность, мосм/л | ||||
| Na* | к+ | Са2+ | Mg2+ | С1- | |||
| Плазма | 136-143 | 3,5-5,0 | 2,38-2,63 | 0,75-1,1 | 96-105 | — | 300 |
| Мафусол | 280 | 4 | - | 1,2 | 109 | 86 фумарат | 410 |
| Реамберин | 142,4 | 4,0 | 1,2 | 109 | 44,7 сукци-нат | 346 | |
| Стерофундин Г-5 | 140 | 4 | 2,5 | 1 | 141 | 10 малат 50 г/л глюкозы | 575 |
190
2) способствуют утилизации жирных кислот и глюкозы клетками;
3) нормализуют кислотно-щелочной баланс и газовый состав
крови;
4) дезагрегируют тромбоциты.
Инфузионные антигипоксанты показаны для лечения и профилактики абсолютной и относительной гиповолемии (кровопотеря, шок), гипоксических состояний различной этиологии и интоксикаций.
5.4. КОМПОНЕНТЫ КРОВИ
В АКУШЕРСКОЙ ПРАКТИКЕ
Компоненты крови — используемые для лечебных целей составляющие крови, которые могут быть приготовлены из цельной крови различными методами.
Среди компонентов крови можно выделить:
• клеточные компоненты (эритроциты, тромбоциты, лейкоциты);
• плазму;
• составляющие плазмы (криопреципитат, криосупернатантная плазма).
Эритроцитсодержащие компоненты (ЭК) предназначены для замещения кровопотери и лечения анемии.
В распоряжении врача может быть несколько ЭК (табл. 22).
Выбор ЭК для замещения кровопотери зависит от ее состава и свойств.
Массивная кровопотеря 25—30 % ОЦК, сопровождающаяся снижением уровня гемоглобина ниже 70—80 г/л, гематокрита ниже 25 % и возникновением циркуляторных нарушений, является показанием к трансфузии ЭК. Есть мнение, что при нормальном газообмене в легких критический уровень доставки кислорода тканям (Са О2) 10 мл/дл осуществляется при гемоглобине 65—70 г/л.
Одна доза перелитого донорского ЭК повышает содержание гемоглобина у реципиента в среднем на 10 г/л, а гематокрита на 4-6 %.
Следует применять нативные ЭК до 3 дней хранения в консерванте CPD (цитрат, фосфат, декстроза) или глюгицир, до 5 дней — в консерванте CPDA-1 (цитрат, фосфат, декстроза, аденин) и до 7 дней — в ресуспендирующем растворе SAGM. Эти рекомендации связаны с тем, что основную и ведущую роль в кислородотранс-портной функции донорских эритроцитов играет промежуточный компонент гликолиза — 2,3-бифосфоглицерат. Через 7 дней хранения в консерванте CPD или глюгицир, через 10 дней в консерванте СPDA-l и через 15 дней в ресуспендирующем растворе SAGM
191
Таблица 22 Состав эритроцитсодержащих компонентов
| Эритроцитсодержащие компоненты | Максимальный срок хранения, сут. | НЬ, г/доза | Остаточное содержание в дозе | ||
| лейкоцитов | тромбоцитов | плазмы | |||
| Эритроциты (эритроцитная масса) | 35/10 | >45 | > 2,5-109 | До 90 % | >70мл |
| Эритроциты с удаленным лейкотромбоцитарным слоем | 35/10 | >43 | < 1,2 • 109 | < 20 • 109 | >70мл |
| Эритроцитная взвесь | До 42 | >45 | > 2,5 • 109 | До 90 % | + |
| Эритроцитная взвесь с удаленным лейкотромбоцитарным слоем | 42/15 | >43 | < 1,2 -109 | < 20 -109 | + |
| Отмытые эритроциты | 1 | >40 | + | + | <0,5г белка (IgA < 0,2 мг) |
| Эритроциты, обедненные лейкоцитами | До 42 | >40 | < 1,0-106 | + | + |
| Криоконсервированные эритроциты | До 10 лет | >36 | < 0,1 - 109 | + | + |
| Эритроциты, полученные методом афереза | 42 | >40 | + | + | + |
содержание этого фермента снижается до уровня, при котором затрудняется диссоциация оксигемоглобина и передача кислорода тканям. Его содержание в донорских эритроцитах после переливания восстанавливается в кровотоке реципиента лишь через 12—24 ч.
ЭК должен быть перелит через фильтр с размером пор не более 170—200 мкм, так как с первых часов хранения спонтанно образуются агрегаты тромбоцитов. В течение суток в них включаются лейкоциты и затем вокруг тромбоцитарно-лейкоцитарных агрегатов формируются нити фибрина. В процессе последующего хранения число микроагрегатов размером от 4 до 200 мкм прогрессивно нарастает. Удаление при трансфузии микроагрегатов от 30 до 40 мкм предотвращает микротромбоэмболию сосудов легких и развитие респираторного дистресс-синдрома. Уменьшить число микроагрегатов можно двумя путями: 1) применять эритроциты с удаленным лейкотромбоцитарным слоем или обедненные лейкоцитами; 2) использовать при переливании эритроцитов микроагрегатные фильтры.
Применение эритроцитов, обедненных лейкоцитами (менее 1 • 106 в дозе) позволяет предотвратить ряд посттрансфузионных реакций и осложнений: HLA-аллоиммунизацию, гипертермическую
192
Таблица 23 Тромбоциты: восстановленные
| Тромбоциты: в | осстановленные | |
| Состав | из обогащенной тромбоцитами плазмы | из лейкотромбоцитар-ного слоя |
| Тромбоциты | > 60 • 109/ | цоза/40 мл |
| Лейкоциты | < 0,2 - 109/доза | < 0,05-109/доза |
| Лейкоциты (после удаления/ЛФ) | <0,2- | 106/доза |
негемолитическую реакцию, посттрансфузионную пурпуру, передачу цитомегаловируса и вируса Эпстайна — Барр, а также снизить частоту возникновения иммуносупрессии и респираторного дистресс-синдрома.
Тромбоциты: восстановленные — компонент донорской крови человека, полученный из цельной крови и содержащий в дозе большую часть тромбоцитов в терапевтически эффективной форме (табл. 23).
Восстановленные тромбоциты применяют при клинически значимом кровотечении, связанном с дефицитом тромбоцитов.
Доза перелитых донорских тромбоцитов увеличивает их число у реципиента на 7 • 109/л.
Свежезамороженная плазма (СЗП) — компонент донорской крови человека для переливания, полученный либо из цельной крови, либо из полученной методом афереза плазмы, замороженный в течение определенного периода времени при определенной температуре, гарантирующей сохранение функционального состояния лабильных факторов свертывания.
СЗП содержит альбумины, иммуноглобулины, а также не менее 70 % от исходного уровня фактора VIII и, по крайней мере, такое же количество других лабильных факторов свертывания и естественных ингибиторов. В дозе СЗП (250 мл) содержится в среднем 0,75 г фибриногена и не менее 150 ME фактора VIII.
Сроки ее хранения: 24 мес. при температуре ниже -25 °С, 3 мес. при температуре от -18 °С до -25 °С.
Размораживание СЗП можно осуществлять на водяной бане (37 °с в течение 20 мин) или с помощью быстрого размораживателя плазмы в течение 12—15 мин. Активность фактора VIII лучше сохраняется при использовании быстрого размораживателя плазмы.
Сразу после размораживания СЗП должна быть перелита через фильтр с размером пор не более 170—200 мкм. Повторное замораживание недопустимо.
193
 СЗП можно применять при нарушениях свертывания, особенно в тех клинических случаях, когда имеется дефицит нескольких фак. торов свертывания крови, и при отсутствии подходящего ви-рус-инактивированного стабильного препарата.
СЗП можно применять при нарушениях свертывания, особенно в тех клинических случаях, когда имеется дефицит нескольких фак. торов свертывания крови, и при отсутствии подходящего ви-рус-инактивированного стабильного препарата.
СЗП не должна использоваться:
• для коррекции дефицита ОЦК;
• при отсутствии дефицита факторов свертывания;
• в качестве источника иммуноглобулинов;
• у пациентов с непереносимостью белков плазмы.
Необходимо использовать только плазму, совместимую по сис
теме АВО.
Криопреципитат — компонент донорской крови человека, получаемый при последующей обработке СЗП и содержащий фракцию криоглобулинов плазмы.
Препарат содержит в дозе не менее 70 ME фактора VIII, не менее 0,14 г фибриногена, и основную часть фактора Виллебранда, фактора XIII и фибронектина.
Криопреципитат можно применять при:
• состояниях с дефицитом фактора VIII (гемофилия А, болезнь Виллебранда при недоступности соответствующих вирус-инактиви-рованных препаратов);
• других состояниях комплексного дефицита факторов свертывания, например ДВС;
• дефиците фибриногена (качественном и количественном).
Криосупернатантная плазма — компонент донорской крови че
ловека, приготовленный из плазмы удалением криопреципитата.
Препарат содержит такое же количество альбумина, иммуноглобулинов и факторов свертывания крови, как в СЗП, за исключением тех, которые остались в удаленном криопреципитате.
Сроки ее хранения: 24 мес. при температуре ниже -25 °С, 3 мес. при температуре от -18 °С до -25 °С.
Размораживание можно осуществлять на водяной бане (37 °С в течение 20 мин) или с помощью быстрого размораживателя плазмы в течение 12—15 мин.
Сразу после размораживания плазма должна быть перелита через фильтр с размером пор не более 170—200 мкм. Повторное замораживание недопустимо.
Препарат можно применять при приобретенных коагулопатиях, синдроме ДВС крови (при уровне фибриногена пациента выше 1,5 г/л).
Необходимо использовать только плазму, совместимую по системе АВО.
194
Информированное добровольное согласие пациента на гемотрансфу-зии. Основы законодательства Российской Федерации об охране здо-ровья граждан от 22 июля 1993 г. № 5487-1, приказы МЗ РФ, методические рекомендации Фонда обязательного медицинского страхования требуют предварительного информированного добровольного согла-сия (ИДС) пациента на любое медицинское вмешательство.
Переливание донорской крови и ее компонентов, даже без дефекта их проведения, сопряжены с развитием реакций и осложнений и требуют ИДС на их проведение.
Предлагаемая форма на ИДС не предусматривает риски, связанные с нарушениями методики и техники трансфузии.
Перед плановой манипуляцией или оперативным вмешательством, возможно, потребующим переливания донорской крови или ее компонентов, лечащий врач и (или) анестезиолог заполняет ИДС пациента (Приложение).
В экстренных ситуациях, требующих принятия срочных решений, когда состояние больного не позволяет ему выразить свою волю, а медицинское вмешательство неотложно, вопрос о переливании донорской крови или ее компонентов в интересах больного решает консилиум, а при невозможности собрать консилиум — непосредственно лечащий (дежурный) врач с последующим уведомлением должностного лица клиники.
Документы по ИДС вклеиваются в историю болезни.
Приложение






