МикроРНК обычно транскрибируются в виде предшественника длиной около 70 нуклеотидов, представляющего собой шпильку с несколькими одноцепочечными участками. Нередко район гена, кодирующий этот предшественник, расположен в одном из интронов регулируемого гена. Специальный фермент, носящий название Dicer (англ. «нарезающий кусочками»), вырезает из транскрипта участок длиной около двух десятков нуклеотидов. Получившаяся микроРНК почти полностью (за исключением очень маленького кусочка) комплементарна участку информационной РНК, считываемой с того гена, который нужно выключить. МикроРНК спаривается с мРНК, тем самым блокируя трансляцию (рис. 26, В).
Интерферирующие малые РНК. Одним из главных событий конца ХХ века в молекулярной биологии стало открытие так называемых малых интерферирующих РНК (si РНК). Оказалось, что это маленькие двуцепочечные РНК (дцРНК), которые могут полностью блокировать действие гена, копией части которого они являются. Обычно в клетках нет дцРНК, но если она там появится по какой-либо причине, в действие вступают особые ферменты. Если молекула дцРНК длинная, то уже знакомый нам фермент Dicer нарезает ее кусочками длиной 20-23 нуклеотида. Эти кусочки и являются siРНК. Затем к ним присоединяются два фермента – геликаза и нуклеаза. Геликаза – фермент, раскручивающий двойную спираль и отделяющий комплементарные цепочки друг от друга, а нуклеаза расщепляет нуклеиновые кислоты. После того, как геликаза разделит siРНК, одна из цепочек окажется связанной с нуклеазой. Этот комплекс присоединяется к комплементарному участку мРНК так, как это делают и регуляторные микроРНК. Нуклеаза, находящаяся в составе этого комплекса, разрезает мРНК, в результате чего трансляция ее оказывается невозможной. Нетрудно видеть, что механизм действия интерферерующих РНК очень похож на действие микроРНК, только в данном случае действие более «радикально» – не блокирование трансляции, а уничтожение мРНК (рис 26, Д).
Искусственное введение небольших двуцепочечных РНК-копий участка определенного гена сейчас широко используется исследователями для «прицельного» выключения именно этого гена. Однако откуда же берутся в клетке дцРНК в естественных условиях? Ведь наличие специального ферментативного комплекса в клетке указывает на его востребованность. Оказалось, что интерферирующие РНК эффективно защищают клетки растений и насекомых от вирусов – ведь у этих организмов нет антител и иммунитета в том виде, в каком он присущ позвоночным. Большинство вирусов растений и насекомых содержат именно РНК, а не ДНК. Правда, далеко не у всех вирусов РНК является двуцепочечной. Однако недавно было показано, что фермент Dicer обладает и другой ферментативной активностью – он может работать как РНК-зависимая РНК-полимераза, т[O29] о есть достраивать одноцепочечную РНК до двуцепочечной, которую затем нарезает кусочками. В клетках позвоночных животных с помощью этого механизма могут уничтожаться дефектные молекулы РНК или молекулы, ставшие ненужными. Пока неизвестно, как клетка различает те РНК, которые нужно достроить и уничтожить, от молекул РНК, необходимых в данное время.
Длинные регуляторные РНК. Использование новых современных методов изучения генома позволило ученым обнаружить у эукариот несколько сотен генов, кодирующих не белки и не те РНК, которые ранее уже были известны (рРНК, тРНК, miРНК, siРНК), а длинные регуляторные РНК. Этот новый класс РНК назвали lincРНК (англ. large intervening non-coding RNAs, большие промежуточные некодирующие РНК). Гены этих РНК оказались очень консервативными, то есть мало меняющимися в ходе эволюции. Это указывает то, что функции их жизненно важны, поэтому большинство мутаций в них отметаются отбором. Точная функция и механизм действия большинства lincРНК пока неизвестны, однако было показано, что они участвуют в регуляции самых разных процессов в клетке – клеточного деления, образования гамет, дифференцировки стволовых клеток, репарации ДНК, транспорта веществ из цитоплазмы в ядро, уничтожения дефектных или ставших ненужными клеток. Они участвуют в работе иммунной системы, росте мышц, функционировании нервной системы. Для некоторых lincРНК детали функционирования известны более подробно. Об этом будет рассказано позднее (§ 27).
§ 14. Принципы репликации.
Преемственность генетического материала в поколениях клеток и организмов обеспечивается процессом репликации – удвоения молекул ДНК с помощью фермента ДНК-полимеразы. В результате этого сложного процесса, осуществляемого комплексом десятков ферментов и не обладающих каталитической активностью белков, необходимых для придания полинуклеотидным цепям нужной конформации, образуются две идентичные двойные спирали ДНК. Репликация происходит в клетке перед делением, поэтому каждая дочерняя клетка получает точно такие же молекулы ДНК, какие имела материнская клетка.
Как и все матричные синтезы (см. § 6), процесс репликации ДНК основан на принципах комплементарности, антипараллельности и униполярности (рис. 27, А). Это означает, что: 1) каждая из двух цепей «материнской» молекулы ДНК служит матрицей для синтеза дополняющей ее, то есть комплементарной, «дочерней» цепи; 2) синтезируемая дочерняя цепь ориентирована антипараллельно матричной (напротив 3'-конца матричной цепи находится 5'-конец дочерней); 3) передвижение ДНК-полимераз – ферментов, синтезирующих новые нити ДНК, возможно лишь в одном направлении – от 3'-концов к 5'-концам матричных цепей. При этом синтез комплементарных нитей всегда ведется в направлении 5'→3'
Кроме этих общих принципов, для репликации характерны и другие, связанные с уникальностью строения молекул ДНК.
Полуконсервативность. В ходе репликация двойная спираль ДНК разделяется на отдельные цепочки, каждая из которых служит матрицей для построения новой, «дочерней» цепи. В результате репликации образуются две идентичные двойные дочерние спирали, в каждой из которых одна из цепей – сохраненная («законсервированная») материнская, та, которая представляла собой половину материнской молекулы. Вторые цепи дочерних молекул – новые, синтезированные из дезоксирибонуклеотидов заново по принципу комплементарности к нитям материнской ДНК. Новые молекулы ДНК ничем не отличаются друг от друга и от материнской двойной спирали (рис 27, А).
Прерывистость. Для того чтобы новые нити ДНК были построены по принципу комплементарности, двойная спираль должна быть раскручена и между родительскими цепями должны отсутствовать водородные связи. Только в этом случае ДНК-полимеразы способны двигаться по материнским нитям и использовать их в качестве матрицы для безошибочного синтеза дочерних цепей. Длина каждой молекулы ДНК любой клетки очень велика, превышая размеры самой клетки во много раз. Например, длина каждой из 46 молекул ДНК человека составляет примерно от 2 до 10 сантиметров, в них содержится от 5 до почти 30 миллионов витков спирали! Раскрутить столько витков от начала до конца
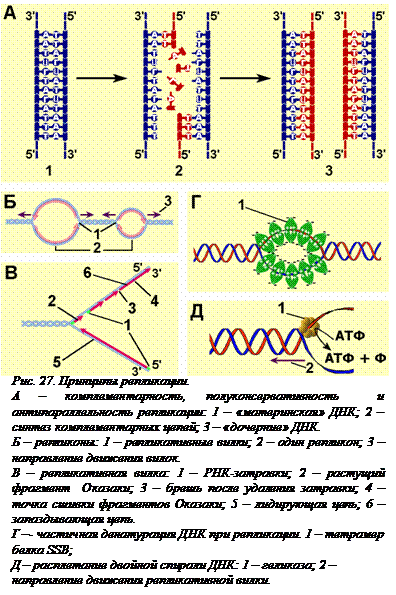 невозможно. И репликация самой короткой двухсантиметровой молекулы от одного конца до другого длилась бы почти две недели. Полное раскручивание спиралей, состоящих из многих миллионов пар нуклеотидов, сопряжено со столь значительным количеством вращений и такими энергетическими затратами, которые невозможны в условиях клетки. Поэтому репликация начинается одновременно в нескольких местах молекулы ДНК. Участок между двумя точками, в которых начинается синтез дочерних цепей, называется репликоном (рис. 27, Б). В эукариотической клетке в каждой молекуле ДНК в зависимости от размеров имеются сотни и даже тысячи репликонов. Репликоны в одной молекуле активируются по расписанию, заданному генетической программой.
невозможно. И репликация самой короткой двухсантиметровой молекулы от одного конца до другого длилась бы почти две недели. Полное раскручивание спиралей, состоящих из многих миллионов пар нуклеотидов, сопряжено со столь значительным количеством вращений и такими энергетическими затратами, которые невозможны в условиях клетки. Поэтому репликация начинается одновременно в нескольких местах молекулы ДНК. Участок между двумя точками, в которых начинается синтез дочерних цепей, называется репликоном (рис. 27, Б). В эукариотической клетке в каждой молекуле ДНК в зависимости от размеров имеются сотни и даже тысячи репликонов. Репликоны в одной молекуле активируются по расписанию, заданному генетической программой.
В каждом репликоне можно видеть репликативную вилку – ту часть молекулы ДНК, которая под действием специальных ферментов уже расплелась. Каждая нить в вилке служит матрицей для синтеза комплементарной дочерней цепи. Именно в репликативной вилке работает ферментативный комплекс, обеспечивающий репликацию ДНК. В ходе репликации вилка перемещается вдоль материнской молекулы, при этом расплетаются новые участки ДНК. Так как ДНК-полимеразы могут двигаться лишь в одном направлении вдоль матричных нитей, а нити ориентированы антипараллельно, то в каждой вилке одновременно ведут синтез два по-разному организованных репликативных ферментативных комплекса. Одна дочерняя цепь (лидирующая) растет непрерывно, а другая (отстающая) – в виде фрагментов длиной в несколько сотен нуклеотидов, названных в честь открывшего их японского ученого фрагментами Оказаки (рис. 27, В). После действия ферментов, изменяющих структуру фрагментов, они сшиваются ДНК-лигазой, образуя непрерывную цепь. Такой механизм синтеза дочерних цепей ДНК фрагментами называют прерывистым.
Потребность в затравке. Все существующие ДНК-полимеразы не способны начинать синтез ни лидирующей цепи, ни фрагментов Оказаки отстающей цепи. Они могут лишь наращивать уже имеющуюся полинуклеотидную нить, последовательно присоединяя дезоксирибонуклеотиды к ее 3'-ОН-концу. Откуда же берется начальный 5'-концевой участок растущей цепи? Его синтезирует особая форма РНК-полимеразы, называемая ДНК-праймазой (от англ. primer – затравка). Размер рибонуклеотидной затравки невелик (< 20 нуклеотидов) в сравнении с размером цепи ДНК, образуемой ДНК-полимеразой. Выполнившая свою функцию РНК-затравка удаляется специальным ферментом, а образованная при этом брешь заделывается ДНК-полимеразой, использующей в качестве затравки 3'-ОН-конец соседнего фрагмента Оказаки.
Белки, участвующие в репликации. Кроме уже упомянутых ДНК-полимеразы, праймазы и лигазы в сложном процессе репликации участвуют и другие белки. Во время репликации обе нити молекулы ДНК должны быть в одноцепочечном состоянии, чтобы служить матрицами для синтеза дочерних цепей. Это значит, что двуцепочечную ДНК нужно частично денатурировать (часто говорят «расплавить») и удерживать нити от спаривания. Это делается с помощью специальных белков – SSB - белков, геликаз и гираз. SSB -белки (англ. single strand binding – связывающиеся с одной нитью)или белки Альбертса, обнаруженные в 1968 г., снижают температуру плавления ДНК на 20-40ºС. SSB -белки представляют собой тетрамеры – объединение четырех субъединиц. Они содержат кластер положительно заряженных аминокислотных остатков, благодаря чему они связываются с ДНК, являющейся полианионом, электростатически. Эти белки имеют повышенное сродство к одноцепочечной ДНК. С двуцепочечной ДНК, не имеющей расплавленных участков, белок не связывается. Но если есть одноцепочечная ДНК, то белки легко садятся на нее и выпрямляют ее, мешая восстановлению двойной спирали. Когда в ДНК образуется расплавленный участок, белок покрывает его сплошным слоем. Молекулы белка, сидящие на комплементарных цепях, не дают им схлопнуться, так как имеют мощный суммарный отрицательный заряд (рис. 27, Г). Участие SSB в репликации абсолютно необходимо. Они не только удерживают матричные цепи ДНК в репликативной вилке в одноцепочечном состоянии, но и защищают одноцепочечную ДНК от действия нуклеаз. Кроме того, они избирательно стимулируют работу ДНК-полимеразы.
Геликазы. Геликазы – это ферменты, денатурирующие ДНК. Геликаза, сидя на одной из цепей ДНК, продвигается вперед, нарушая при этом водородные связи и разделяя цепочки ДНК(рис. 27, Д). Для движения по двойной спирали ДНК и разрушения водородных связей она использует энергию АТФ. Геликаза не может начать плавление нативной ДНК, в которой нет одноцепочечных участков, так как ей нужна посадочная площадка – небольшой район, где цепи ДНК отошли друг от друга. Откуда берется такая площадка в нативной ДНК? Эта проблема решается с помощью топоизомераз.
 Топоизомеразы. Топоизомеразы – это ферменты, изменяющие топологию ДНК. Они меняют число зацеплений одной цепи за другую. Все топоизомеразы делятся на два класса: релаксазы, уменьшающие число зацеплений и гиразы, увеличивающие число зацеплений. Гиразы узнают определенные последовательности нуклеотидов и делают разрезы в обеих цепях ДНК. После разрыва цепей гираза поворачивает концы ДНК на 360º и снова сшивает цепи ДНК. В этом процессе используется энергия АТФ. Увеличение числа витков в замкнутой молекуле приводит к возникновению в ней напряжения, которое релаксируется путем закручивания всего кольца в противоположном направлении – образования суперспирали (рис. 28, А-В). Суперспирализация приводит к снятию напряжения в закрученной гиразами молекуле, а освобождающаяся механическая энергия идет на плавление «легкоплавких» АТ-богатых участков. Все это возможно только в кольцевых молекулах или в линейных, но концы которых закреплены и не могут свободно вращаться.
Топоизомеразы. Топоизомеразы – это ферменты, изменяющие топологию ДНК. Они меняют число зацеплений одной цепи за другую. Все топоизомеразы делятся на два класса: релаксазы, уменьшающие число зацеплений и гиразы, увеличивающие число зацеплений. Гиразы узнают определенные последовательности нуклеотидов и делают разрезы в обеих цепях ДНК. После разрыва цепей гираза поворачивает концы ДНК на 360º и снова сшивает цепи ДНК. В этом процессе используется энергия АТФ. Увеличение числа витков в замкнутой молекуле приводит к возникновению в ней напряжения, которое релаксируется путем закручивания всего кольца в противоположном направлении – образования суперспирали (рис. 28, А-В). Суперспирализация приводит к снятию напряжения в закрученной гиразами молекуле, а освобождающаяся механическая энергия идет на плавление «легкоплавких» АТ-богатых участков. Все это возможно только в кольцевых молекулах или в линейных, но концы которых закреплены и не могут свободно вращаться.
Репликация ДНК прокариот начинается с того, что в суперспирализованной благодаря работе гиразы кольцевой двуцепочечной молекуле плавится АТ-богатый участок, на который сразу же садятся SSB -белки. Этот участок называют ori (англ. origin – начало). Его размер – 245 пар нуклеотидов. Молекула ДНК Е. coli имеет один участок начала репликации и две расходящиеся в противоположных направлениях репликативные вилки (рис. 28, Г). В клетках прокариот существует три разных ДНК-полимеразы (полимеразы I, II и III). В репликативных вилках работает полимераза III.
Поскольку ДНК прокариот кольцевая, то когда репликация заканчивается, вилки встречаются, и лигаза соединяет синтезированные цепи. Осуществляющая репликацию ДНК-полимераза III образует асимметричный димер и одновременно ведет непрерывный синтез лидирующей цепи и фрагментов Оказаки запаздывающей цепи. Удаление РНК-затравок и заделывание образующихся при этом брешей берет на себя ДНК-полимераза I. Фрагменты Оказаки сшиваются лигазой.
§ 15. Особенности репликации у эукариот.
 Репликация у эукариот имеет некоторые особенности. Во-первых, ДНК эукариот во много раз длиннее ДНК прокариот, а ДНК-полимеразы работают на порядок медленнее, чем прокариотические. Казалось бы, что репликация у эукариот должна занимать гораздо больше времени. Но это не так. Дело в том, что, кольцевая молекула ДНК прокариот представляет собой один репликон. В линейной ДНК эукариот репликонов много. У них в каждой молекуле ДНК не один, как у прокариот, а много районов ori и репликативных вилок, в которых синтез идет одновременно (рис. 29, табл. 4). Во-вторых, ДНК эукариот линейная, то есть, не замкнута в кольцо, а мы знаем, что для посадки геликазы на ДНК требуется плавление участка ori. У эукариот линейные молекулы ДНК в ядрах с помощью специальных белков во многих местах прикреплены к ядерной мембране. Этим достигается топологическая замкнутость участков молекулы, без чего невозможно образование супервитков. В каждом отдельном участке ДНК между местами прикрепления есть свой ori. Участок ДНК между двумя ori – это отдельный репликон. Следовательно, каждая эукариотическая хромосома является полирепликоном. За счет этого время репликации ДНК E. сoli и человека соизмеримо, хотя в клетке человека ДНК в 1000 раз больше.
Репликация у эукариот имеет некоторые особенности. Во-первых, ДНК эукариот во много раз длиннее ДНК прокариот, а ДНК-полимеразы работают на порядок медленнее, чем прокариотические. Казалось бы, что репликация у эукариот должна занимать гораздо больше времени. Но это не так. Дело в том, что, кольцевая молекула ДНК прокариот представляет собой один репликон. В линейной ДНК эукариот репликонов много. У них в каждой молекуле ДНК не один, как у прокариот, а много районов ori и репликативных вилок, в которых синтез идет одновременно (рис. 29, табл. 4). Во-вторых, ДНК эукариот линейная, то есть, не замкнута в кольцо, а мы знаем, что для посадки геликазы на ДНК требуется плавление участка ori. У эукариот линейные молекулы ДНК в ядрах с помощью специальных белков во многих местах прикреплены к ядерной мембране. Этим достигается топологическая замкнутость участков молекулы, без чего невозможно образование супервитков. В каждом отдельном участке ДНК между местами прикрепления есть свой ori. Участок ДНК между двумя ori – это отдельный репликон. Следовательно, каждая эукариотическая хромосома является полирепликоном. За счет этого время репликации ДНК E. сoli и человека соизмеримо, хотя в клетке человека ДНК в 1000 раз больше.
|
Таблица 4. Характеристики репликонов у про- и эукариот
| |||
| Организм | Количество репликонов | Средний размер репликона, тыс. пар нуклеотидов | Скорость движения репликативной вилки п.н./мин. |
| E. сoli | 1 | 4200 | 50000 |
| Дрожжи | 500 | 40 | 3600 |
| Дрозофила | 3500 | 40 | 2600 |
| Лягушка | 15000 | 200 | 500 |
| Мышь | 25000 | 150 | 2200 |
| Бобы | 35000 | 300 | 2200 |
Как и у прокариот, в каждом репликоне синтез ДНК идет непрерывно по лидирующей цепи и прерывисто по запаздывающей. Отличие заключается в том, что размер фрагментов Оказаки (200-400 нуклеотидов) у эукариот меньше, чем у прокариот (1000-2000 нуклеотидов), а скорость работы ДНК-полимеразы на порядок ниже, чем у прокариот (табл. 4).
У эукариот РНК-затравки удаляются специальной РНК-азой Н (от англ. hybrid), узнающей «гибридные», то есть те, в которых одна нить ДНК, а другая – РНК, участки молекулы. Бреши заделываются специальной ДНК-полимеразой, а фрагменты Оказаки сшиваются лигазой.
Недорепликация 3'-концов матрицы. Удаление крайних РНК-праймеров, комплементарных 3'-концам обеих цепей линейной «материнской» молекулы ДНК, приводит к тому, что дочерние цепи оказываются короче на 10-20 нуклеотидов (у разных видов размер РНК-затравок различен). Поэтому все эукариотические линейные молекулы ДНК всегда имеют выступающий на размер праймера 3’-конец (рис. 30, А). Это порождает проблему недорепликации концов линейных молекул. Ведь в каждом следующем раунде репликации новая молекула ДНК оказывается короче на длину праймера. В случае репликации кольцевых бактериальных ДНК этой проблемы не существует, так как первые по времени образования РНК-затравки удаляются ферментом, который одновременно заполняет образующуюся брешь путем наращивания 3'-ОН-конца растущей цепи ДНК, направленной в «хвост» удаляемому праймеру. Для того чтобы генетическая информация в линейных молекулах не терялась, нужны особые меры для восстановления недореплицированнх концов.
 Теломераза. Проблема недорепликации3'-концов линейных молекул ДНК решается эукариотическими клетками с помощью специального фермента – теломеразы. Этот фермент был обнаружен у равноресничной инфузории Tetrahymena thermophila, а впоследствии – в клетках дрожжей, растений и животных. Теломераза является ДНК-полимеразой, достраивающей 3'-концы линейных молекул ДНК хромосом короткими (6-8 нуклеотидов) повторяющимися последовательностями. У позвоночных таким повтором служит некодирующая последовательность нуклеотидов TTAГГГ. Помимо белковой части теломераза содержит РНК, включающую повторы ААУЦЦЦ, комплементарные теломерным повторам в ДНК. Эта РНК выполняет роль матрицы для наращивания ДНК повторами. Длина теломеразной РНК колеблется от 150 нуклеотидов у простейших до 1400 нуклеотидов у дрожжей, у человека – 450 нуклеотидов. Сам факт наличия в молекуле РНК последовательности, по которой идет матричный синтез куска ДНК, позволяет отнести теломеразу к своеобразной обратной транскриптазе, то есть ферменту, способному вести синтез ДНК по матрице РНК.
Теломераза. Проблема недорепликации3'-концов линейных молекул ДНК решается эукариотическими клетками с помощью специального фермента – теломеразы. Этот фермент был обнаружен у равноресничной инфузории Tetrahymena thermophila, а впоследствии – в клетках дрожжей, растений и животных. Теломераза является ДНК-полимеразой, достраивающей 3'-концы линейных молекул ДНК хромосом короткими (6-8 нуклеотидов) повторяющимися последовательностями. У позвоночных таким повтором служит некодирующая последовательность нуклеотидов TTAГГГ. Помимо белковой части теломераза содержит РНК, включающую повторы ААУЦЦЦ, комплементарные теломерным повторам в ДНК. Эта РНК выполняет роль матрицы для наращивания ДНК повторами. Длина теломеразной РНК колеблется от 150 нуклеотидов у простейших до 1400 нуклеотидов у дрожжей, у человека – 450 нуклеотидов. Сам факт наличия в молекуле РНК последовательности, по которой идет матричный синтез куска ДНК, позволяет отнести теломеразу к своеобразной обратной транскриптазе, то есть ферменту, способному вести синтез ДНК по матрице РНК.
Как уже было сказано, все линейные молекулы ДНК имеют
выступающие однонитевые 3'-концы материнских цепей. Они-то и узнаются теломеразой, которая последовательно наращивает материнские цепи, используя 3'-ОН-концы их в качестве затравок, а РНК, входящую в состав фермента, в качестве матрицы. Образующиеся длинные одноцепочечные концы, в свою очередь, служат матрицами для синтеза дочерних цепей по традиционному репликативному механизму.
Как это происходит? Сначала выступающий конец ДНК, содержащий теломерные повторы, комплементарно связывается с матричным участком теломеразной РНК, затем теломераза наращивает ДНК, используя в качестве затравки ее 3'-ОН-конец, а в качестве матрицы – РНК, входящую в состав фермента. После этого происходит перемещение удлиненной ДНК относительно фермента. Следом снова идет удлинение и очередное перемещение. Таким образом, теломераза наращивает и без того выступающий конец ДНК. Новый раунд репликации начнется с нового конца, который теперь намного дальше прежнего начала репликации (рис. 30, Б). Поэтому то, что было недореплицировано раньше, дореплицируется. Но «ступенька» на конце молекулы все равно останется.
В результате образуются специализированные концевые структуры хромосом – теломеры. Они состоят из многократно повторенных коротких последовательностей ДНК и специфических белков (см. § 19). Поскольку теломерные последовательности нуклеотидов не являются кодирующими, они выступают в роли буферной зоны как защита от проблемы концевой репликации. Укорочение ДНК в ходе каждого раунда репликации лишь сокращает нетранскрибируемый текст теломеры, но не приводит к утрате смысловых последовательностей – генов и регуляторов их экспрессии. Таким образом, репликация обеспечивает передачу всего генетического материала в поколениях клеток и организмов.
§ 16. Репарация ДНК.
Молекулы ДНК – единственные макромолекулы, в самой структуре которых заложена способность к устранению повреждений и восстановлению исходной формы. Осуществляется это с помощью особого процесса – репарации. Комплементарность цепей в двойной спирали позволяет исправить повреждение, возникшее в одной из цепей, по матрице другой цепи. Если же повреждения возникают одновременно в одном месте обеих цепей, то такие дефекты не исправляются и могут быть причиной гибели клетки. К счастью, такие повреждения чрезвычайно редки.
 Апуринизация. Наиболее частым повреждением ДНК является апуринизация – потеря пуриновых оснований. Она может происходить спонтанно. В каждой соматической клетке человека теряется за сутки около 5000 аденинов и гуанинов, а при повышении температуры в результате болезни это количество увеличивается до 10000. Происходит это при разрыве N-гликозидной связи между пурином и дезоксирибозой. В сто раз реже из ДНК выщепляются пиримидины.
Апуринизация. Наиболее частым повреждением ДНК является апуринизация – потеря пуриновых оснований. Она может происходить спонтанно. В каждой соматической клетке человека теряется за сутки около 5000 аденинов и гуанинов, а при повышении температуры в результате болезни это количество увеличивается до 10000. Происходит это при разрыве N-гликозидной связи между пурином и дезоксирибозой. В сто раз реже из ДНК выщепляются пиримидины.
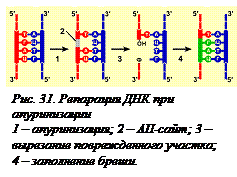
После отщепления азотистого основания в цепи образуется АП-сайт (апуриновый или апиримидиновый участок). Специфическая репарационная эндонуклеаза расщепляет сахарофосфатный остов в АП-сайте с образованием 3’-гидроксильного и 5’-фосфатного концов. Начиная с 5’-фосфатного конца, экзонуклеаза отщепляет дезоксирибофосфат, у которого нет азотистого основания, и еще 2-3 нуклеотида. Образующаяся брешь в 3-4 нуклеотида заделывается специальной репарационной ДНК-полимеразой, которая использует 3’-гидроксильный конец в качестве затравки. В заключение лигаза сшивает концы, и цепь оказывается восстановленной (рис. 31). Если бы АП-сайт сохранялся, то после репликации одна из дочерних цепей ДНК была бы короче на один нуклеотид, а после второй репликации появилась бы молекула, лишенная одной комплементарной пары. Это изменило бы весь смысл генетической информации, закодированной в поврежденном гене.
Дезаминирование. Под действием химических веществ, попадающих в клетку из окружающей среды, таких как алкилирующие агенты (азотистые соединения, нитрозомочевина), при изменении рН в ядре клетки, увеличении температуры может происходить дезаминирование азотистых оснований в составе ДНК.
В результате дезаминирования аденин превращается в гипоксантин, который образует две водородные связи с цитозином. Поэтому во время репликации вместо тимина, который был против аденина, включится цитозин, что приведет к замене комплементарной пары 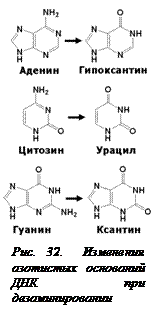 нуклеотидов АТ на другую комплементарную пару ГЦ.Дезаминирование гуанина превращает его в ксантин, образующий водородные связи с тимином, а при дезаминировании цитозина образуется урацил. В обоих случаях после репликации пара нуклеотидов ГЦ окажется замененной на пару АТ (рис. 32). Тимин – единственное основание в ДНК, которое не может быть дезаминировано. Если бы дезаминированные основания сохранялись в ДНК, то через две репликации вместо пары АТ стояла бы пара ГЦ; на месте пары ГЦ появилась бы пара АТ, а пара ЦГ была бы заменена на пару ТА. При транскрипции ошибка переписывалась бы в РНК и при трансляции могла бы приводить к замене одной аминокислоты на другую. Замены аминокислот могут сказаться на структуре белка и выполнении им своей функции.
нуклеотидов АТ на другую комплементарную пару ГЦ.Дезаминирование гуанина превращает его в ксантин, образующий водородные связи с тимином, а при дезаминировании цитозина образуется урацил. В обоих случаях после репликации пара нуклеотидов ГЦ окажется замененной на пару АТ (рис. 32). Тимин – единственное основание в ДНК, которое не может быть дезаминировано. Если бы дезаминированные основания сохранялись в ДНК, то через две репликации вместо пары АТ стояла бы пара ГЦ; на месте пары ГЦ появилась бы пара АТ, а пара ЦГ была бы заменена на пару ТА. При транскрипции ошибка переписывалась бы в РНК и при трансляции могла бы приводить к замене одной аминокислоты на другую. Замены аминокислот могут сказаться на структуре белка и выполнении им своей функции.
В клетке имеются специфические N-гликозилазы – ферменты, расщепляющие гликозидную связь между дезаминированным основанием и дезоксирибозой. Это гипоксантин-N-гликозилаза, ксантин-N-гликозилаза и урацил-N-гликозилаза. Они узнают «испорченное» основание и отщепляют его, в результате чего образуется АП-сайт. Он «лечится» теми же ферментами, которые работают при апуринизации.
Образование тиминовых димеров. Под действием на ДНК ультрафиолетового света происходит сшивание пиримидинов, стоящих рядом в одной цепи молекулы. При сшивании двух тиминов образуется циклобутановое производное, блокирующее репликацию, а, следовательно, и передачу генетической информации следующему поколению клеток и организмов (рис. 33).
 У бактерий и низших эукариот тиминовые димеры удаляются путем прямой фоторепарации. Фермент фотолиаза узнает тиминовые димеры и образует с ними комплекс. При освещении видимым светом в диапазоне длин волн 300-600 нм происходит активация фермента, циклобутановое кольцо разрывается и вновь получается два тимина.
У бактерий и низших эукариот тиминовые димеры удаляются путем прямой фоторепарации. Фермент фотолиаза узнает тиминовые димеры и образует с ними комплекс. При освещении видимым светом в диапазоне длин волн 300-600 нм происходит активация фермента, циклобутановое кольцо разрывается и вновь получается два тимина.
У бактерий существует и другой механизм ликвидации тиминовых димеров. Он называется эксцизионной репарацией. Его суть в том, что из поврежденной цепи ДНК вырезается (эксцизия – вырезание) фрагмент, содержащий тиминовый димер, и образующаяся брешь в 12-14 нуклеотидов заделывается ДНК-полимеразой, использующей в качестве матрицы неповрежденную цепь. Лигаза сшивает концы, и следов от повреждения не остается.
По такому же механизму осуществляется удаление тиминовых димеров у высших эукариот. У млекопитающих по меньшей мере девять разных генов кодируют ферменты эксцизионной репарации. Мутация в одном из них, нарушающая процесс репарации, является причиной тяжелой наследственной болезни человека – пигментной ксеродермы. Люди, страдающие этим заболеванием, очень чувствительны к ультрафиолетовому свету. Даже при слабом воздействии солнечных лучей у них развиваются различные повреждения кожи, в том числе и разные формы рака кожи.
Под действием ионизирующей радиации или рентгеновских лучей в ДНК возникают одноцепочечные и двуцепочечные разрывы сахарофосфатного скелета. Азотистые основания при этом могут оставаться неповрежденными. Одноцепочечные разрывы сшиваются лигазой, а двуцепочечные могут привести к фрагментации хромосом и даже к гибели клетки.
Глава II. Гены и геномы
§ 17. Гены и геномы.
Гены. Что такое ген? После того, как была установлена химическая природа наследственного вещества и доказана материальная природа гена, определения гена менялись несколько раз. Первоначальное определение «один ген – один признак» очень быстро оказалось слишком расплывчатым и, в общем случае, неверным, так как за развитие одного признака может отвечать несколько генов, а один ген может оказывать влияние на развитие нескольких признаков. Определение «один ген – один фермент» также оказалось неверным, так как очень многие ферменты – белки с четвертичной структурой, и поэтому являются продуктом нескольких разных генов. А после открытия нетранслируемых генов, например, генов транспортных или рибосомных РНК, а также альтернативного сплайсинга, и определение «один ген – одна полипептидная цепь» также нельзя считать верным. Так как у бактерий нет сплайсинга, то для прокариот возможно определение «ген – участок ДНК, кодирующий первичную структуру одной полипептидной цепочки или одной рРНК или одной тРНК». Для эукариот ген можно определить как участок ДНК, с которого считывается одна функциональная молекула РНК. Эта молекула потом может подвергаться сплайсингу и редактированию, благодаря чему может синтезироваться несколько разных полипептидных цепочек, закодированных в одном гене. У прокариот одна молекула РНК может считываться с нескольких генов, составляющих оперон (см. § 6). У многих вирусов все гены транскрибируются и затем транслируются в виде одной гигантской молекулы полипротеина, которая потом разрезается на отдельные белки.
У прокариот ген устроен довольно просто – промотор, оператор, структурная часть (белок-кодирующая область) и терминатор. При этом регуляторные части гена (промотор, оператор, терминатор) есть не у всех генов. Это связано с тем, что гены прокариот образуют структурно-функциональные блоки – опероны. В состав одного оперона входят гены, кодирующие белки, участвующие в одной биохимической цепи реакций, или разные рРНК или несколько тРНК. Каждый оперон является единицей транскрипции, то есть по нему образуется одна непрерывная молекула РНК, в которой может быть закодировано несколько белков, рибосомные или транспортные РНК. Поэтому и регуляторные участки являются общими для всех генов одного оперона. Кроме того, некоторые гены, продукты которых нужны клетке постоянно, работают все время и являются нерегулируемыми (в их опероне нет оператора). Общая длина транскрибированной РНК незначительно отличается от длины самого гена (не транскрибируются промотор и часть терминатора). В считанной РНК также есть 5’- и 3’-нетранслируемые области.






