ВВЕДЕНИЕ
Биология – наиболее стремительно развивающаяся область естествознания. Двадцатый век – век бурного прогресса науки. Основной вопрос естественных наук – физики, химии, биологии – можно сформулировать так: «Как устроена и работает материя?». Среди наиболее стремительно развивающихся наук о природе, несомненно, первое место занимает биология. Не случайно эксперты считают, что XXI век будет «веком биологии».
С древнейших времен существовала и развивалась единая наука о природе – та самая, которую позже, в античные времена назвали «физика», а сейчас можно назвать «естествознание». Биологии как таковой не было, а те науки, которые сейчас относят к кругу биологических, являлись частью этой физики-естествознания. В IV веке до н. э. Аристотель и Теофраст из общей науки о природе выделили науки о живом. Но занимались они исключительно описанием. Описательные разделы есть в любой науке, но настоящая, полноценная наука обязательно включает в себя фундаментальные составляющие, в которых путем теоретических размышлений и спланированных экспериментов добывают знания о причинах и механизмах наблюдаемых явлений. В XIX веке физика и биология окончательно разделились. Именно вторая половина XIX века – начало развития не просто описательной, а фундаментальной, направленной на установление общих закономерностей, биологической науки – генетики, эволюционного учения. Вторая половина ХХ века – новый толчок, беспрецедентно стремительное развитие молекулярной биологии, биофизики, информационной биологии.
Такое неравномерное развитие биологических наук объясняется тем, что биологические системы неизмеримо сложнее, чем системы, которые изучала классическая физика. Сами технические возможности изучать такие системы начали появляться только с XIX века.
Термин «биология» (греч. βιος – жизнь, λογος – наука, слово) был впервые предложен в 1802 году выдающимся французским естествоиспытателем и эволюционистом Жаном Батистом Ламарком для обозначения науки о жизни как особом явлении природы. Важнейшими вехами в истории новой, фундаментальной, биологии стали публикации в 1859 году книги Ч.Дарвина «Происхождение видов путем естественного отбора» и в 1865 году работы Г.Менделя «Опыты с растительными гибридами».
40-е годы ХХ века – время рождения молекулярной биологии. Важнейшей датой в ее развитии считается 1953 год – установление структуры ДНК, главной хранительницы наследственной информации. Молекулярная биология – это наука о механизмах хранения, воспроизведения, передачи и реализации генетической информации, о структуре и функциях основных биополимеров – нуклеиновых кислот и белков.
Успехи молекулярной биологии привели к возникновению генной инженерии – совокупности методов, позволяющих путем операций in vitro (в пробирке) переносить генетическую информацию из одного организма в другой. Перспективы применения генно-инженерных методов захватывающи – от обеспечения полноценным экологически чистым питанием всего населения Земли до лечения и предупреждения болезней, являющихся в настоящее время неизлечимыми.
Другим следствием развития молекулярной биологии и совершенствования методов исследования живых объектов стало возникновение новой отрасли биологии – геномики, комплексной науки, изучающей геномы разных организмов.
Развитие кибернетики и информатики способствовало возникновению и развитию информационной биологии – науки, использующей методы прикладной математики и статистики для анализа генетической информации, предсказания структуры макромолекул, моделирования эволюционных процессов. Живые системы настолько сложны, что рассчитывать все взаимодействия генов и их продуктов в клетке возможно только с применением мощной вычислительной техники.
Созданное В.И.Вернадским учение о биосфере вместе с возникшей в конце XIX века экологией к настоящему времени приобрело огромное значение не только как фундаментальная наука о свойствах такой сложнейшей системы, какой является Земля с населяющими ее живыми организмами, но и как прикладная наука, изучающая влияние человека на окружающую среду.
Разработанная австрийским биологом Людвигом фон Берталанфи общая теория систем помогает понять общие закономерности возникновения и свойств биологических систем, сущность самого явления жизни.
Конец ХХ и начало XXI века – время необычайно быстрого развития биологических наук. Усовершенствование технических средств молекулярно-биологических исследований позволило полностью прочитать геномы человека, мыши, собаки, других млекопитающих, сотен бактерий и вирусов. Более того, стали доступны для исследования ДНК вымерших животных – мамонта, некоторых насекомых. Частично прочитан геном неандертальца. Ученые научились синтезировать искусственные белки и нуклеиновые кислоты заданного состава и формы, создавать ферменты, «оперировать» гены. Идут работы по созданию искусственной клетки. На очереди задачи продления жизни человека, лечение тяжелых наследственных заболеваний, рака.
В числе важнейших этапов развития биологии в ХХ веке можно указать:
1901 год – вторичное открытие законов Менделя Г. де Фризом, К. Корренсом и Э. Чермаком.
1910 год – установление локализации генов в хромосомах Т.Морганом.
1926 год – публикация монографии В.И.Вернадского «Биосфера».
1926 год – открытие искусственного мутагенеза Г.Мёллером.
1944 год– д оказательство генетической роли нуклеиновых кислот О. Эйвери, К. Мак-Леодом и М. Маккарти
1953 год – установление структуры двойной спирали ДНК Дж. Уотсоном, Ф.Криком и М.Уилкинсом.
1961 год – открытие генетической регуляции синтеза ферментов А. Львовым, Ф. Жакобом и Ж. Моно.
1962 год – расшифровка генетического кода М. Нирнбергом, Г. Матеи и С. Очоа.
1968 год – публикация работы Л. фон Берталанфи «Общая теория систем. Основания, развитие, применение»
1970 год – открытие фермента обратной транскриптазы и явления обратной транскрипции Г. Темином, Д.Балтимором и Р.Дульбекко.
1974 год – открытиерестриктаз Г. Смитом, Д. Натансом и В. Арбером. Пересадка гена лягушки в бактериальную клетку С.Коэном и Г.Бойером. Начало генной инженерии.
1978 год – открытие сплайсинга Ф.Шарпом и Р.Робертсом.
1980 год – создание первого трансгенного млекопитающего (мыши) М.Кляйном.
1987 год – открытие полимеразной цепной реакции К. Маллисом.
1997 год – клонировано первое млекопитающее овца Долли.
1988-2003 годы – проект «Геном человека».
1998 год – открытие явления РНК-интерференции Э. Файром и К. Меллоу.
1999-настоящее время – полная расшифровка геномов многих бактерий и вирусов, некоторых растений и животных.
Этот список неполон – открытия, многие из которых по праву могут считаться выдающимися, следуют одно за другим.
Живая материя. Живой мир необычайно разнообразен. В настоящее время обнаружено и описано примерно 500 тыс. видов растений и более 1,5 млн. видов животных, более 3 тыс. видов бактерий и сотен тысяч грибов. Число еще не описанных видов оценивается, по меньшей мере, в 1-2 млн. Описанные к настоящему времени вирусы – только незначительная часть огромного мира неклеточных живых систем. Поэтому не теряют своей значимости описательные науки – ботаника, зоология, микробиология и присоединившаяся к ним в ХХ веке вирусология. Выявление и объяснение общих закономерностей явлений и процессов для всего многообразия организмов — задача общей биологии.
Живая материя – сложная система с особыми свойствами. Системой называют (от греч. s u t e m a – целое, составленное из частей; соединение) множество элементов, находящихся в отношениях и связях друг с другом, образующих определенную целостность, единство. Биологические системы любого уровня организации очень сложны, они состоят из множества разнородных элементов, связанных между собой прямыми и обратными связями. Существование прямых и обратных связей означает наличие информации, которой обмениваются элементы системы. Одним из основных свойств живой материи является возникновение, передача и реализация огромного количества информации. Вот это наличие прямых и обратных связей, то есть обмена информацией, делает системы принципиально отличными от простых элементов в первую очередь тем, что у систем возникают новые свойства, отсутствующие у любого из ее элементов. В природе большинство объектов – системы, начиная с атома и кончая всей Вселенной.
Важным свойством живых систем является единство химического состав а. Несмотря на то, что живые организмы построены из тех же химических элементов, что и объекты неживой природы, молекулярный состав их очень различен. В живых организмах 98% всех атомов приходится на четыре элемента: углерод, кислород, азот и водород, находящихся в составе органических соединений и воды. Такие органические молекулы как аминокислоты и моносахара, являющиеся составной частью биополимеров (белков, полисахаридов, нуклеиновых кислот) существуют в виде двух форм, являющихся зеркальным отражением друг друга («правые» и «левые» стереоизомеры). Важнейшей особенностью живой материи является хиральная (греч.χειρου – руки) чистота – то, что в состав всех живых организмов входят биополимеры, построенные только из «левых» аминокислот и только «правых» сахаров.
Обмен веществ и энергии. Одно из важнейших свойств живых систем – то, что они являются открытыми. Такие сложные системы термодинамически неравновесны, их существование невозможно без внешнего источника энергии и веществ, за счет которых и поддерживается это неравновесие. Прекращение поступления энергии и вещества приводит к гибели биологической системы.
Изменчивость – приобретение новых признаков и свойств. Она дает возможность гибкого приспособления к меняющимся условиям среды. В основе наследственной изменчивости лежат изменения генетической информации.
Способность к развитию. Это свойство, в теории систем называемое эмерджентность (англ. emergence – всплытие, появление), является одним из универсальных свойств сложных систем. Оно известно с древнейших времен в формулировке «целое больше, чем сумма частей». Это означает, что сложность отношений и связей в системе приводит к возникновению новых свойств, которые нельзя предсказать, исходя только из свойств составляющих систему частей. Благодаря этому сложные системы способны к самоорганизации – развитию с усложнением строения. Развитие – это изменение строения и функционирования живой системы, приводящее к качественно новому состоянию. Различают индивидуальное и историческое развитие. В ходе индивидуального развития биологическая система возникает, постепенно и последовательно проявляет свои свойства. Индивидуальное развитие обычно ограничено временем жизни организма. Историческое развитие – эволюция, происходит постоянно, начиная с момента возникновения жизни около 4 млрд. лет назад. Результатом эволюции является все многообразие живого на Земле.
Одним из свойств систем является иерархичность их устройства. Вся природа представляет собой такую иерархичную систему: элементарные частицы – атомы – молекулы – макромолекулы – клетки – организмы – популяции – экосистемы – Земля – Солнечная система – Галактика – Вселенная. Живая природа органично включается в эту иерархию.
Уровни организации жизни. Для живой природы характерны разные уровни организации ее структур, между которыми существует сложное соподчинение. Жизнь на каждом уровне изучают соответствующие разделы биологии: молекулярная биология, цитология, генетика, анатомия, физиология, эволюционное учение, экология.
Самый нижний, наиболее древний уровень жизни — это уровень молекулярных структур. На субмолекулярном уровне проходит граница между живым и неживым. Выше находится клеточный уровень жизни. И клетка, и заключенные в ней макромолекулярные структуры в главных чертах строения у всех организмов сходны.
Органно-тканевый уровень характерен только для многоклеточных организмов, у которых клетки и образованные из них части организма достигли высокой степени структурной и функциональной специализации.
Следующий уровень — это уровень целостного организма. Организмы могут быть как многоклеточными, так и одноклеточными, но в любом случае они взаимодействуют с внешней средой как целостная структура. Это возможно потому, что функционирование отдельных клеток, органов и тканей, составляющих организм, осуществляется согласованно и направлено на поддержание правильной работы целого организма. У одноклеточных организмов клеточный и организменный уровни совпадают, а отдельные функции выполняются особыми «агрегатами» - органоидами.
Вид, объединяющий сходные в основных чертах организмы, составляет более сложный уровень организации жизни. Здесь действуют свои законы — законы внутривидовых отношений организмов.
Наконец, еще более высоким уровнем является уровень биоценозов, т. е. сообществ всех видов, населяющих ту или иную территорию или акваторию. На этом уровне действуют законы межвидовых отношений.
Совокупность всего живого, населяющего Землю, составляет биосферный уровень организации жизни.
Глава I. Молекулярная биология.
§ 1. Структура белков
 В состав живого входят самые различные органические соединения, но то, без чего жизнь на Земле не существует – это главные биополимеры– белки и нуклеиновые кислоты. Основным «строительным материалом» и «инструментами», осуществляющими процессы жизнедеятельности, являются белки. Огромное, практически бесконечное разнообразие белков позволяет им справляться почти со всеми функциями живого. Пожалуй, только к хранению и передаче наследственной информации они не способны.
В состав живого входят самые различные органические соединения, но то, без чего жизнь на Земле не существует – это главные биополимеры– белки и нуклеиновые кислоты. Основным «строительным материалом» и «инструментами», осуществляющими процессы жизнедеятельности, являются белки. Огромное, практически бесконечное разнообразие белков позволяет им справляться почти со всеми функциями живого. Пожалуй, только к хранению и передаче наследственной информации они не способны.
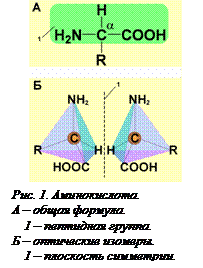
Белки – это полимеры, мономерами которых являются аминокислоты. Аминокислотами называются органические соединения, в состав которых входят две функциональные группы – карбоксильная группа и аминогруппа. Группировка, в которой к одному атому углерода присоединены и карбоксильная и аминогруппа (α-положение), называется пептидной группой (рис. 1, [O1] А). В природе обнаружено около 200 аминокислот, из них в большинстве организмов встречается около 60, но в состав белков входит только 22 аминокислоты (одна из них, пролин, по химической структуре является не амино-, а иминокислотой).
Все аминокислоты, за исключением глицина, существуют в виде двух оптических изомеров. Эти изомеры идентичны по своим химическим свойствам, их различие состоит в том, что они отклоняют плоскость поляризованного света в противоположные стороны. Таким свойством обладают все молекулы, у которых все четыре валентности одного атома углерода заняты разными заместителями (рис. 1, Б). Все аминокислоты, которые включаются в белки, являются левовращающими стереоизомерами, у которых аминогруппа находится в α-положении (в пролине в α-положении находится иминогруппа). Помимо L - аминокислот в организме есть не 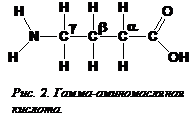 включающиеся в белки D-аминокислоты и аминокислоты с другим (не a-) положением аминогруппы. В некоторых белках, например, в светящемся белке светлячка, есть D-аминокислоты, но они не включаются в молекулу во время синтеза, а образуются из L-аминокислот в результате химической модификации в готовой молекуле белка под действием ферментов. Важную роль в организме человека играет не входящая в состав белков γ-аминомасляная кислота, являющаяся нейромедиатором (рис. 2[O2]).
включающиеся в белки D-аминокислоты и аминокислоты с другим (не a-) положением аминогруппы. В некоторых белках, например, в светящемся белке светлячка, есть D-аминокислоты, но они не включаются в молекулу во время синтеза, а образуются из L-аминокислот в результате химической модификации в готовой молекуле белка под действием ферментов. Важную роль в организме человека играет не входящая в состав белков γ-аминомасляная кислота, являющаяся нейромедиатором (рис. 2[O2]).
Первичная структура белка. Белки представляют собой цепочку соединенных друг с другом аминокислот. Такое соединение возможно потому, что аминокислоты обладают двумя функциональными группами – кислотной и оснóвной. Эти группы в одной молекуле не могут взаимодействовать между собой из-за жесткости структуры, а будучи в разных молекулах могут реагировать друг с другом. Аминокислоты соединяются в полипептид с помощью ковалентных пептидных (амидных) связей. Последовательность расположения аминокислотных остатков в полипептидной цепи представляет собой первичную структуру белка (рис 3, А[O3]). Подавляющее большинство природных белков представляют собой нерегулярные полимеры. Регулярные, с закономерным чередованием аминокислот, белки встречаются крайне редко. Это всегда структурные белки, представляющие собой очень длинные прочные нити. Примером является белок шелка фиброин. Это полимер, в котором регулярно повторяется шестерка аминокислот Гли-Ала-Гли-Ала-Гли-Сер. Почти регулярную первичную структуру имеет коллаген – структурный белок соединительной ткани кожи.
Благодаря нерегулярности разнообразие возможных белков практически бесконечно. Например, у трипептида, состоящего из трех разных аминокислот, возможно 3! = 6 различных первичных структур. У олигопептида, состоящего из двадцати разных аминокислот, разнообразие первичных структур 20!, это ≈ 2×1018. Разнообразие первичных структур среднего по размеру белка (примерно 500 аминокислот) составляет уже ≈ 20500 вариантов (если все аминокислоты представлены в эквимолярных соотношениях).
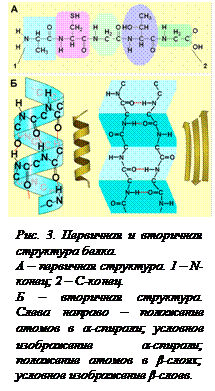 Вторичная структура белка может быть регулярной α -спиралью и нерегулярной β -складчатой структурой. В α -спирали карбонильная группа С=О аминокислотного остатка образует водородную связь с группой NHаминокислотного остатка, находящегося через четыре мономера от него. На один виток α -спирали приходится 3,6 аминокислотных остатков. В определенных случаях регулярность спирали нарушается. Как правило, это происходит в местах расположения пролина либо находящихся рядом друг с другом одинаково заряженных радикалов. β -складки также образуются с помощью водородных связей. При этом молекула не закручивается в спираль, а складывается «гармошкой» (рис. 3, Б). Водородные связи могут образовывать не только одиночные, но и рядом расположенные полипептиды, входящие в один белок. Как правило, в одной молекуле полипептида чередуются участки α и β- структур. Эти участки отличаются по своим физическим свойствам – β- слои более жесткие. В некоторых белках есть участки, не обладающие вторичной структурой. На их долю может приходиться до 40% длины полипептида.
Вторичная структура белка может быть регулярной α -спиралью и нерегулярной β -складчатой структурой. В α -спирали карбонильная группа С=О аминокислотного остатка образует водородную связь с группой NHаминокислотного остатка, находящегося через четыре мономера от него. На один виток α -спирали приходится 3,6 аминокислотных остатков. В определенных случаях регулярность спирали нарушается. Как правило, это происходит в местах расположения пролина либо находящихся рядом друг с другом одинаково заряженных радикалов. β -складки также образуются с помощью водородных связей. При этом молекула не закручивается в спираль, а складывается «гармошкой» (рис. 3, Б). Водородные связи могут образовывать не только одиночные, но и рядом расположенные полипептиды, входящие в один белок. Как правило, в одной молекуле полипептида чередуются участки α и β- структур. Эти участки отличаются по своим физическим свойствам – β- слои более жесткие. В некоторых белках есть участки, не обладающие вторичной структурой. На их долю может приходиться до 40% длины полипептида.
Третичная структура белка – этопространственная конформация полипептида, имеющего вторичную структуру, и обусловленная взаимодействиями между радикалами аминокислот (рис. 4, [O4] А).
Существует четыре типа взаимодействий между радикалами.
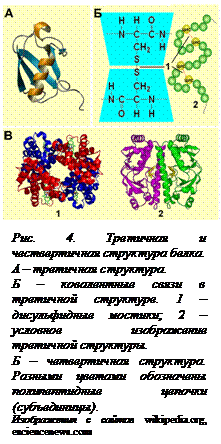 1.Ковалентные связи между остатками двух цистеинов – так называемые дисульфидные мостики (Рис 4, Б).
1.Ковалентные связи между остатками двух цистеинов – так называемые дисульфидные мостики (Рис 4, Б).
2.Ионные (электростатические) взаимодействия между противоположно заряженными радикалами аминокислотных остатков. Например, положительно заряженная ε-аминогруппа лизина (– NH 3 +) притягивается отрицательно заряженной карбоксильной группой (СОО-) глутаминовой или аспарагиновой кислоты.
3. Водородные связи образуют все аминокислотные радикалы, имеющие гидроксильные, амидные или карбоксильные группы.
4. Гидрофобные взаимодействия возникают между неполярными радикалами в водной среде. Выталкиваемые из воды гидрофобные радикалы аминокислот, стремясь занять наименьший объем, формируют гидрофобное ядро, внутри которого вода отсутствует. В результате молекула приобретает сложную пространственную конформацию, только сохраняя которую белок может выполнять свою биологическую функцию.
В образовании третичной структуры гидрофобные взаимодействия являются определяющими в силу своей неизбирательности и многочисленности. Из 22 аминокислот 9 содержат гидрофобные радикалы, каждый из которых может взаимодействовать с любым из них. Гидрофобное ядро существует у большинствабелков.
Четвертичная структура белка – это объединение двух или большего числа полипептидных цепей, имеющих третичную структуру, для выполнения общей функции (рис. 4, В). Четвертичную структуру образуют и поддерживают водородные, электростатические и дисульфидные связи.Четвертичной структурой обладает около 5% белков, в том числе гемоглобин, иммуноглобулины, инсулин. Почти все матричные ферменты (ДНК- и РНК- полимеразы) имеют четвертичную структуру.
 Правильные вторичная, третичная и четвертичная структуры белков – необходимое условие их функционирования. Например, некоторые белки могут устойчиво существовать и в форме α- спирали и в форме β- слоев. Эти изменения существенно меняют свойства белков, что может привести к заболеванию. Такие заболевания известны – скрепи овец, «коровье бешенство», болезнь Крейцфельда-Якоба, болезнь куру, фатальная семейная бессонница людей. Причиной этих болезней являются так называемые прионные белки (рис. 5[O5], А). Эти белки присутствуют в норме в клетках центральной нервной системы. Заболевание возникает, когда молекулы приобретают неправильную вторичную структуру – в них уменьшается количество α- спиральных участков и увеличивается число β- слоев. Такие молекулы не выполняют своих функций и не уничтожаются ферментами. Они накапливаются в клетках мозга и вызывают их гибель. У больных животных и человека мозг становится похожим на губку из-за многочисленных пустот на месте погибших клеток (рис. 5, Б).
Правильные вторичная, третичная и четвертичная структуры белков – необходимое условие их функционирования. Например, некоторые белки могут устойчиво существовать и в форме α- спирали и в форме β- слоев. Эти изменения существенно меняют свойства белков, что может привести к заболеванию. Такие заболевания известны – скрепи овец, «коровье бешенство», болезнь Крейцфельда-Якоба, болезнь куру, фатальная семейная бессонница людей. Причиной этих болезней являются так называемые прионные белки (рис. 5[O5], А). Эти белки присутствуют в норме в клетках центральной нервной системы. Заболевание возникает, когда молекулы приобретают неправильную вторичную структуру – в них уменьшается количество α- спиральных участков и увеличивается число β- слоев. Такие молекулы не выполняют своих функций и не уничтожаются ферментами. Они накапливаются в клетках мозга и вызывают их гибель. У больных животных и человека мозг становится похожим на губку из-за многочисленных пустот на месте погибших клеток (рис. 5, Б).
Примером важности правильной третичной и четвертичной структуры является наследственное заболевание серповидно-клеточная анемия, возникающее из-за нарушения третичной и четвертичной структур белка глобина. Гемоглобин – комплекс белка глобина с небелковой железосодержащей частью - гемом. Глобин имеет четвертичную структуру. Он состоит из двух альфа- и двух бета- полипептидных цепей (это общепринятые названия цепей, не имеющие отношения к их вторичной структуре), обладающих третичной структурой. В сумме это 574 аминокислоты. У всех здоровых людей на 6-ом месте от N-конца в бета-цепи находится отрицательно заряженная глутаминовая кислота. У больных серповидно-клеточной анемией вместо нее стоит неполярный валин. Такой гемоглобин теряет растворимость, образуется волокнистый осадок, деформирующий клетку. Эритроцит принимает форму серпа (рис. 5, В, Г). Такие эритроциты плохо переносят кислород.
Глобулярные и фибриллярные белки. 95% белков имеют гидрофобное ядро. Молекулы таких белков формируют округлые частицы – глобулы. Остальные 5% белков имеют нитевидную форму. Это фибриллярные белки. Подавляющее число глобулярных белков растворимо. Это связано с тем, что нерастворимые гидрофобные радикалы составляющих их аминокислот «спрятаны» внутри глобулы. Фибриллярные белки содержат больше заряженных аминокислот, чем глобулярные. Отдельные цепи этих белков растворимы, а их комплексы неполярны и нерастворимы. Примерами таких белков могут служить α-кератины (на их долю приходится почти весь сухой вес волос, шерсти, рогов, копыт, ногтей, чешуи, перьев), коллаген (белок кожи, сухожилий, хрящей), фиброин (белок шелка).
Денатурация и ренатурация. Большинство взаимодействий, поддерживающих пространственную конформацию белковых молекул, легко нарушаются при изменении внешних условий. При повышении температуры, например, разрываются водородные связи, усиливающееся броуновское движение нарушает компактность гидрофобных ядер. Изменение ионной силы раствора может нарушить электростатические взаимодействия. Такие воздействия приводят к денатурации – нарушению нативной (природной, «правильной») третичной и четвертичной структуры белковых молекул, что обычно сопровождается потерей функциональной активности. Денатурация может быть обратимой, когда при нормализации условий происходит восстановление нативной структуры, и необратимой. Необратимость денатурации часто связана с образованием «незаконных» межмолекулярных связей. Примером необратимо денатурированного белка является белок сваренного куриного яйца, он теряет прозрачность и растворимость.
§ 2. Функции белков
Белком называют отдельный полипептид или агрегат нескольких полипептидов, выполняющий биологическую функцию. Полипетид – этопонятие химическое, он представляет собой одну полимерную цепочку, состоящую из аминокислот. Белок – понятие биологическое, он может представлять собой как отдельную молекулу полипептида, так и объединение нескольких полипептидов. Например, антитело – молекула, состоящая из четырех полипептидных цепей, которые по отдельности не являются белками, белок – только их функциональный агрегат. Многие ферменты состоят из нескольких субъединиц – отдельных полипептидов. Белки, в силу своего огромного разнообразия, способны выполнять самые различные функции в клетке и в организме. Эти функции можно разделить на следующие группы: 1) каталитическая, 2) защитная, 3) регуляторная, 4) рецепторная, 5) структурная, 6) функция трансформации энергии, 7) транспортная, 8) питательная, 9) буферная, 10) энергетическая, 11) другие.
Каталитическая функция белков. В клетках и организмах протекает огромное количество химических реакций, очень многие из которых в физиологических условиях могут идти только в присутствии катализаторов. Но даже и те реакции, которые в принципе могут протекать самопроизвольно, в клетке также идут с помощью катализаторов – ферментов. Практически все ферменты являются белками. Лишь некоторые ферменты, рибозимы, представляют собой молекулы РНК. Ферменты отличаются от неорганических катализаторов, используемых в химии, некоторыми важными свойствами. Это: 1) очень высокая эффективность, 2) строгая специфичность, 3) узкий оптимум условий среды и 4) способность к регуляции. Как и неорганические катализаторы, ферменты понижают энергию активации, только, как правило, гораздо сильнее. Например, реакцию разложения пероксида водорода до кислорода и воды платина ускоряет в 220000 раз, а фермент каталаза – в 93000000000 раз! Но те реакции, которые невозможны термодинамически, ферменты катализировать не могут. Неорганические катализаторы могут ускорять самые разные реакции, тогда как в клетке для каждой реакции существует свой фермент. Это делает возможным одновременное протекание множества разных реакций внутри одной клетки. Как правило, фермент «узнает» свои субстраты (вещества, участвующие в данной реакции) по пространственной конфигурации. С этим связано такое качество большинства ферментов как узкие пределы условий среды (температура, ионная сила раствора, рН), в которых ферменты могут работать – ведь изменение именно этих параметров вызывает денатурацию белков. Денатурация, представляющая собой изменение пространственной структуры молекулы, лишает ее функциональной активности.
Как работают ферменты? Молекула фермента обязательно имеет один или несколько активных центров, с которыми связываются молекулы субстратов. Некоторые ферменты, катализирующие реакции, для которых нужна энергия, имеют и центры связывания АТФ. Как правило, ферменты осуществляют акт катализа за счет изменения своей конформации. Например, если фермент должен осуществить соединение двух субстратов в один продукт, он должен связать эти субстраты с образованием фермент-субстратного комплекса (рис. 6, [O6] А). Сам акт связывания меняет конфигурацию фермента и его активных центров за счет взаимодействий с субстратами (электростатических, гидрофобных – в зависимости от конкретной реакции). В результате этого молекулы субстратов оказываются, во-первых, повернутыми друг к другу так, как они должны быть расположены в продукте, а во-вторых, несколько деформированными, причем именно таким образом, чтобы усилить реакционную способность реагирующих групп. Это может быть, например, оттягивание на себя отрицательно заряженными аминокислотами активного центра протона гидроксильной группы субстрата, что облегчает его перенос на другую молекулу. Такая «целенаправленная деятельность» ферментов обеспечивает их очень высокую эффективность. Некоторые ферменты для своей работы нуждаются в небольших молекулах-помощниках, называемых коферментами.






