| Металл | Температура плавления, ºC | Микротвердость, МПа | |||||
| металла | борида | карбида | нитрида | борида | карбида | нитрида | |
| Ti | |||||||
| V | |||||||
| Zr | |||||||
| Nb | |||||||
| Mo | – | – | |||||
| W | – | – |
1.10.2. Самораспространяющийся высокотемпературный
синтез
Самораспространяющийся высокотемпературный синтез (СВС) основан на явлении распространения фронта горения в порошках некоторых химических элементов, в результате сильной экзотермичности при взаимодействии этих элементов с бором, углеродом, азотом, кремнием и другими металлоидами. Обобщенная химическая схема процесса может быть представлена следующим образом:
Σai Xi + ΣbiYi = Z + Q, (1.27)
где Х – Ti, Zr, Hf, V, Nb, Ta, Mo, W и другие металлы; Y – B, C, N, Si, и другие элементы; Z – бориды, карбиды, нитриды, силициды и другие соединения металлов, а также твердые растворы или интерметаллиды; Q – тепловой эффект. Элементы «Х» обычно применяют в виде порошков, «Y» ‑ в порошкообразном, газообразном или жидком состояниях. Получаемый продукт «Z» является тугоплавким соединением и обычно находится в твердом состоянии. В зависимости от ведущей реакции горения и агрегатного состояния реагентов все СВС ‑ системы делят на четыре класса: безгазовые, фильтрационные, газовыделяющие и металлотермические.
В безгазовыхсистемах исходные компоненты, промежуточные и конечные продукты находятся в твердом или жидком состояниях. Возможно незначительное газовыделение, вызванное очисткой от примесей. Синтез проводят в вакууме или в инертном газе. Состав продуктов горения практически не зависит от атмосферы процесса.
Фильтрационный синтез протекает в гибридной системе металл-газ, при этом состав продуктов горения, а также параметры процесса сильно зависят от давления и состава газовой фазы. На доставку (фильтрацию) газа в зону горения существенно влияют габариты и пористость сбрикетированного металлического порошка.
Газовыделяющими являются системы с легколетучими компонентами – серой, селеном, фосфором и сжиженным газом (жидким азотом). В этом случае синтез проводят в герметичных емкостях, полностью заполненных исходными твердыми компонентами для того, чтобы при испарении образующийся газ не покидал реакционный объем, а оставался в порах.
Металлотермические системы характерны тем, что горение имеет две принципиально различные химические стадии: восстановление оксидов и последующее взаимодействие продуктов восстановления между собой и со специальными добавками, вводимыми в шихту. Восстановителями в этих системах могут быть магний или алюминий.
Схема СВС процесса показана на рис. 1.16.
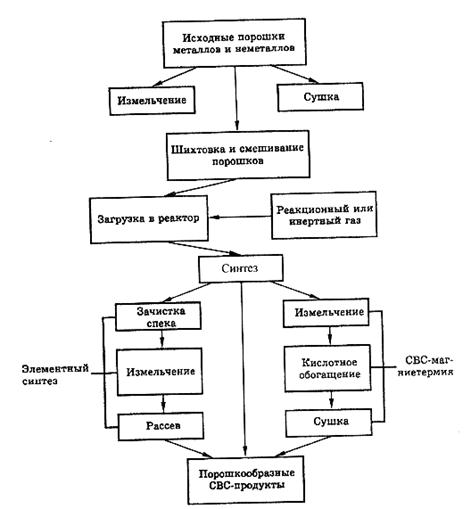
Рис. 1.16. Схема СВС – технологии получения порошка
Синтез проводится в реакторе (рис. 1.17). Реакционная зона реактора имеет обычно объем от 1 до 30 л. Внутреннее устройство реактора зависит от типа синтезируемого продукта. При синтезе карбидов, боридов или силицидов внутреннюю поверхность реактора футеруют графитом. При синтезе нитридов и гидридов реактор оснащают специальным устройством для подачи реагирующего газа в зону реакции. После загрузки шихты реактор закрывают и, в зависимости от специфики процесса, вакуумируют, или заполняют инертным газом. Инициирование начала процесса осуществляют с пульта управления подачей кратковременного электрического импульса на вольфрамовую спираль, касающуюся исходной шихты. В начале синтеза возникает яркое свечение фронта горения, поскольку температура процесса составляет, в зависимости от системы, 1500-4000 ºC. Светящаяся зона распространяется вглубь шихты со скоростью 0,005 – 0,15 м/c.
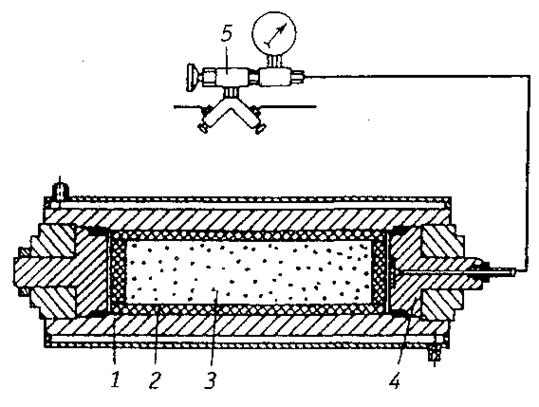
Рис. 1.17. Схема СВС - реактора: 1 – корпус; 2 – графитовая
футеровка; 3 – реакционная шихта; 4 – грибковый затвор;
5 – газораспределительный узел
Степень превращения исходных продуктов при СВС зависит от термодинамических и кинетических ограничений. Изменяя дисперсность реагентов, размер и плотность порошкового тела, теплоотдачу с поверхности и температуру горения, можно в широких пределах регулировать процесс СВС. В результате получают однофазные соединения с уровнем чистоты не ниже чистоты исходных реагентов. Высокое качество получаемых продуктов, простота аппаратурного оформления, высокие скорости синтеза, минимальные энергозатраты обеспечивают расширение промышленного применения СВС.
1.10.3. Золь-гель процесс
В основе этого процесса лежит образование гидрооксидов металлов при химическом превращении высокодисперсных систем – золей в рыхлые аморфные структуры – гели. Золи представляют собой системы, в которых частицы высокодисперсной твердой фазы участвуют в броуновском движении и, благодаря этому, находятся во взвешенном состоянии. Различают гидрозоли, органозоли и аэрозоли, у которых дисперсионная среда соответственно вода, органическая жидкость или газ. Золи способны коагулировать, т. е. образовывать крупные агрегаты частиц в виде структурированных систем, например гелей. Коагуляция происходит при удалении лишней воды из системы, что достигается повышением температуры, воздействием электромагнитных полей, жестких излучений, механическими или химическими воздействиями.
Процессы в водных средах происходят в такой последовательности: гидролиз → полимеризация → нуклеация → рост. Процесс нуклеации представляет собой образование статистических зародышей критического размера.
Золь-гель процессы разделяют на коллоидные и полимеризационные. В коллоидных системах образование гелей происходит в растворах, содержащих золь одного или более компонентов. Полимеризационный процесс формирует непрерывную полимерную структуру геля, который может содержать катионы различной природы. Размер и распределение частиц порошка зависят от процессов нуклеации и последующего их роста. Для достижения монодисперсности порошков необходимо регулировать концентрации исходных компонентов и растворителя на стадии нуклеации. Изменением концентрации раствора, можно регулировать форму частиц синтезируемого порошка.
Золь-гель процессом изготавливают порошки оксидов титана, циркония, гафния, вольфрама, алюминия и других металлов. Эти порошки обладают высокой степенью дисперсности, соответственно большой удельной поверхностью и активны при спекании. Золь-гель процесс позволяет получать и нанопорошки.
1.11. Распыление металлических расплавов
Промышленное производство распыленных порошков началось в середине прошлого века. Уже в 1959 г. в США и Канаде объем производства железных порошков составил 6 тыс.т., в ФРГ 2,2 тыс.т. и в Англии 0,5 тыс.т. В настоящее время в мире производится около 500 тыс.т. распыленных металлических порошков. Кроме порошков железа, различными способами распыления производят порошки алюминия, меди, свинца, цинка, титана, циркония, молибдена, вольфрама, а также сплавов на основе перечисленных и других металлов. Важно подчеркнуть, что технологии распыления особенно эффективны при получении порошков высоколегированных и многокомпонентных сплавов, поскольку обеспечивают высокую степень однородности химического состава и дисперсное строение литого металла. Методы распыления различаются по виду источников нагрева металла (индукционный, электродуговой, электронный, лазерный, плазменный и др.), по типу силового воздействия на распыляемый расплав (энергия потоков газа, жидкости, механическое воздействие центробежных сил и др.), а также по типу среды, в которой протекает процесс распыления (восстановительная, окислительная, инертная, вакуум).
1.11.1. Разрушение струи жидкости
Жидкое состояние, являясь промежуточным между твердым и газообразным состояниями, обладает отдельными свойствами, как твердых тел, так и газов. Жидкости изотропны и текучи как газы, но их плотность, сжимаемость и теплоемкость близки к аналогичным свойствам твердых тел. Как и твердые тела, жидкости занимают в пространстве определенный объем. Детальное обоснование близости жидкостей и твердых тел вблизи температуры затвердевания было впервые проведено Я.И. Френкелем. Опираясь на представление о квазикристаллическом строении жидкостей, он получил качественное описание теплового движения атомов и молекул в жидкостях и на основе решеточной модели объяснил диффузию и вязкость жидкостей, процессы плавления и кристаллизации. Структура жидкости в решеточной модели рассматривается как сильно искаженная, расшатанная и неупорядоченная структура твердого тела с разрывами (дырками) между атомами. Такие разрывы мгновенно возникают и мгновенно залечиваются, но они всегда, в любой момент времени, существуют в объеме жидкости. Сумма всех разрывов создает дополнительный объем жидкости по отношению к объему твердого тела.
Наиболее важными свойствами металлических расплавов, во многом определяющими процесс их распыления, являются вязкость и поверхностное натяжение. Вязкостью называют свойство жидкости, характеризующее сопротивление сдвигу. Вязкость жидкости или обратное ей свойство текучести обусловлена наличием дополнительного объема у жидкости по отношению к объему твердого тела. Зависимость вязкости жидкости от ее свободного объема описывается простой эмпирической формулой
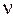 = В/V-Vо, (1.28)
= В/V-Vо, (1.28)
где 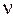 ‑ коэффициент кинематической вязкости; В – константа, Vо – минимальный удельный объем жидкости, близкий к объему твердого тела; V – удельный объем реальной жидкости.
‑ коэффициент кинематической вязкости; В – константа, Vо – минимальный удельный объем жидкости, близкий к объему твердого тела; V – удельный объем реальной жидкости.
Иногда вязкость жидкости характеризуют коэффициентом динамической вязкости. Между коэффициентами кинематической и динамической вязкости существует зависимость
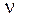 =
=  /
/ 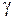 ж, (1.29)
ж, (1.29)
где  – коэффициент динамической вязкости;
– коэффициент динамической вязкости; 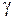 ж – плотность жидкости.
ж – плотность жидкости.
Вязкость жидких металлов существенно зависит от температуры, с ростом температуры вязкость уменьшается.
Поверхностное натяжение жидкости ‑ это работа образования физической поверхности раздела фаз, отнесенная к единице поверхности. Для дисперсных систем, образующихся при распылении, поверхностная энергия может составить значительную часть молекулярно-кинетической энергии вещества.
Процесс диспергирования жидкости приводит к образованию множества новых поверхностей раздела, причем часть молекул из объема жидкости переходит в ее поверхностные слои с более высокой энергией. При этом затрачивается работа на преодоление межмолекулярных сил
ΔА = σ ΔS, (1.30)
где σ ‑ свободная энергия единицы поверхности раздела или поверхностное натяжение;  S- вновь образовавшаяся поверхность.
S- вновь образовавшаяся поверхность.
При плавлении, распылении и охлаждении расплав взаимодействует с газами и жидкостями. Схема взаимодействия с газами включает в себя физическую адсорбцию газа на поверхность расплава, хемосорбцию газа в расплаве с образованием на поверхности расплава тонких пленок оксидов, нитридов и др. и диффузию атомов газа в глубь расплава с образованием химических соединений. Наиболее важными являются процессы взаимодействия расплава с кислородом азотом и водородом. При взаимодействии с кислородом на поверхности расплава мгновенно образуются оксидные пленки с кристаллической или аморфной структурой. Интенсивность взаимодействия зависит от химического состава расплава и газовой среды, а также от размера жидких капель, их реакционной поверхности. При распылении расплавов, легированных титаном, алюминием, хромом, ванадием и другими химически активными элементами, которые создают трудно восстановимые оксиды, целесообразно применять в качестве энергоносителей инертные газы, не содержащие кислорода.
Азот образует в расплавах нитриды, поэтому порошки металлов, в которых азот хорошо растворяется (железо, хром, ванадий, молибден, титан и др.) отличаются повышенной твердостью и более низкой пластичностью.
Водород образует гидриды с молибденом, титаном, цирконием, танталом, рением и некоторыми другими металлами. При снижении температуры растворенный водород обычно выделяется из металла, что может приводить к образованию пористости распыленных порошков и изделий.
Любая струя жидкости, самопроизвольно вытекающая из сосуда, даже без видимого воздействия на нее внешней среды, испытывает действие малых возмущений, которые порождают пульсацию жидкости в струе. Причинами таких возмущений могут быть шероховатость стенок канала, через который течет струя, искажение формы выходного отверстия и др. Множество малых возмущений порождают в струе волновой характер перемещения жидкости с растущей амплитудой колебания волны, скорость роста которой имеет максимум. Эта волна и образует будущую каплю, размер которой определится длиной волны. Оптимальная длина волны (λопт) определяется радиусом сопла истечения жидкости (Rо)
λопт = 4,5 Rо. (1.31)
Схема распада струй, в зависимости от скорости их истечения, показана на рис. 1.18. При относительно малой скорости истечения струи (< 25 м/с), характер и степень деформации струи определяются только осесимметричными колебаниями, амплитуда которых возрастает по мере удаления от выходного отверстия. Распад струи сопровождается образованием однородных по размеру крупных капель. При увеличении скорости истечения до 25 - 100 м/с возникают осенесимметричные колебания, искривляющие струю, из-за повышенного влияния воздушной атмосферы. Зона начала разрушения струи смещается ближе к выходному отверстию. Дальнейшее повышение скорости истечения (> 100 м/с) приводит к возникновению режима объемного распыления, причем зона разрушения сдвигается непосредственно к срезу сопла, образуя факел из распыленных капель жидкости неоднородных по размеру.
Распад струи жидкости газовым потоком представляет собой сложный физический процесс, в котором определяющую роль играют аэродинамические силы, величина которых зависит не только от скорости движения распыляющего газа, но и от его плотности. Этим силам противостоят силы поверхностного натяжения и вязкость расплава. Распад струи расплава под воздействием газового потока описывают критериальным уравнением:
d/D = φ (WE, LP, M, N), (1.32)
где d – cредний диаметр капель расплава; D – диаметр струи расплава; WE – критерий Вебера, определяющий соотношение сил инерции и сил поверхностного натяжения; L – критерий Лапласа, характеризующий соотношение сил вязкости и поверхностного натяжения расплава; М и N – критерии, характеризующие соответственно соотношение плотности газа (энергоносителя) и расплава и вязкости газа и расплава. Указанные критерии представляют собой: WE = Vг2 γг Do / σ; LP = ηж2 / (σγж Do); М = Vг2 γг / Vж2 γж); N = ηг / ηж, где Vг и Vж – cоответственно скорости газа и расплава; γг, γж – плотности газа и расплава соответственно; ηг, ηж ‑ вязкости газа и расплава соответственно; σ – поверхностное натяжение расплава; Dо – диаметр первоначальной пряди (крупной капли).
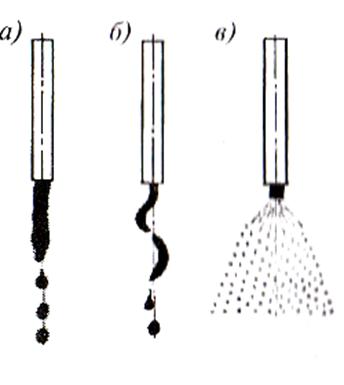
Рис. 1.18. Схема распада струй в зависимости от
скорости их истечения (W):
а ‑ W<25 м/c; б – W = 25-100 м/c; в ‑ W>100 м/c
Диспергирование струи начинается при некоторой критической (для данной струи) скорости газового потока. Исследование процесса распыления с помощью высокоскоростной киносъемки позволило выявить три структурные зоны в очаге распыления. Первая зона представляет собой сплошную, не распавшуюся часть струи после выхода ее из канала. Длина этой зоны колеблется от 1 до 10 мм и зависит от удаления фокуса распыления от выходного среза сопла газовой форсунки. Вторая зона соответствует началу разрушения струи, которая расслаивается в этой зоне на отдельные нити, пряди и крупные капли преимущественно цилиндрической формы. Протяженность второй зоны, которая по существу является первичной зоной дробления струи, составляет 10 - 20 мм. Вследствие большой разницы в относительных скоростях перемещения газа и металла струи, газ-энергоноситель начинает проникать в массу металла, создавая в ней объемы с высокими напряжениями сжатия. При выходе частично диспергированных объемов из зоны максимальных напряжений сжатия, они как бы взрываются, образуя поток дисперсных капель различного размера и формы. Процесс вторичного дробления прядей, нитей и крупных капель на частицы конечных размеров завершается в третьей зоне. Условием дробления является превышение скоростного напора потока газа над силами поверхностного натяжения в капле
γг Vг/2 > σ d. (1.33)
Средний размер частиц, образующихся в результате распыления струи расплава газовым потоком, оценивается эмпирической формулой:
dср = K(σ/γж)0,22(ηж/γж)0,57 / Vг, (1.34)
где К ‑ константа, определяемая геометрией сопла.
Очевидно, что основными факторами, определяющими дисперсность порошка при газовом распылении, являются энергия газового потока, вязкость и поверхностное натяжение расплава.
Расчеты, выполненные по формуле (1.34), показывают, что при распылении стали и значении исходных данных К = 600; σ = 1,83 Н/м; γж = 7000 кг/м3; η = 0,0054 Па·с; Vг = 100; 300; 400 м/c средний размер частиц составит d = 300; 100 и 70 мкм соответственно.
По структуре зона распыления, или как ее еще называют факел распыления, представляет собой трехфазную непрерывно пульсирующую смесь газа и металла, находящегося в жидком и затвердевшем состояниях. Скорость перемещения капель расплава сначала резко возрастает, а затем, по мере удаления от фокуса распыления, падает. Ускорение капель в газовом потоке зависит от их размера и уменьшается с увеличением размера. Скорость газового потока по направлению от среза сопла непрерывно снижается.
Процесс распыления расплава водой отличается от газового распыления, прежде всего, более высокой плотностью энергоносителя, (вода примерно в 1000 раз плотнее газа) и наличием большого количества паров воды в зоне распыления. Высокая плотность воды позволяет обеспечить увеличение импульса движения и кинетической энергии, упрощает проблему диспергирования и создает возможность получения более мелких фракций порошка. При контакте высокотемпературного расплава с водой происходит интенсивное парообразование как вокруг струи металла, так и вокруг каждой капли. Уже при температуре расплава 560 - 600°С в зоне контакта воды с расплавом возникает режим пленочного кипения, при котором происходит кипение локальных объемов воды на поверхности контакта при сохранении в основной массе воды исходного агрегатного состояния. Образующийся перегретый и сжатый пар активно включается в процесс диспергирования. Таким образом, процесс разрушения струи и диспергирования капель расплава происходит при комбинированном воздействии на расплав высокоэнергетических потоков воды и пара.
При взаимодействии капель воды с расплавом, капли мгновенно превращаются в пар и в зависимости от угла встречи с расплавом “выбивают” из него капли жидкого металла различной формы. Наиболее эффективное диспергирование расплава реализуется по механизму взрыва при соударении капель воды с каплями расплава.
Размер образующихся частиц, при распылении расплава водой, определяется по зависимости
d = K1 lnP/VВ sinα, (1.35)
где К1 ‑ константа, определяемая свойствами расплава и конструкцией распылительных форсунок; Р ‑ давление воды; Vв ‑ скорость потока воды; a ‑ угол атаки водяной струи.
1.11.2. Скорость охлаждения расплава при распылении
В общем случае теплообмен расплава с окружающей средой осуществляется теплопроводностью, конвекцией и излучением. Теплопроводность и конвекция обычно объединяются в понятие теплообмена соприкосновением. Такой вид теплообмена описывается уравнением Ньютона:
q = a(Тп - Тс), (1.36)
где q – удельный тепловой поток с поверхности расплава; a - коэффициент теплоотдачи; Тп и Тс – абсолютные температуры поверхности расплава и окружающей среды соответственно.
Теплообмен излучением описывается уравнением Стефана-Больцмана:
q = C0(Тп/100)4, (1.37)
где С0 – коэффициент лучеиспускания абсолютно черного тела (С0=5,7 Вт/м2К4).
Для реального серого тела, например, капли расплава, движущейся в вакуумной камере, уравнение для удельного потока принимает вид:
q = eС0[(Тп/100)4-(Тс/100)4], (1.38)
где e - степень черноты реального тела; Тс – абсолютная температура стенки вакуумной камеры.
В общем виде уравнение теплового баланса для охлаждающейся капли расплава можно представить следующим образом:
dq=F{a(Tп-Тс)+eС0[(Тп/100)4-(Тс/100)4]}dt=mcpdT, (1.39)
где F–поверхность капли; m – масса капли, ср – удельная теплоемкость расплава; dt - время охлаждения капли на величину dT.
Для сферической капли диаметром d скорость охлаждения составит:
dT/dt=  {a(Тп-Тс)+eС0[(Тп/100)4-(Тс/100)4]}. (1.40)
{a(Тп-Тс)+eС0[(Тп/100)4-(Тс/100)4]}. (1.40)
В фигурных скобках формул (1.39) и (1.40) первое слагаемое характеризует долю теплового потока, отводимого от расплава теплопроводностью и конвекцией, а второе слагаемое – долю излучаемого тепла. При распылении и затвердевании сплавов в вещественной среде (газ, жидкость) вклад лучистого теплообмена мал и им обычно пренебрегают.
Среднюю скорость охлаждения капель металлического расплава для типичного случая распыления в вещественной среде можно представить в общем виде:
Vохл =  , (1.41)
, (1.41)
где k – константа для данного расплава.
Очевидно, что скорость охлаждения расплава будет тем выше, чем меньше капля расплава и больше коэффициент теплоотдачи с ее поверхности.
Величина коэффициента a обычно находится по формулам общей теории теплообмена с использованием критериев подобия. В условиях вынужденного движения газа или жидкости (вынужденная конвекция) интенсивность теплообмена характеризуется критерием Нуссельта:

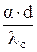 , (1.42)
, (1.42)
где d – характерный размер тела, в данном случае размер капли расплава; lс – коэффициент теплопроводности окружающей среды.
В свою очередь критерий Нуссельта является функцией критериев Рейнольдса и Прандтля:
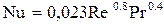 . (1.43)
. (1.43)
Критерий Рейнольдса определяет гидромеханическое подобие течения среды
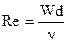 , (1.44)
, (1.44)
где W – относительная скорость движения среды (газа или жидкости); n - коэффициент кинематической вязкости среды.
Критерий Прандтля является теплофизической характеристикой
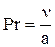 , (1.45)
, (1.45)
где а – коэффициент температуропроводности среды.
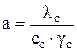 , (1.46)
, (1.46)
где lс, сс, gс – коэффициент теплопроводности, удельная теплоемкость и плотность среды, соответственно.
При теплообмене в газе формула (1.43) упрощается, поскольку для двухатомных газов Рr = 0,72 и критерий Нуссельта будет зависеть только от изменения критерия Рейнольдса. При малых значениях критерия Рейнольдса (Re < 150) критерий Нуссельта определяют по формуле:
Nu = 2 + 0,16 Re1/2. (1.47)
При значениях Rе > 150 используют другую формулу:
Nu = 0,62 Re1/2. (1.48)
В качестве примера, выполним расчет средней скорости охлаждения капель расплава инструментальной стали при распылении высокоскоростным потоком азота. Для расчета примем следующие, близкие к практике распыления, исходные данные:
‑ размер капель расплава – 100 мкм (1×10-4 м); абсолютные температуры расплава Тп и окружающий среды Тс – 1800Ки 300К, соответственно;
‑ скорость газа – 100 м/с;
‑ коэффициент кинематической вязкости газа, n = 7,9×10 -5 м2/с;
‑ коэффициент теплопроводности газа, lс = 2,6×10 -2 Вт/(м×К);
‑ плотность расплава стали, gж = 7×103кг/м3;
‑ теплоемкость расплава стали, ср @ 840 Дж/(кг×К).
По формуле (1.44) определяем критерий Рейнольдса:
Re = 100 ·1·10-4 / 7,9·10-5 = 126,6
По формуле (1.47) определяем критерий Нуссельта:
Nu = 0,62 ·126,61/2 ≈ 6,98
Определим коэффициент теплоотдачи, используя формулу (1.42):
α = Nu·lс / d = 6,98·2,6×10 -2 / 1·10-4 ≈ 1,5·103 Вт/(м2×К)
С учетом (1.40) и пренебрегая излучением, получим среднюю скорость охлаждения:
Vохл = 6·1,5·103 (1800-300) / 1·10-4·7·103·840 ≈ 2,3·104 К/c.
1.11.3. Формообразование распыленных частиц
В отделенных от струи расплава жидких каплях сохраняются пульсирующие волновые колебания. В случае усиления пульсации за счет аэродинамических сил взаимодействия с окружающей средой процесс деления капель продолжается. При затухании пульсации силы поверхностного натяжения стремятся придать капле сферическую форму. Период колебаний капли и время их затухания зависят от вязкости расплава и поверхностного натяжения. Очевидно, что время, необходимое для сфероидизации (tсф) жидкой капли размером d должно быть меньше времени ее затвердевания:
tсф < (t1+t2), (1.49)
где t1 – время охлаждения капли до температуры затвердевания Т3; t2 – время затвердевания с выделением скрытой теплоты затвердевания.
Значения t1, t2 и tсф могут быть рассчитаны по формулам:
t1 = dcрγж · ln [(ТП-ТС) / (ТЗ – ТС)] / 6α, (1.50)
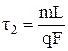 , (1.51)
, (1.51)
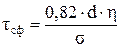 . (1.52)
. (1.52)
Рассчитаем значения t1, t2 и tсф для случая распыления стали при следующих значениях исходных данных:
‑ температура затвердевания расплава, Тз = 1600 К;
‑ коэффициент динамической вязкости, h = 0,0054 Па×с;
‑ поверхностное натяжение расплава, s = 1,83 Н/м;
‑ скрытая теплота затвердевания, L = 2,6×105 Дж/кг;
‑ поверхность капли, F = 3,14×10-8 м2;
‑ масса капли, m = 3,66×10-9 кг.
Остальные исходные данные те же, что и в предыдущем расчете скорости охлаждения капель расплава.
В соответствии с (1.50):
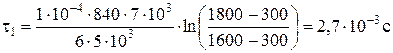
 .
.
Для расчета t2 предварительно определим величину теплового потока: 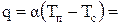 1,5×103×1500 ≈ 2,25×106 Вт/м2.
1,5×103×1500 ≈ 2,25×106 Вт/м2.
Подставив численные значения в (1.51), получим:
t2 = 3,66·10-9 · 2,6·105 / 2,25·106 · 3,14·10-8 ≈ 1,35·10-2 c.
Cуммарное время полного затвердевания капли:
t = t1 + t2 ≈ 2,7·10-3 + 1,35·10-2 ≈ 1,62·10-2 с.
Время сфероидизации капли в соответствии с (1.52):
tсф = 0,82 · 1·10-4 · 5,4·10-3 / 1,83 ≈ 2,43·10-7 c.
Очевидно, что tсф << (t1+t2), следовательно, капля успеет сфероидизироваться до полного затвердевания. Однако такой вывод справедлив для условий распыления расплава в газовой атмосфере без существенного окисления капель. Взаимодействие капель расплава с кислородом, как уже отмечалось, приводит к образованию оксидных пленок на поверхности, причем пленка из тугоплавких оксидов сдерживает процесс сфероидизации и в этом случае форма порошковых частиц может отличаться от сферической. При распылении струи расплава потоком воды, капли, в связи с более интенсивным охлаждением, часто сохраняют неправильную форму. Время сфероидизации капель возрастает с увеличением вязкости расплава и уменьшением сил поверхностного натяжения. Вводя в расплав различные добавки, изменяющие его свойства, можно, в определенной мере, регулировать форму частиц. В частности, введение в расплав железа небольших добавок алюминия, цинка, марганца, лития, титана, кальция и магния (от 0,05 до 2 % по массе) сопровождается уменьшением поверхностного натяжения расплава и способствует получению распыленных порошков неправильной формы.
1.11.4. Кристаллизация распыленных частиц
Еще в 1878 г. Д.К. Чернов, исследуя структуру литой стали, отметил, что кристаллизация металла состоит из двух элементарных процессов. Первый представляет собой зарождение мельчайших кристаллических частиц, а второй ‑ рост этих частиц. Систематические исследования процесса образования центров кристаллизации и их роста вначале на прозрачных органических жидкостях, а затем и на металлах были выполнены Г. Тамманом. В результате была сформирована теория самопроизвольной или гомогенной кристаллизации, суть которой сводится к следующему. В металлических расплавах при температуре несколько ниже, чем температура равновесной кристаллизации, под воздействием флуктуаций энергии возникают упорядоченные агрегаты атомов - кластеры, способные при дальнейшем понижении температуры самопроизвольно стать твердой частицей - центром кристаллизации. Часть таких центров продолжает рост с определенной скоростью. Число центров кристаллизации (ЧЦ), возникающих в единицу времени, и линейная скорость их роста, скорость кристаллизации (СК), определяются величиной переохлаждения (DТ):
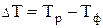 , (1.53)
, (1.53)
где Тр ‑ равновесная температура кристаллизации; Тф ‑ фактическая температура кристаллизации.
Графически изменение параметров кристаллизации ЧЦ и СК в зависимости от величины переохлаждения показано на рис. 1.19. При равновесной температуре кристаллизации, когда DТ = 0, значения ЧЦ и СК также равны нулю. С появлением и по мере увеличения переохлаждения значения ЧЦ и СК возрастают, проходят через максимум и снижаются до нуля. Рост величин ЧЦ и СК объясняется тем, что с увеличением переохлаждения возрастает разность свободных энергий жидкого и твердого состояний.
| Скорость кристаллизации Число центров | 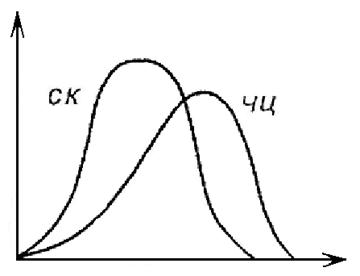 Степень переохлаждения
Степень переохлаждения
|
| Рис. 1.19. Параметры кристаллизации в зависимости от степени переохлаждения |
Последующее уменьшение ЧЦ и СК при больших переохлаждениях связано с повышением вязкости и уменьшением диффузионной подвижности атомов. При очень большом переохлаждении подвижность атомов может стать настолько низкой, что они не смогут сформировать правильную кристаллическую решетку и расплав затвердеет в аморфном, стеклообразном состоянии.
Следует иметь в виду, что далеко не все образующиеся в расплаве зародыши способны к дальнейшему росту. Изменение термодинамического потенциала системы при образовании зародыша радиусом r в изотермических условиях описывается формулой:
 , (1.54)
, (1.54)
где j1, j2 - термодинамические потенциалы жидкой и твердой фаз s - поверхностное натяжение на границе раздела фаз.
Первый член формулы (1.54) представляет изменение объемной энергии, а второй - поверхностной. Термодинамический потенциал жидкой и твердой фаз в условиях равновесия одинаков j1 = j2 . С появлением переохлаждения, когда температура расплава ниже равновесной температуры кристаллизации, твердая фаза становится более устойчивой (j2 < j1). Величина переохлаждения тем больше, чем больше разность (j1 - j 2). Поскольку второй член уравнения (1.54) всегда имеет положительное значение, то образование зародышей может происходить только в переохлажденной жидкости и в том случае, когда изменение свободной энергии фаз перекроет по величине значение поверхностной энергии, затраченной на образование поверхности раздела.
Способными к росту могут быть зародыши, размер которых больше некоторой критической величины rk. Критический размер зародыша соответствует максимуму кривой и может быть определен из условия:
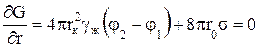 . (1.55)
. (1.55)
В соответствии с (1.55) критический размер зародыша определится равенством:
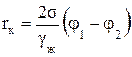 . (1.56)
. (1.56)
Изложенные представления о гомогенном зарождении центров кристаллизации неоднократно подвергались критике. Еще в работах А.А. Бочвара, К.П. Бунина и других отмечалось, что реальные технические расплавы содержат нерастворимые взвешенные частицы, которые могут служить готовыми центрами кристаллизации при минимальных переохлаждениях. При наличии таких частиц в расплаве не может развиться глубокое переохлаждение, следовательно, сам процесс кристаллизации является не гомогенным, а гетерогенным.
Автором исследовалась структура литого молибдена, образцы которого были получены в различных условиях охлаждения. На рис. 1.20а демонстрируется фотография макроструктуры слитка, выплавленного электродуговым способом в медном охлаждаемом водой кристаллизаторе.

А)
Б)
В)
Рис. 1.20. Макро и микроструктура литого молибдена:
а – слиток с столбчатой структурой, Vохл < 1 К/c;
б – слиток с равноосной структурой, Vохл ≈ 1 К/c;
в – гранула, Vохл ≈ 104 К/c, х350
Слиток затвердевает при мощном тепловом воздействии электрической дуги на лунку расплава. При этом способе плавки первые кристаллы появляются в начальный период на поверхности затравки и стенках кристаллизатора, которые служат готовой поверхностью раздела. Последующий рост возникших кристаллов происходит в глубь расплава в направлении, обратном градиенту температуры. Перед фронтом кристаллизации возникает минимальная по величине и протяженности зона термического переохлаждения, достаточного для роста кристаллов и недостаточного для возникновения новых центров кристаллизации. Поперечный размер столбчатых кристаллов определяется числом центров кристаллизации, возникших в первоначальный момент плавки при формировании жидкой лунки расплава. Чем выше температура перегрева расплава и меньше содержание в нем растворимых примесей, тем меньше возникает кристаллов и соответственно больше их поперечный размер.
При заливке молибденового расплава в медную изложницу резко меняется характер его кристаллизации (рис. 1.20б). Центры кристаллизации, очевидно, возникают во всем объеме расплава, причем размер зерна одинаков в центре слитка и у его поверхности. Расчетная скорость охлаждения слитка Æ 60 мм при массе 5 кг составила 7·102 К/с.
На рис. 1.20в иллюстрируется микроструктура молибденовой гранулы Æ 0,5 мм. Расплав распыляли центробежным способом в вакууме. Расчетная скорость охлаждения ~ 104 К/с. Характер структуры гранулы такой же как у слитка, залитого в изложницу. Важно то, что в момент кристаллизации молибденовая капля не имела контакта с вещественной средой, следовательно, можно полагать, что в данном случае имела место только гомогенная объемная кристаллизация. В пользу этого предположения говорит и то, что в жидком молибдене, температура которого с учетом перегрева составляет около 3000°С, вряд ли могут быть нерастворимые примеси, способные играть роль центров кристаллизации. При объемной кристаллизации должно выполняться условие:
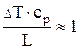 , (1.57)
, (1.57)
где  и L – удельная теплоемкость и скрытая теплота затвердевания расплава.
и L – удельная теплоемкость и скрытая теплота затвердевания расплава.
Принимая известные для молибдена значения  = 435 Дж/кг×°С и L = 290×103 Дж/кг можно приближенно оценить величину переохлаждения DТ» 667°С.
= 435 Дж/кг×°С и L = 290×103 Дж/кг можно приближенно оценить величину переохлаждения DТ» 667°С.
Более поздние исследования других авторов показали, что в мелких каплях расплава могут развиваться еще более значительные переохлаждения. В табл. 1.8 представлены значения глубины переохлаждения для различных металлов в каплях диаметром 10 - 15 мкм.
Таблица 1.8






