Общие положения
Электролитическое получение порошков представляет собой выделение металла разложением водных растворов или бескислородных расплавленных солей путем пропусканием через них постоянного электрического тока. Используемые при электролизе растворы и расплавы солей называют электролитами. Электролиты являются проводниками второго рода, передача электричества в них осуществляется движением положительных и отрицательных ионов, образующихся за счет диссоциации молекул электролита. Процесс электрохимического превращения происходит непосредственно на границе электрод - электролит. Источник электрического тока играет роль своеобразного насоса, «перекачивающего» электроны с одного полюса цепи на другой. В результате такой «перекачки» на катоде образуется избыток отрицательно заряженных электронов, и он приобретает отрицательный заряд, соответственно другой электрод (анод), лишившийся электронов, приобретает положительный заряд.
Источником ионов выделяемого металла служит анод, содержащий этот металл, и электролит, в состав которого входит раствор или расплав соединения соответствующего металла. При отсутствии электрического тока ионы в электролите движутся хаотически. Внешнее электрическое поле, наложенное на электролит, создает упорядоченное движение ионов: положительно заряженные ионы (катионы) движутся к катоду, а отрицательно заряженные (анионы) ‑ к аноду. Чем выше напряжение, приложенное к электродам, тем больше скорость ионов. В соответствии с величиной напряжения, требуемого для выделения металла на катоде, металлы располагаются в определенной последовательности, образуя ряд напряжений, например цинк, железо, олово, медь, серебро, золото. Чем левее в этом ряду находится металл, тем он более электроотрицателен и требует большего напряжения на катоде для его выделения. Чем больше сродство металла к кислороду, тем труднее его выделить из водных растворов. Поэтому алюминий, магний, цирконий, титан и другие, химически активные металлы выделяют из расплавов солей, а не из водных растворов.
Количество катодного осадка при электролитическом выделении прямо пропорционально силе тока, времени его прохождения через электролит и электрохимическому эквиваленту металла (закон Фарадея). Однако реальное количество осадка, получаемое на практике всегда меньше расчетного. Это связано с совместным разрядом на катоде ионов нескольких элементов и с утечкой тока, из-за несовершенной электроизоляции. Для оценки степени несовпадения расчетных и практически получаемых количеств осадка используют показатель А, называемый выходом по току, %:
А = (qp/qт) · 100, (1.25)
где qp – масса вещества, реально выделившегося вещества; qт – расчетная масса вещества, которая должна выделиться в соответствии с законом Фарадея.
Например, при производстве электролизом меди за сутки было получено 235 кг (qp) порошка. Электролиз проводился при силе тока 10000 А. Электрохимический эквивалент меди 1,1858 г/(А·ч). Соответствующее расчетное количество меди должно составить:
qт=1,1858·10000·24=284,6 кг.
Выход по току: А = (235/284,6)·100 = 82,5 %.
Для питания электролизеров служат специальные электроподстанции, оборудованные преобразователями переменного тока в постоянный. Преобразователями служат мотор-генераторы, ртутные преобразователи, кремниевые или германиевые выпрямители. Переменный ток промышленной частоты 50 Гц и напряжением 10000 В преобразуется в постоянный ток силой до 25000 А при напряжении 425 В.
Сила тока на рабочей поверхности электролизера – основной параметр, определяющий производительность электролиза. Сила тока, отнесенная к суммарной поверхности катодов и анодов, определяет катодную и анодную плотность тока. Катодная и анодная плотность тока обычно не совпадают, поскольку различаются рабочие поверхности катодов и анодов. Повышение плотности тока увеличивает число ионов, разряжающихся на катоде и соответственно повышает производительность, однако чрезмерная катодная плотность тока сопровождается выделением на катоде побочных элементов и снижает выход по току. Неприемлема и излишняя анодная плотность тока, поскольку при этом может возникнуть, так называемый «анодный эффект». Этот эффект представляет собой ухудшение смачиваемости анода электролитом в результате искрения и образования газовой прослойки. Это приводит к прекращению выделения металла на катоде. Анодный эффект может иметь место как при электролизе водных растворов, так и при электролизе расплавов. В целом, электролиз, по сравнению с другими способами производства порошков, отличается универсальностью и обеспечивает возможность получения порошков с высоким уровнем чистоты и хорошими технологическими свойствами. Существенными недостатками электролиза являются высокая энергоемкость и сравнительно низкая производительность.
Электролиз водных растворов
В настоящее время в промышленном масштабе способом электролиза водных растворов производят порошки меди, железа, хрома, никеля, кобальта, цинка, кадмия, свинца, олова, сурьмы, серебра и некоторых редких металлов и их сплавов. В зависимости от условий электролиза, пригодные для производства порошков катодные осадки, обычно подразделяют на три группы.
1. Твердые, хрупкие, плотные осадкиникеля, кобальта, железа, хрома, образуются в тех случаях, когда электролиз проводят при незначительных концентрациях водородных ионов, повышенных содержаниях ионов выделяемого металла и низких плотностях тока.
2. Губчатые мягкие осадки представляют собой скопления отдельных мелких кристаллов, легко поддающихся растиранию. Такие осадки получают при сравнительно низкой плотности тока, повышенной кислотности раствора и уменьшенной концентрации в электролите катионов выделяемого металла.
3. Рыхлые, или черные осадки являются высокодисперсными порошками, которые получаются в готовом виде непосредственно в процессе электролиза. Получению таких порошков способствуют высокая плотность тока, повышенная кислотность электролита и наличие в нем некоторых примесей, или осаждаемого металла в составе комплексного аниона.
На рис. 1.13 в качестве типового примера, приведена технологическая схема производства медного порошка электролизом кислого раствора сернокислой меди. Аноды представляют собой плиты катодной меди размером 880х980х10 мм. Электролитом является сернокислый раствор сульфата меди СuSO4. При диссоциации веществ, составляющих электролит, образуются катионы меди Сu2+ и водорода Н+, а также анионы SO42- и ОН-. Катоды могут быть пластинчатого или стержневого типа. Пластинчатые катоды представляют собой листы катодной меди размером 830х930х(3-4) мм, а стержневые катоды – медные трубки диаметром 12-16 мм с толщиной стенки 3 мм. Анодов в ванне электролизера всегда на один больше, чем катодов (например, 12 листовых катодов и 13 анодов), так что крайними всегда являются аноды, а вся поверхность любого из катодов является рабочей. Расстояние между центрами одноименных электродов примерно 150 мм.
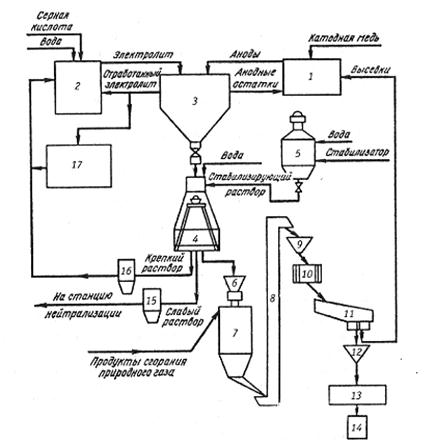
Рис. 1.13. Технологическая схема получения электролитического медного порошка: 1 – плавильное устройство; 2 – узел корректировки электролита; 3 – электролиз; 4 – промывка, стабилизация и
обезвоживание порошка; 5 – приготовление стабилизирующего
раствора; 6,9,12 – бункеры-накопители порошка; 7 – сушилка;
8 – элеватор; 10 – дробилка; 11 – классификатор; 13 – смеситель;
14 – узел упаковки готовой продукции; 15,16 – ловушки для порошка; 17 – узел регенерации электролита
Типовой состав электролита и режим электролиза:
‑ катодная плотность тока, А/см2 …………….. 1800-3250;
‑ концентрация ионов меди, г/л ……………… 10-16;
‑ концентрация серной кислоты, г/л …………. 125-180;
‑ температура электролита, ºC ………………... 48-55;
‑ циркуляция электролита, л/мин …………….. 40-60;
‑ напряжение на ванне, В ……………………… 1,3-1,7.
Конструкция ванн для электролиза обычно ящичного или бункерного типа с деревянным, железобетонным или металлическим каркасом, футерованным кислотостойким материалом (винипласт, сурьмянистый свинец, пластмассы). Емкость ванн 2-5 м3. Ванны в электрическую цепь включают последовательно, а электроды в них – параллельно. Соответственно одинаковы силы тока (8000 – 12500 А) в каждой из 17 – 24-х ванн серии и напряжение между электродами, такое же, как напряжение на ванне. Медный порошок снимают с катода специальными скребками из нержавеющей стали через каждые 1 – 2 ч работы ванны.
Выравнивание концентрации ионов в объеме электролита осуществляется системой замкнутой рециркуляции, при которой за 1 ч происходит примерно десятикратный обмен электролита. Одновременно с циркуляцией осуществляют регенерацию электролита, поскольку при электролизе происходит существенное изменение его состава – электролит обогащается медью. Регенерация обеспечивается включением в сблокированную систему специальных регенеративных ванн с нерастворимыми свинцовыми анодами. Необходимое число таких ванн в системе определяется в зависимости от прироста концентрации меди в электролите и некоторых других факторов. Обычно это пятая, шестая или седьмая ванна в серии. В регенеративных ваннах выделение меди на катоде уменьшает концентрацию ее катионов в электролите, а на аноде образуется кислород и происходит регенерация серной кислоты. По мере накопления примесей часть электролита выводят из системы циркуляции, а вместо него вводят свежий электролит.
Счищенный с катодов медный порошок периодически выгружают из ванны без ее отключения. Выгрузка порошка осуществляется специальной гидровакуумной системой. Механически захваченный с порошком электролит отмывают горячей водой в специальных промывателях, в которых вода фильтруется через слой порошка, находящегося на сетчатом днище из нержавеющей стали. Расход воды – 10 м3 на 1 т порошка. После обработки горячей водой проводят стабилизацию порошка, промывая его раствором хозяйственного мыла или мылонафта (400 г мыла на 1 м3 воды), для создания гидрофобной пленки, защищающей порошок от коррозии. Расход стабилизирующего раствора 6 м3 на 1 т порошка. Избыток стабилизатора удаляют промывкой порошка в холодной воде.
После промывки порошок обезвоживают и сушат. Наиболее эффективно обезвоживание в центрифугах. Содержание влаги после центрифугирования снижается до 8-10 %. Обезвоженный порошок сушат в специальных вращающихся барабанах воздухом при 100 ºC или в кипящем слое продуктами конверсии природного газа. Высушенный порошок измельчают в мельницах непрерывного действия с устройством для рассева порошка на фракции. После просева, путем смешивания порошка одной марки, формируются отдельные партии порошка массой около 1т. Затем порошок затаривают в стальные барабаны массой по 75 – 80 кг.
По ГОСТ 4960-75 предусмотрено изготовление электролитического порошка меди шести марок: ПМ-порошок нестабилизированный; ПМС-А, ПМС-1, ПМС-В – порошок стабилизированный, ПМС-К – порошок стабилизированный конопаточный, ПМС-Н – порошок стабилизированный низкодисперсный. Порошки различаются по содержанию примесей и гранулометрическому составу. Влажность порошка – менее 0,05 %. Содержание сернокислых соединений металлов – менее 0,01 % и прокаленного осадка после обработки азотной кислотой – менее 0,05 %. В табл. 1.3 и 1.4 приводится химический и гранулометрический состав медных порошков.
Таблица 1.3
Химический состав (%) и насыпная плотность (г/cм3)






