
Оксигеновмісні кислоти та їх ангідриди
| Ангідрид | Формула кислоти | Назва кислоти |
| B2O3 CO2 SiO2 N2O3 N2O5 P2O3 P2O5 SO2 SO3 SeO2 SeO3 TeO2 TeO3 Cl2O Cl2O3 Cl2O5 Cl2O7 CrO3 – Mn2O7 – | HBO2 H2B4O7 H3BO3 H2CO3 H2SiO3 H4SiO4 HNO2 HNO3 H3PO3 HPO3 H4P2O7 H3PO4 H2SO3 H2SO4 H2SeO3 H2SeO4 H2TeO3 H6TeO6 HClO HClO2 HClO3 HClO4 H2CrO4 H2Cr2O7 H2MnO4 HMnO4 H2FeO4 | метаборатна тетраборатна ортоборатна карбонатна метасилікатна ортосилікатна нітритна нітратна ортофосфітна метафосфатна дифосфатна ортофосфатна сульфітна сульфатна селенітна селенатна телуритна ортотелуратна гіпохлоритна хлоритна хлоратна перхлоратна хроматна дихроматна манганатна перманганатна фератна |
ДОДАТОК В
Відносні електронегативності елементів

ДОДАТОК Г
Вплив знака ∆Н і ∆S на направленність і характер проходження реакції
| № п/п | З н а к | Характер реакції | ||
| ∆Нр | ∆Sр | ∆Gp | ||
| – | + | – | Реакція необоротна і проходить повністю в прямому напрямку | |
| + | – | + | Реакція необоротна і проходить в зворотному напрямку. В прямому напрямку реакція термодинамічно неможлива | |
| – | – | + або – (в залежності від абсолютних величин ∆Н, ∆S, Т) | Реакція оборотна. Низькотемпературний режим сприяє проходженню реакції в прямому напрямку, а високотемпературний – в зворотному. | |
| + | + | + або – (в залежності від абсолютних величин ∆Н, ∆S.Т) | Реакція оборотна Високотемпературний режим сприяє проходженню реакції в прямому напрямку, а низькотемпературний – в зворотному |
Термодинмічні константи деяких речовин
| Речовина | ΔН0 | ΔG0 | S0 | Речови-на | ΔН0 | ΔG0 | S0 |
| AgCl | -127,2 | -109,9 | +96,2 | KCl | -435,9 | -408 | +82,56 |
| AlCl3 | -704,6 | -629,0 | +109,4 | KBr | -392,2 | -379,2 | +96,4 |
| Al(OH)3 | -1315 | -1157 | +70,1 | KMnO4 | -813,4 | -713,8 | +171,71 |
| Al2O3 | -1676,8 | -1583,3 | +50,95 | KNO3 | -493,2 | -393,1 | +132,93 |
| BaCO3 | -1217,1 | -1137,2 | +113,0 | K2SO4 | -1433,7 | -1316,4 | +175,7 |
| BaCl2 | -859,1 | -811,4 | +123,8 | MgCl2 | -641,1 | -591,6 | +89,8 |
| BaO | -553,9 | -525,4 | +70,5 | MgO | -601,8 | -569,6 | +26,9 |
| BaSO4 | -1474,2 | -1363,2 | +132,3 | N2 | +199,6 | ||
| C (алмаз) | +1,828 | +2,834 | +2,37 | NH3 | -46,19 | -16,7 | +192,6 |
| С (графіт) | +5,74 | NO | +90,31 | +80,6 | +210,7 | ||
| CO | -110,6 | -137,2 | +197,7 | NO2 | +33 | +51,5 | +240,2 |
| CO2 | -393,8 | -394,6 | +213,8 | NaCl | -411,1 | -384,0 | +72,12 |
| CaC2 | -59,9 | -64,9 | +70 | Na2CO3 | -1137,5 | -1047,5 | +136,4 |
| CaCO3 | -1207,7 | -1129,6 | +91,6 | O2 | +205,0 | ||
| CaCl2 | -796,3 | -748,9 | +104,7 | O3 | -142,3 | -162,7 | +238,8 |
| CaO | -635 | -603,6 | +39,7 | H2O(г) | -241,98 | -228,8 | +188,9 |
| Ca(OH)2 | -986,8 | -899,2 | +83,4 | H2O(р) | -286,0 | -237,4 | +70,0 |
| Cl2 | +222,9 | P (черв.) | -17,6 | -12,13 | +22,8 | ||
| HCl(г) | -92,4 | -94,5 | +186,9 | H2S | -21 | -33,8 | +205,7 |
| CuCl2 | -215,7 | -171,5 | +108,2 | H2SO4 | -814,2 | -690,3 | +156,9 |
| CuSO4 | -771,4 | -662,2 | +109,3 | SiO2 | -911,6 | -857,2 | +41,9 |
| Fe | +27,2 | ZnCl2 | -415,33 | -369,6 | +111,54 | ||
| FeCl3 | -399,7 | -334,2 | +142,4 | ZnS | -205,6 | -200,85 | +57,78 |
| FeO | -265,0 | -244,5 | +60,8 | ZnO | -348,0 | -318,2 | +43,9 |
| FeSO4 | -929,5 | -825,5 | +121 | ZnSO4 | -978,6 | -871,6 | +124,7 |
| Fe2O3 | -822,7 | -740,8 | +87,5 | SO2 | -297,2 | -300,41 | +248,2 |
| Fe3O4 | -1117,9 | -1014,8 | +146,3 | PCl3 | -287,02 | -260,5 | +311,7 |
| H2 | 130,7 | PCl5 | -374,89 | -305,4 | +364,5 |
ДОДАТОК Д
Розчинність кислот, основ та солей у воді
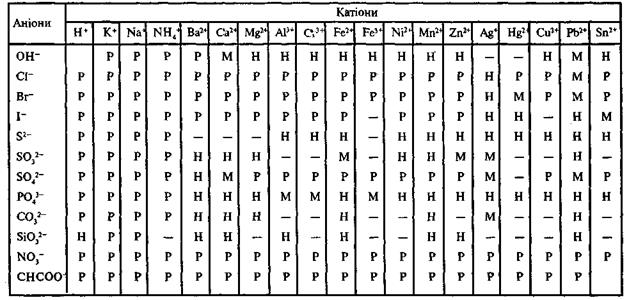
Примітка. P- розчинна, M - малорозчинна, H - практично нерозчинна,
прочерк - сполука розкладається водою або не існує.
ДОДАТОК Ж
Ряд стандартних електронних потенціалів







