В сухую пробирку помещают 2 капли этилового спирта, 2 капли раствора марганцевокислого калия и 3 капли раствора серной кислоты. Осторожно нагревают содержимое пробирки над пламенем горелки, Розовый раствор обесцвечивается. Ощущается характерный запах уксусного альдегида, который можно обнаружить также по цветной реакции с фуксинсернистой кислотой.
Химизм процесса: (написать уравнение реакции).
Спирты окисляются легче, чем соответствующие предельные углеводороды, что объясняется влиянием имеющейся в их молекуле гидроксигруппы. Первичные спирты превращаются при окислении в альдегиды в мягких условиях, в кислоты – в более жестких условиях. Вторичные спирты дают при окислении кетоны.
Взаимодействие изоамилового спирта с серной кислотой
В пробирку помещают 4 капли серной кислоты (d = 1,84 г/мл) и осторожно, при встряхивании и охлаждении, добавляют 2 капли изоамилового спирта. Полученную однородную, почти без запаха жидкость оставляют постоять 2-3 мин. Затем 3-4 капли продукта помещают в пробирку с 5-6 каплями холодной воды. Образуется прозрачный, не имеющий запаха раствор изоамилсерной кислоты, которая представляет собой кислый (неполный) сложный эфир изоамилового спирта и серной кислоты. (Схема превращений).
Если при смешивании изоамилового спирта с кислотой произошло разогревание, то водный раствор получается мутным и появляется запах диизоамилового эфира.
Спирты образуют сложные эфиры не только с минеральными кислотами, но и с органическими. Получение этилацетата, а также механизм реакции этерификации будут изучены позже.
Получение диэтилового эфира
В сухую пробирку вводят 2 капли этилового спирта и 2 капли серной кислоты. Смесь осторожно нагревают над пламенем горелки до побурения раствора. К горячей смеси очень осторожно добавляют еще 2 капли этилового спирта. Ощущается характерный запах диэтилового эфира.
Диэтиловый эфир является продуктом межмолекулярной дегидратации этилового спирта, условиями протекания которой являются нагревание смеси, содержащей избыток спирта по отношению к содержанию серной кислоты (каталитическое количество) до 140оС. Если количество серной кислоты значительно больше, чем масса вступающего в реакцию спирта, то при нагревании до 160оС и выше реакция протекает по механизму внутримолекулярной дегидратации с образованием алкена.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Как влияют размер и строение углеводородного радикала на физические свойства спиртов? Поясните на примере этилового и гексилового спиртов.
2. Почему температура кипения этилового спирта значительно выше, чем диметилового эфира?
3. Расположите следующие соединения в порядке увеличения их кислотности: 2-метил-2-бутанол; 2-пентанол; 3-метил-1-бутанол; вода; метанол; аммиак; ацетилен.
4. Сравните отношение к НCI: н-бутилового, трет-бутилового и неопентилового спиртов. Укажите спирт, который взаимодействует с HCI только в присутствии ZnCI2.
5. Напишите уравнения реакций, характеризующих кислотные и основные свойства бутилового спирта.
6. Расположите в ряд по легкости дегидратации следующие спирты 4-метил-1-пентанол; 3-метил—бутанол; 3-метил-3-пентанол. Напишите уравнения меж- и внутримолекулярной дегидратации для одного из приведенных спиртов.
7. Напишите уравнения реакций первичного, вторичного и третичного спиртов состава С5Н12О с уксусной кислотой (в присутствии серной кислоты).
8. Напишите схемы реакций окисления первичного, вторичного бутилового спирта и 2-метил-1-бутанола.
9. Предложите для следующих соединений схемы синтеза, исходя из пропилового спирта и других необходимых реагентов: пропилена, изопропилового спирта, ацетона, дипропилового эфира.
10. Напишите уравнения реакций взаимодействия этиленгликоля с натрием, уксусной и азотной кислотами, а также уравнения реакций меж- и внутримолекулярной дегидратации.
11. С помощью каких реакций можно выделить 1-гексанол из смеси с гексаном и гексеном-1?
12. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: метан® ацетилен® этилен ® этанол ®1,3-бутадиен® бутан ®1-бутен ® 2-бутанол.
13. Какое влияние на свойства спиртов оказывает присутствие нескольких гидроксильных групп? Приведите соответствующие уравнения реакций.
ЛАБОРАТОРНАЯ РАБОТА №7
Тема: ФЕНОЛЫ
Цель работы: Практическое освоение характерных свойств фенолов и их отличительных особенностей.
Оборудование и реактивы: фенол кристаллический; насыщенный раствор фенола; едкий натр, 2н раствор; раствор фенолята натрия; соляная кислота, 2н раствор; углекислый кальций; хлорное железо, 0,1н раствор; бромная вода, насыщенный раствор; серная кислота (d=1,84 г/мл); азотная кислота (d=1,4 г/мл); нитрит натрия, 0,02н раствор; пирокатехин, 1% раствор; резорцин, 1% раствор; гидрохинон, 1% раствор; пирогаллол, 1% раствор, водяная баня; пробирки; стеклянные трубки с оттянутым концом; газоотводные трубки; капельная воронка.
Теоретическая часть
Органические соединения, у которых гидроксильная группа связана непосредственно с бензольным кольцом, называют фенолами ( Ar-OH ).
В зависимости от числа гидроксильных групп в ядре различают одно-, двух- и трехатомные фенолы.
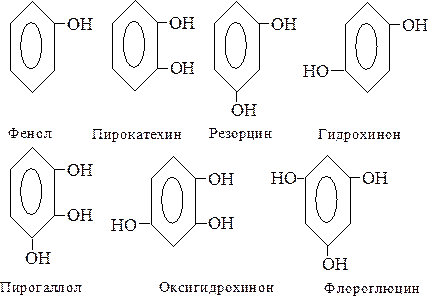 |
Методы получения
Фенол является одним из важных продуктов нефтехимии. Источником фенола и его метильных гомологов служит каменноугольная смола, кроме того в значительных количествах его получают синтетическими способами.
1. Кумольный способ:
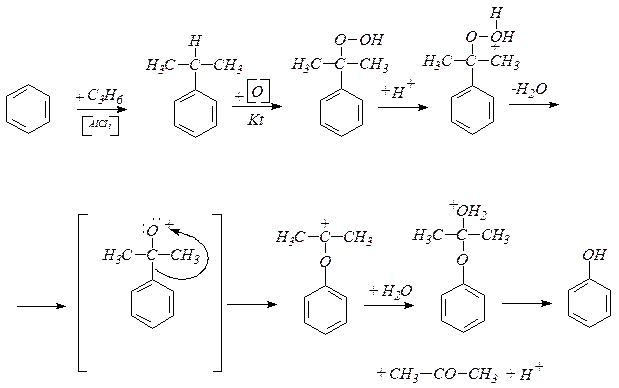
2. Сплавление солей сульфокислот с гидроксидом натрия:
С6Н5SO3Na + 2NaOH ¾® C6H5ONa + Na2SO3 + H2O
2C6H5ONa + CO2 + H2O ¾®2C6H5OH + Na2CO3
3. Гидроксилирование ароматических производных в жестких условиях при 300-350оС и 150-200 ат:
С6Н5CI + NaOH ¾® C6H5OH + NaCI
Двух- и трехатомные фенолы получают аналогичными способами.
4. В лаборатории фенолы получают гидролизом солей диазония путем нагревания подкисленных растворов:
C6H5 – N+=N + H2O ¾® C6H5OH + N2 + H+
Химические свойства
Большинство фенолов – бесцветные твердые вещества. Простейший фенол C6H5OH обладает характерным запахом, плавится при 42оС. Температура плавления фенола сильно понижается от примеси небольших количеств воды (кристаллогидрат C6H5OH•H2O плавится при 16оС). Фенол гигроскопичен, кристаллы его при стоянии на воздухе расплываются. Раствор фенола в воде обладает антисептическими свойствами. Пары фенола токсичны, а сам он вызывает ожоги кожи.
Химические свойства фенола определяются наличием гидроксигруппы и бензольного кольца, взаимно влияющих друг на друга
Сопряжение неподеленной электронной пары атома кислорода гидроксильной группы приводит к смещению электронной плотности в сторону бензольного кольца, что усиливает подвижность атома водорода. Фенолы являются более сильными кислотами, чем предельные одноатомные спирты (pКа =10). Кислотность фенолов зависит также от характера заместителей в ядре. Введение в ядро электроноакцепторных заместителей (нитрогруппы, атомов галогенов) приводит к увеличению кислотных свойств.
С другой стороны, являясь заместителем I рода, гидроксигруппа приводит к повышению электронной плотности в о- и п-положениях бензольного кольца, что облегчает реакции электрофильного замещения.
Двух- и трехатомные фенолы во многих химических реакциях обнаруживают сходство с одноатомными фенолами, участвуя одной, двумя или тремя гидроксигруппами. Двухатомные фенолы более сильные кислоты, чем одноатомный фенол. Они легко окисляются и являются сильными восстановителями. Пирокатехин при окислении образует о-бензохинон:
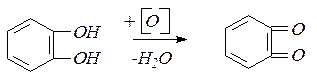
Две структуры – бензоидная и хиноидная – легко переходят друг в друга. Хиноидные группировки относятся к важным хромофорным системам в молекулах красителей.

К наиболее характерным химическим свойствам можно отнести следующие.
1. Проявляя кислотные свойства, фенол реагирует с гидроксидом натрия, образуя феноляты:

2. Фенолы легко алкилируются при действии на феноляты галогенпроизводных, особенно в присутствии порошка меди, а также при действии на фенол алкилсульфатов, эфиров сульфокислот или диазометана:

3. Фенол конденсируется с окисью этилена с образованием фенилового эфира полиэтиленгликоля:
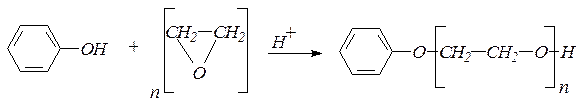
4. фенолы не этерифицируются непосредственно карбоновыми кислотами. Эфиры фенолов могут быть получены действием ангидридов или галогенангидридов кислот на феноляты или растворы фенолов в пиридине:

5. Гидроксильная группа в фенолах с большим трудом замещается на галоген:

6. При перегонке фенолов с цинковой пылью гидроксильная группа замещается на водород:
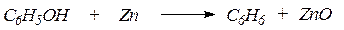
7. Галогенирование фенола действием растворов галогенов или галогенирующих средств идет с большой скоростью и преимущественно в пара -положение. Конечным продуктом галогенирования в ядро являются тригалогенофенолы. Возможно дальнейшее галогенирование:

8. Нитрование фенола идет уже при действии разбавленной азотной кислоты. При дальнейшем нитровании концентрированной азотной кислотой получается тринитрофенол – пикриновая кислота:

9. При сульфировании фенолов получаются о- и п- фенолсульфокислоты:

10. Фенолы легко конденсируются с альдегидами:
а) при действии щелочных или кислых катализаторов на смесь фенола и какого-либо альдегида жирного ряда происходит конденсация в о- и п- положениях при обычной температуре рост молекулы за счет конденсации фенола с альдегидом идет в линейном направлении:
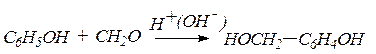
11. При действии на фенол перекиси водорода в присутствии железного катализатора получается с небольшим выходом пирокатехин:

При действии на фенол хромовой смесью образуется п- бензохинон и продукты его дальнейших изменений:

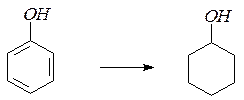
12. При гидрировании водородом в присутствии катализатора фенолы превращаются в спирты ряда циклогексана:
Экспериментальная часть
Растворение фенола в воде
В пробирку помещают 2 капли жидкого фенола, прибавляют 2 капли воды и взбалтывают. Образуется мутная жидкость – эмульсия фенола. Дают содержимому пробирки отстояться. После отстаивания эмульсия постепенно расслаивается: верхний слой – раствор фенола в воде, нижний – раствор воды в феноле. Фенол плохо растворим в холодной воде.
Осторожно нагревают содержимое пробирки – получается однородный раствор. При охлаждении вновь образуется мутная жидкость. При повышении температуры увеличивается как растворимость фенола в воде, так и растворимость воды в феноле, и при 68оС они смешиваются друг с другом в любых соотношениях.
Получение фенолята натрия
В пробирку помещают 4 капли эмульсии фенола в воде и добавляют 2 капли раствора едкого натра. Немедленно образуется прозрачный раствор фенолята натрия. Раствор оставляют для следующего опыта.
Написать уравнение реакции получения фенолята натрия.
Фенолы обладают кислотными свойствами, они легко вступают в реакцию с водными растворами щелочей, образуя аналогичные алкоголятам феноляты. По этой причине простейший фенол называют “карболовой кислотой”. Более сильный кислотный характер фенолов по сравнению со спиртами объясняется влиянием бензольного кольца.






