Ќеорганические соединени€ по составу дел€тс€ на гомо- и гетеросоединени€. √омосоединени€ Ц это вещества, состо€щие из атомов одного элемента. ќни подраздел€ютс€ на металлы и неметаллы. √етеросоединени€, или сложные вещества, состо€т из атомов двух или более элементов. ќни дел€тс€ на классы: оксиды, основани€, кислоты, соли.
ќсновани€ и кислородсодержащие кислоты часто рассматриваютс€ как гидраты оксидов и объедин€ютс€ в единый класс гидроксидов, имеющих основный, амфотерный или кислотный характер.
ќксидами называютс€ бинарные соединени€, в которых один из элементов Ц кислород со степенью окислени€ Ц2. Ќапример: 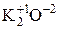 ,
, 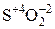 .
.
Ќазвание оксида состоит из слова Ђоксидї и названи€ элемента в родительном падеже. ѕеременна€ степень окислени€ указываетс€ в скобках:
Fe2O3 Ц оксид железа (III);
FeO Ц оксид железа (II);
Sќ2 Ц оксид серы (IV).
ќксиды дел€тс€:
Ц на несолеобразующие или безразличные (N2O, NO, CO, SiO);
Ц солеобразующие: а) основные; б) амфотерные; в) кислотные.
ќсновные оксиды Ц это оксидыметаллов со степенью окислени€ металла +1, +2. »сключение составл€ют оксиды BeO, ZnO, SnO, PbO, €вл€ющиес€ амфотерными. ќсновным оксидам отвечают гидроксиды Ц основани€. Ќапример:
ќсновной оксид
Na 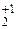 O
Ca+2O O
Ca+2O
| ќснование Na+1OH Ca+2(OH)2 |
јмфотерные оксиды Ц оксиды металлов со степенью окислени€ металла +3, +4 и BeO, ZnO, SnO, PbO со степенью окислени€ +2.
јмфотерным оксидам отвечают гидроксиды, про€вл€ющие как свойства кислот, так и свойства оснований. Ќапример:
јмфотерный оксид
Be+2O
Cr 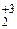 O3 O3
| ќснование Be+2(OH)2 Cr+3(OH)3 | ислота H2Be+2O2 HCr+3O2 |
ислотные оксиды Ц оксиды неметаллов с любой степенью окислени€ и оксиды металлов с высокими степен€ми окислени€ (выше +4).
ислотным оксидам отвечают гидроксиды Ц кислоты. Ќапример:
| ислотный оксид | ислота |
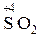
| 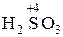
|
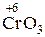
| 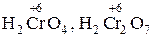
|
„тобы правильно написать формулу кислоты, соответствующую данному оксиду, к оксиду добавл€ем H2O и подсчитываем число атомов каждого элемента:
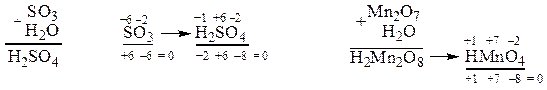
’имические свойства:
1. ќсновные оксиды (только оксиды щелочных и щелочноземельных металлов) при взаимодействии с водой дают основани€ Ц щелочи:
Na2ќ + H2O = 2NaќЌ
Bаќ + H2O = Bа(ќЌ)2
ислотные оксиды (кроме SiO2 и некоторых других) при взаимодействии с водой образуют кислоты:
SO3 + H2O = H2SO4
N2O3 + H2O = 2HNO2
јмфотерные оксиды с водой не взаимодействуют.
2. ќсновные и амфотерные оксиды реагируют с кислотами, образу€ соль и воду:
MgO(осн) + 2HCl = MgCl2 + H2O
Cr2O3(амф) + 6HCl = 2CrCl3 + 3H2O
3. ислотные и амфотерные оксиды взаимодействуют с основани€ми (амфотерные только со щелочами), образу€ соль и воду:
SO2(кисл) + 2KOH = K2SO3 + H2O
Al2O3(амф) + 2NaOH 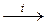 2NaAlO2 + H2O
2NaAlO2 + H2O
4. ќсновные оксиды реагируют с кислотными, образу€ соли:
Bаќ(осн) + SO3(кисл) = BaSO4
—аќ(осн) + Cl2O7(кисл) 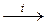 Ca(ClO4)2
Ca(ClO4)2
ѕолучение:
1. ќкисление простых и сложных веществ кислородом:
2Mg + O2 = 2MgO
2ZnS + 3O2 = 2ZnO + 2SO2
2. –азложение кислородсодержащих солей, оснований, кислот при нагревании:
|
|
|
—а—ќ3 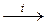 —аќ + —ќ2
—аќ + —ќ2
Cu(OH)2 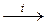 CuO + H2O
CuO + H2O
2H3PO4 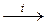 P2O5 + 3H2O
P2O5 + 3H2O
ќсновани€ми называютс€ вещества, образующие при диссоциации анионы одного вида, анионы гидроксила (ќЌЦ).
ќсновани€ дел€тс€:
Ц на хорошо растворимые в воде щелочи (гидроксиды щелочных и щелочноземельных металлов: NaOH, Ba(OH)2 и др.)и малорастворимые в воде основани€ (Fe(OH)2, Cu(OH)2 и др.);
Ц oднокислотные (LiOH, NH4OH) и многокислотные (Mg(OH)2, Sc(OH)3).
ислотность оснований определ€ют по числу гидроксогрупп, св€занных с металлом.
Ќазвание основани€ образуетс€ из слова Ђгидроксидї и названи€ металла в родительном падеже, причем дл€ металла с переменной степенью окислени€ указываетс€ степень окислени€. Ќапример, KOH Ц гидроксид кали€, но Fe(OH)2 Ц гидроксид железа (II).
’имические свойства:
1. ќсновани€ взаимодействуют с кислотами (реакци€ нейтрализации):
2LiOH + H2SO4 = Li2SO4 + 2H2O
Fe(OH)2 + 2HCl = FeCl2 + 2H2O
2. ќсновани€ реагируют с кислотными оксидами:
Ba(OH)2 + N2O3 = Ba(NO2)2 + H2O
2NaOH + SiO2 = Na2SiO3 + H2O
3. ўелочи взаимодействуют с растворами солей, если в результате реакции выпадает осадок:
FeCl3 + 3NaOH = Fe(OH)3¯ + 3NaCl
Ca(OH)2 + Na2CO3 = CaCO3¯ + 2NaOH
4. ќсновани€ (щелочи) реагируют с неметаллами:
Cl2 + 2KOH = KCl + K—lO + H2O
3S + 6NaOH = 2Na2S + Na2SO3 + 3H2O
5. ќсновани€ (щелочи) взаимодействуют с металлами, оксиды и гидроксиды которых амфотерны:
Zn + 2KOH + 2H2O = K2[Zn(OH)4] + H2
ѕолучение:
1. Ќерастворимые основани€ получают при взаимодействии растворов солей и щелочей:
FeCl3 + 3NaOH Ѓ Fe(OH)3¯ + 3NaCl
2. ўелочи получают:
а) преимущественно электролизом водных растворов солей:
2NaCl + 2H2O 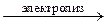 2NaOH + H2 + Cl2
2NaOH + H2 + Cl2
б) путем взаимодействи€ металлов с водой:
2Na + 2H2O = 2NaOH + H2
в) при взаимодействии оксидов с водой:
CaO + H2O = Ca(OH)2
ислотами называютс€ вещества, образующие при диссоциации катионы одного вида, катионы водорода (H+).
ислоты дел€тс€:
Ц на бескислородные (HCl, H2S) и кислородсодержащие (HNO3, H2SO4);
Ц одноосновные (HNO3, HClO4) и многоосновные (H2SO3, H3PO4).
ќсновность кислоты определ€ют по числу атомов водорода в кислоте, способных замещатьс€ на атомы металла.
Ќазвание кислородсодержащей кислоты дают по названию образующего ее элемента. ≈сли данный элемент образует несколько кислот, в которых про€вл€ет разные степени окислени€, то в названи€х этих кислот используют разные суффиксы. Ќазвани€ кислот, соответствующих высшей степени окислени€ элемента, содержат суффикс
Ђ-нї или Ђ-овї: HNќ3 Ц азот н а€, H3AsO4 Ц мышь€к ов а€. ¬ названии кислот, в которых элемент имеет меньшую степень окислени€, добавл€ют суффикс Ђ-истї: HNќ2 Ц азот ист а€, H3AsO3 Ц мышь€ков ист а€.
Ќазвание бескислородной кислоты дают по названию образующего ее элемента с добавлением слова Ђводородна€ї: HF Ц фтороводородна€ кислота, H2S Ц сероводородна€ кислота.
’имические свойства:
1. ислоты взаимодействуют с основани€ми (нейтрализаци€):
2HClO4 + —а(OH)2 = Ca(ClO4)2 + 2H2O
H3PO4 + 3KOH = K3PO4 + 3H2O
2. ислоты реагируют с основными и амфотерными оксидами:
H2SO4 + MgO = MgSO4 + H2O
2HNO3 + BeO = Be(NO3)2 + H2O
3. ислоты взаимодействуют с сол€ми, если в результате реакции образуетс€ осадок, газ или более слаба€ кислота:
H3PO4 + 3AgNO3 = Ag3PO4¯ + 3HNO3
2HCl + FeS = FeCl2 + H2S≠
NaNO2 + HCl = NaCl + HNO2
Ѕолее сильна€ и менее летуча€ кислота вытесн€ет слабые, малорастворимые и более летучие кислоты из их солей. —ила кислот уменьшаетс€ в следующем р€ду:
|
|
|
H2SO4,  , H2SO3, Ќ2—ќ3, H2SiO3
, H2SO3, Ќ2—ќ3, H2SiO3
4. ислоты реагируют с металлами, которые расположены в р€ду напр€жений до водорода, с выделением водорода (кроме HNO3 и H2SO4(конц)):
2HCl + Zn = ZnCl2 + H2
H2SO4(разб) + Mg = MgSO4 + H2
H2SO4(разб) + Cu ¹
но:
2H2SO4(конц) + Cu = CuSO4 + SO2 + 2H2O
9HNO3(разб) + 4Mg = 4Mg(NO3)2 + NH3 + 3H2O
5. ислоты взаимодействуют с неметаллами (концентрированные кислоты при нагревании):
5HNO3 + P = t H3PO4 + 5NO2 + H2O
ѕолучение:
1. –астворение кислотных оксидов в воде:
SO3 + H2O = H2SO4
Cl2O7 + H2O = 2HClO4
2. ¬ытеснение из солей действием более сильной кислоты:
Na2SiO3 + H2SO4 = Na2SO4 + H2SiO3
3. Ѕескислородные кислоты получают, раствор€€ в воде продукт взаимодействи€ простых веществ с водородом:
H2 + Cl2 = 2HCl
јмфотерные гидроксиды про€вл€ют как основные, так и кислотные свойства, реагиру€ с кислотами и щелочами:
Al(OH)3 + 3HCl Ѓ AlCl3 + 3H2O
Al(OH)3 + NaOH 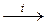 NaAlO2 + 2H2O
NaAlO2 + 2H2O
или
Al(OH)3 + NaOH Ѓ Na[Al(OH)4]
—ол€ми называютс€ соединени€, состо€щие из катионов металла и анионов кислотного остатка.
 —редние соли Ц продукты полного замещени€ водорода кислоты на металл или гидроксогрупп основани€ на кислотный остаток: Na2CO3, CaCl2, CuSO4, Ba3(PO4)2.
—редние соли Ц продукты полного замещени€ водорода кислоты на металл или гидроксогрупп основани€ на кислотный остаток: Na2CO3, CaCl2, CuSO4, Ba3(PO4)2.
ислые соли Ц продукты неполного замещени€ водорода многоосновных кислот на металл: NaHCO3, Ca(H2PO4)2.
ќсновные соли Ц продукты неполного замещени€ гидроксо≠групп многокислотных оснований на кислотный остаток: (CuOH)2Cќ3, FeOHSO4.
ƒвойные соли Ц это соли, образованные разными катионами и анионами одного вида: KFe(SO4)2.
—мешанные соли Ц это соли одного и того же катиона и различных анионов: Ca(OCl)Cl.
омплексные соли Ц это соли, содержащие комплексные ионы: Na3[AlF6], K3[Fe(CN)6].
Ќазвание средней соли состоит из латинского названи€ кислотного остатка и названи€ металла в родительном падеже, причем дл€ металлов, про€вл€ющих разные степени окислени€, указывают степень окислени€. ислотные остатки кислородсодержащих кислот содержат суффикс Ђ-атї, если образующий кислоту элемент имеет высшую степень окислени€, и Ђ-итї Ц в случае более низкой степени окислени€ элемента, например: Mg(N+5O3)2 Ц нитр ат магни€, Mg(N+3O2)2 Ц нитр ит магни€.
Ќазвани€ кислотных остатков бескислородных кислот содержат суффикс Ђ- идї, например: Ag2S Ц сульф ид серебра, CaCl2 Ц хлор ид кальци€.
Ќоменклатура кислых солей состоит из названи€ кислотного остатка и приставки Ђгидро - ї, Ђдигидро - ї и т. д., котора€ отражает число незамещенных на металл атомов водорода: KHSO4 Ц гидро сульф ат кали€, —a(H2PO4)2 Ц дигидро фосф ат кальци€.
Ќазвани€ основных солей содержат приставку Ђгидроксо - ї, Ђдигидроксо - ї и т. д. перед названием металла, котора€ отражает число незамещенных на кислотный остаток гидроксогрупп: (CuOH)2SO4 Ц сульфат гидроксо меди, Fe(OH)2ClO4 Ц перхлорат дигидроксо железа (III).
’имические свойства:
1. —оли реагируют с кислотами:
AgNќ3 + HCl = AgCl↓ + HNO3
2. —оли взаимодействуют в растворах со щелочами:
2NaOH + CuSO4 = Cu(OH)2¯ + Na2SO4
3. –астворы солей реагируют между собой, если образуетс€ осадок:
Ba(NO3)2 + Na2SO4 = BaSO4 ¯ + 2NaNO3
4. —оли взаимодействуют с металлами. Ѕолее активные металлы вытесн€ют менее активные из растворов солей:
CuSO4 + Fe = FeSO4 + Cu
5. Ќекоторые соли разлагаютс€ при нагревании:
—а—ќ3 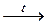 —аќ + —ќ2
—аќ + —ќ2
2AgNO3 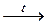 2Ag + 2NO2 + O2
2Ag + 2NO2 + O2
ѕолучение:
1. ¬заимодействие металлов с неметаллами:
2Fe + 3Cl2 = 2FeCl3
2. ¬заимодействие металлов с кислотами:
Fe + 2HCl = FeCl2 + H2
3. ¬заимодействие металлов с растворами солей:
Zn + CuSO4 = ZnSO4 + Cu
4. ¬заимодействие оксидов с кислотами и щелочами:
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
SiO2 + 2NaOH = Na2SiO3 + H2O
5. ¬заимодействие оксидов между собой:
CaO + N2O5 = Ca(NO3)2
6. —оли получают по реакци€м обмена в растворах между сол€ми и кислотами, сол€ми и щелочами, сол€ми и сол€ми, кислотами и основани€ми:
|
|
|
Na2CO3 + 2HCl = CO2 + H2O + 2NaCl
CuCl2 + 2NaOH = Cu(OH)2¯ + 2NaCl
Ba(NO3)2 + K2SO4 = BaSO4¯ + 2KNO3
ислые соли
ѕолучение
1. ¬заимодействие кислоты с недостатком основани€.
KOH + H2SO4 = KHSO4 + H2O
2. ¬заимодействие основани€ с избытком кислотного оксида
Ca(OH)2 + 2CO2 = Ca(HCO3)2
3. ¬заимодействие средней соли с кислотой
Ca3(PO4)2 + 4H3PO4 = 3Ca(H2PO4)2
’имические свойства.
1. “ермическое разложение с образованием средней соли
Ca(HCO3)2 = CaCO3 + CO2 + H2O
2. ¬заимодействие со щЄлочью. ѕолучение средней соли.
Ba(HCO3)2 + Ba(OH)2 = 2BaCO3 + 2H2O
ќсновные соли
ѕолучение






