Одной из основных областей применения координационных соединений является аналитическая химия. Использование координационных соединений в аналитической химии происходило параллельно с развитием теоретических представлений об этом классе соединений. В ряде случаев аналитические реакции были выявлены эмпирически и лишь позднее стало ясно, что они связаны с комплексообразованием. Так многие колориметрические методы количественного определения ионов металлов основаны на образовании ими координационных соединений. Введение хромофорных групп в органические лиганды позволило получать разнообразные реагенты для фотометрического определения ионов. Современные теоретические представления позволяют интерпретировать и предсказывать характер абсорбционных спектров в зависимости от природы центрального атома и лигандов.
Необычайно широко использование координационных соединений в химической технологии. Так криолит Na3[AlF6] используется при электролитическом получении алюминия, в стекольной промышленности и для получения эмалей. Соединение Na2[SiF6] вводят в шихту при варке стекол, что оказывает влияние на вязкость и кристаллизационные свойства стекла. Обогащение поверхностей металлов азотом и углеродом для увеличения их твердости, износостойкости и придания антифрикционных свойств проводят с помощью смеси солей с непременным включением цианидов, в частности K4[Fe(CN)6].
Современные требования к созданию новых материалов и технологий выделения и очистки металлов явились мощным толчком к развитию химии координационных соединений. Лиганды существенно влияют на окислительно-восстановительные потенциалы ионов металлов, на этом свойстве основаны методы электрохимического разделения металлов. Гидрометаллургические технологии получения редких и благородных металлов целиком основаны на процессах комплексообразования, причем некоторые аналитические методики разделения лишь с небольшими изменениями были перенесены в схемы технологических процессов. Например, было известно, что оксиоксимы являются избирательными реагентами на ионы меди, поэтому при разработке ныне действующих процессов выделения меди были использованы реагенты этого класса.
Применение координационных соединений в качестве красителей и пигментов в ряде случаев привело к вытеснению операции протравы. Химическая сущность протравы состоит в закреплении на волокне ионов металлов с последующим их взаимодействием с органическим красителем и образованием координационных соединений. Ион металла играет роль мостика между молекулами волокна и красителя, увеличивая его светостойкость. В красителях наиболее часто используются ионы хрома(III), кобальта(III) и меди(II). Комплексы хрома с азосоединениями типа
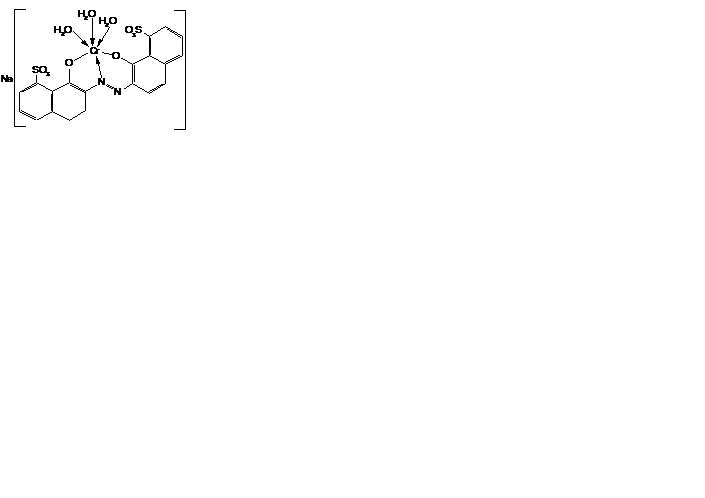
начали использоваться в качестве красителей еще в 1919 году.
В последние десятилетия большое внимание уделяется биологическим аспектам координационной химии. Еще в 1969 году было установлено, что цис-[Pt(NH3)2Cl2] обладает ярко выраженными противоопухолевыми свойствами, тогда как транс-изомер этого комплекса такие свойства не проявляет. Экспериментально доказано, что цис-комплекс платины избирательно подавляет синтез ДНК, но мало влияет на синтез РНК. К настоящему времени испытано более тысячи комплексов платины с разнообразными аминами и ацидолигандами и отобрано около 30 наиболее перспективных соединений.






