Расчет равновесных концентраций после сливания двух растворов
Пример 20. Вычислить концентрацию Cd2+ в растворе, полученном смешением 500 мл 0,4 моль/л CdCl2 и 450 мл 4 моль/л KCN.
Решение. После смешения растворов протекает реакция комплексообразования
Cd2+ + 4CN– = 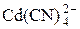
Равновесная концентрация ионов Cd2+ определяется процессом комплексообразования, протекающим в присутствии избытка CN–. Равновесие образования комплекса 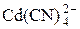 характеризуется константой устойчивости:
характеризуется константой устойчивости:
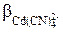 =
= 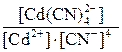 = 1,29 ∙ 1017
= 1,29 ∙ 1017
Рассчитаем концентрации веществ после смешения:
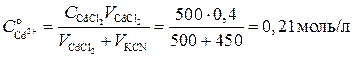
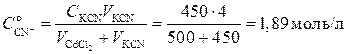
При значительном избытке лиганда и достаточно большой константе устойчивости можно принять, что
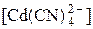 =
= 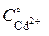 = 0,21 моль/л
= 0,21 моль/л
[CN–] = 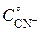 – 4 ∙
– 4 ∙ 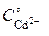 = 1,89 – 4 ∙ 0,21 = 1,05 моль/л
= 1,89 – 4 ∙ 0,21 = 1,05 моль/л
Подставим эти данные в выражение для константы устойчивости, выразим равновесную концентрацию ионов Cd2+ и рассчитаем ее:
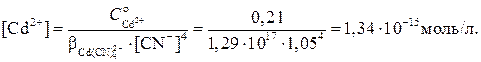
ЛИТЕРАТУРА
1. Лурье Ю.Ю. Справочник по аналитической химии. – М.: Химия, 1989. – 448 с.
2. Аналитическая химия. Справочные материалы: учебно-методическое пособие по дисциплинам «Аналитическая химия» и «Аналитическая химия и физико-химические методы анализа» для студентов химико-технологических специальностей / сост.: А.Е. Соколовский, Е.В. Радион. – Минск: БГТУ, 2005. – 80 с.
3. Радион Е.В., Коваленко Н.А. Основы качественного анализа: тексты лекций по дисциплинам «Аналитическая химия», «Аналитическая химия и физико-химические методы анализа» для студентов химико-технологических специальностей. – Минск: БГТУ, 2012. – 73 с. (электронный ресурс)
4. Радион Е.В. Классические методы анализа: практическое применение: тексты лекций по дисциплинам «Аналитическая химия», «Аналитическая химия и физико-химические методы анализа» для студентов химико-технологических специальностей. – Минск: БГТУ, 2013. – 81 с. (электронный ресурс)
5. Аналитическая химия. Лабораторный практикум: учебно-методическое пособие для студентов химико-технологических специальностей и специальностей 1-57 01 01 «Охрана окружающей среды и рациональное использование природных ресурсов»,
1-57 01 03 «Биоэкология», 1-48 01 05 «Химическая технология переработки древесины» / А.Е. Соколовский [и др.]. – Минск: БГТУ, 2012. – 111 с.
6. Прикладное ПО «Расчет кривых кислотно-основного титрования» (входит в состав электронного учебно-методического комплекса по аналитической химии; установлено в учебных лабораториях кафедры)
7. Компьютерный расчет кривых кислотно-основного титрования: методические рекомендации и индивидуальные задания по дисциплине «Аналитическая химия и физико-химические методы анализа» для студентов химико-технологических специальностей / сост.: Е.В. Радион, А.К. Болвако. – Минск: БГТУ, 2012. – 41 с. (электронный ресурс)
ОГЛАВЛЕНИЕ
| введение.............................................. | |
| 1. Общие вопросы теории растворов.............. Раствор как среда для проведения аналитических реакций..... Основы теории сильных электролитов. Активность, коэффициент активности, ионная сила растворов......... Примеры выполнения расчетов............................ § Расчет ионной силы раствора....................... § Расчет коэффициентов активности................... § Расчет активностей ионов.......................... | |
| 2. Равновесие в системе осадок–раствор........ Растворимость осадков и факторы, влияющие на нее......... Влияние ионной силы на растворимость МРС............... Влияние одноименных ионов на растворимость осадка........ Влияние конкурирующих реакций на растворимость МРС..... Смещение равновесия осаждения-растворения............... Использование реакций осаждения в аналитической химии.... Примеры выполнения расчетов............................ § Расчет значения реальной константы растворимости.... § Расчет растворимости МРС в его насыщенном водном растворе......................................... § Расчет растворимости МРС в присутствии разноименных ионов (солевой эффект)............... § Расчеты с применением критерия практически полного осаждения....................................... § Расчет растворимости МРС в присутствии одноименных ионов........................................... 3. Кислотно-оснóвное равновесие................ Равновесия в водных растворах кислот, оснований и амфолитов. Расчет рН протолитических систем......... Равновесия и расчет рН в растворах кислот (с примерами расчетов)....................................... Равновесия и расчет рН в растворах оснований (с примерами расчетов)........................... Равновесия и расчет рН в растворах амфолитов (с примерами расчетов)............................ Буферные растворы.................................... Механизм буферного действия....................... Использование буферных растворов.................. Расчет рН буферных смесей (с примерами расчетов)...... Буферная емкость.................................. Расчеты при приготовлении буферных растворов (с примерами расчетов)........................... Распределительные диаграммы для кислотно-оснóвных систем. Использование реакций кислотно-оснóвного взаимодействия в аналитической химии............................... Примеры выполнения расчетов............................ § Расчет значения рН после сливания двух растворов.... 4. Окислительно-восстановительное равновесие...................................... Правила записи уравнения Нернста (с примерами записи)..... Факторы, влияющие на величину электродного потенциала.... Направление окислительно-восстановительных реакций...... Изменение направления окислительно-восстановительных реакций............................................ Использование реакций окисления-восстановления в аналитической химии............................... Примеры выполнения расчетов............................ § Расчет константы равновесия ОВР................... § Расчет значения Е после сливания двух растворов...... § Расчет значения Е при протекании конкурирующих реакций осаждения................................ § Расчет значения Е при протекании конкурирующих реакций комплексообразования..................... 5. Комплексообразование......................... Основные понятия...................................... Моно- и полидентатные лиганды. Хелатные комплексы....... Равновесия в растворах комплексных соединений............ Комплексообразование с монодентатными лигандами..... Комплексообразование с полидентатными лигандами..... Использование реакций комплексообразования в аналитической химии............................... Примеры выполнения расчетов............................ § Расчет равновесных концентраций после сливания двух растворов........................................ | |
| Литература............................................. |
Учебное издание
Радион Елена Вадимовна
Соколовский Александр Евгеньевич
ТЕОРЕТИЧЕСКИЕ ОСНОВЫ
АНАЛИТИЧЕСКОЙ ХИМИИ
Учебное пособие
Редактор Т. Е. Самсанович
Компьютерная верстка
Корректор Т. Е. Самсанович
Издатель:
УО «Белорусский государственный технологический университет».
ЛИ № 02330/0549423 от 08.04.2009.
ЛП № 02330/0150477 от 16.01.2009.
Ул. Свердлова, 13а, 220006, г. Минск






