Причины буферного действия заключаются в следующем. Ионы Н+ или ОН–, которые добавляются к буферу, не остаются свободными, а связываются в молекулы слабого электролита.
Проиллюстрируем механизм буферного действия на примере ацетатного буфера, который состоит из CH3COOH и CH3COONa. В растворе ацетатного буфера имеют место равновесия:
CH3COOH ↔ CH3COO– + H+
CH3COONa → CH3COO– + Na+
При добавлении к нему небольшого количества сильной кислоты ионы Н+ связываются с ацетат-ионами в молекулы слабой уксусной кислоты, в результате чего значение рН практически не меняется:
CH3COO– + H+ ↔ CH3COOH
При добавлении небольшого количества щелочи ионы ОН– связываются с ионами H+, образуя молекулы воды, поэтому значение рН тоже практически не меняется:
H+ + ОН– ↔ Н2О
В фосфатном буфере, состоящем из двух солей NaH2PO4 и Na2HPO4, оба компонента диссоциированы на ионы:
NaH2PO4 → Na+ + H2PO4–
Na2HPO4 → 2Na+ + HPO42–
При добавлении Н+ гидрофосфат переходит в дигидрофосфат, связывая поступившие протоны:
HPO42– + H+ ↔ H2PO4–
При добавлении ОН– происходит кислотно-основная реакция с участием дигидрофосфата, в ходе которой ионы ОН– связываются в молекулы Н2О:
H2PO4– + ОН– ↔ HPO42– + Н2О
Использование буферных растворов
Буферные растворы используют во всех случаях проведения химических реакций и технологических процессов, когда требуется поддерживать постоянное значение рН в ходе их проведения.
Ход многих аналитических химических реакций, которые используются для обнаружения и разделения, зависит от рН среды, поэтому для поддержания необходимого значения рН используют буферные растворы. В особенности это касается следующих реакций:
1) С участием анионов слабых кислот или катионов слабых оснований. Например, групповые разделения – осаждение катионов II аналитической группы, III аналитической группы с помощью групповых реактивов – проводятся только в аммиачном буфере [3]. Реакции обнаружения ионов Mg2+ c Na2HPO4, PO43– с Mg2+, Ba2+ с K2Cr2O7 и многие другие также проводятся в среде рН -буферов [3].
2) Цветных качественных реакций с органическими реагентами. Например, при обнаружении ионов Al3+ капельной реакцией с ализарином необходимо, помимо анализируемого раствора и реактива, нанести на полоску фильтровальной бумаги HCl и поместить ее над емкостью с конц. NH4OH (первый компонент аммиачного буфера). При взаимодействии кислоты и слабого основания образуется второй компонент буфера – NH4Cl, и тем самым создаются необходимые условия для протекания цветной реакции [3].
При проведении определения с использованием метода комплексонометрического титрования важнейшим условием также является присутствие буфера в титруемом растворе.
Буферные растворы образуются в ходе кислотно-оснóвного титрования слабых протолитов и их смесей до точки эквивалентности или между двумя точками эквивалентности.
Примеры использования буферов в химической технологии и полиграфии:
§ в офсетной печати используется фосфатный буфер с рН = 6,8;
§ в гальванопроцессах используется борный буфер с рН» 5 и т. д.
В крови человека тоже есть рН -буфер с рН = 7,3–7,5, состоящий из Н2СО3 и НСО3–. Если значение рН крови по каким-либо причинам не укладывается в данный интервал, то это приводит к летальному исходу.
Расчет рН буферных смесей
1. Буферный раствор на основе слабой
кислоты и ее соли
Рассмотрим расчет значения рН на примере цианидного буфера, состоящего из HCN и NaCN. В растворе оба компонента диссоциируют, причем соль полностью:
NaCN → Na+ + CN–,
а кислота – обратимо:
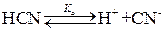
Запишем выражение для константы равновесия:
 Þ
Þ
 (3.14)
(3.14)
Поскольку степень диссоциации (α) слабой кислоты мала, то можно сделать допущение, что равновесная концентрация недиссоциированной кислоты равна ее общей концентрации в растворе:
[HCN]» C кисл.
Кроме того, равновесную концентрацию цианид-ионов можно принять практически равной общей концентрации соли
[CN–]» C соли,
поскольку NaCN, как сильный электролит, диссоциирует полностью. При этом диссоциация слабой кислоты подавляется за счет поступления ионов CN– из соли.
Подставим эти выражения в формулу (3.14) и получим:
 Þ
Þ
 (3.15)
(3.15)
Используя эту расчетную формулу, можно объяснить также свойства буферных растворов:
§ «Значение рН буферного раствора не меняется при разбавлении». Как видно из формулы (3.15), если раствор разбавить в n раз, то концентрация обоих компонентов буфера тоже уменьшится в n раз, однако отношение концентраций останется постоянным Þ значение рН не изменится. Однако, при очень сильном разбавлении (³ 104 раз) значение рН меняется на 0,5–1,0 ед. рН.
§ «Значение рН буферного раствора мало меняется при добавлении небольших количеств Н+ или ОН–». При добавлении небольшого количества Н+ концентрация слабой кислоты несколько увеличивается, а концентрация соли – уменьшается. При этом отношение концентраций компонентов буфера немного меняется, но логарифм этого отношения меняется очень незначительно Þ значение рН практически не изменяется. Если же добавить к буферу небольшое количество ОН–, то концентрация слабой кислоты несколько уменьшится, а концентрация соли – увеличивается, но логарифм этого отношения меняется очень незначительно Þ значение рН также практически не изменяется.
2. Буферный раствор на основе слабого
основания и его соли
Рассмотрим расчет значения рН на примере аммиачного буфера, состоящего из NH4OH и NH4Cl. В растворе оба компонента диссоциируют, причем соль полностью:
NH4Cl → NH4+ + Cl–
а основание – обратимо:

Запишем выражение для константы равновесия:
 Þ
Þ
 (3.16)
(3.16)
Поскольку степень диссоциации (α) слабого основания мала, то можно сделать допущение, что равновесная концентрация недиссоциированного основания равна его общей концентрации в растворе:
[NH4OH]» C осн.
Кроме того, равновесную концентрацию ионов NH4+ можно принять практически равной общей концентрации соли
[NH4+]» C соли,
поскольку NH4Cl, как сильный электролит, диссоциирует полностью. При этом диссоциация слабого основания подавляется за счет поступления ионов NH4+ из соли.
Подставим эти выражения в формулу (3.16) и получим:
 Þ
Þ
 Þ
Þ
 (3.17)
(3.17)
3. Буферный раствор на основе двух солей многоосновной кислоты
Рассмотрим расчет значения рН на примере фосфатного буфера, состоящего из NaH2PO4 и Na2HPO4. В этой системе дигидрофосфат натрия NaH2PO4, имеющий больше ионов H+, выступает в роли кислоты по отношению к своей соли – гидрофосфату натрия Na2HPO4 (меньше ионов H+).
Следовательно, для расчета значения рН необходимо воспользоваться формулой (3.15). Для выяснения вопроса, какое значение pKa фосфорной кислоты надо подставить в формулу, запишем равновесие между компонентами буфера:

Следовательно, необходимо подставить pKa,2. Тогда расчетная формула примет вид:
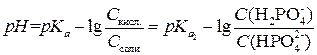
Буферная емкость
Способность буферных растворов поддерживать значение рН постоянным не безгранична. Любой буферный раствор обладает определенной буферной емкостью.
Буферная емкость – это такое количество моль эквивалентов сильной кислоты или сильного основания, которое нужно добавить к 1 л буферной раствора, чтобы изменить его значение рН на 1 ед.:

где 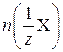 – количество моль экв. кислоты или щелочи; Δ рН – изменение рН после добавления кислоты или щелочи; V – объем буферного раствора, л.
– количество моль экв. кислоты или щелочи; Δ рН – изменение рН после добавления кислоты или щелочи; V – объем буферного раствора, л.
Чем больше буферная емкость, тем лучше буфер удерживает постоянным значение рН.
Факторы, влияющие на буферную емкость:
§ суммарная концентрация компонентов смеси: чем она больше, тем больше буферная емкость;
§ соотношение концентраций компонентов буфера: чем ближе к 1 значение
 ,
,
тем больше буферная емкость, поэтому максимальная буферная емкость достигается при одинаковых концентрациях компонентов:
С кисл. = С соли или С осн. = Ссоли
В этих случаях, согласно формулам (3.15) и (3.17) значения рН буферных растворов равны:
pH = pKa или pH = 14 – pKb
На практике обычно готовят буферы со значениями рН
pH = pKa ± 1 или pH = (14 – pKb) ± 1
Для этого задают отношения концентраций компонентов буферной смеси

в интервале от 10: 1 до 1: 10. Рецептуры для приготовления буферных растворов с различными значениями рН приводятся в справочнике [1]. Методики определения буферной емкости изложены в [5].






