Рассмотрим расчет значений объемов исходных растворов, необходимых для приготовления заданного объема буферного раствора с заданным значением рН, на примере лабораторной работы № 12 [5].
Вариант 1. Приготовление ацетатного
буферного раствора
Алгоритм действий:
1. Рассчитать отношение концентраций компонентов ацетатного буфера, зная необходимое значение рН буферного раствора и табличное значение pKа уксусной кислоты. В результате получим численное значение:
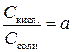
2. В буферном растворе отношение концентраций компонентов всегда равно отношению количества молей компонентов, поскольку они находятся в одном и том же объеме раствора:

3. При сливании растворов уксусной кислоты и гидроксида натрия протекает реакция:

Для того, чтобы получился буфер, состоящий из СН3СООН и СН3СООNa, кислоту надо взять в избытке по отношению к щелочи Þ при одинаковых концентрациях исходных растворов (0,1 моль/л) всегда V кисл > V щел.
4. Рассчитаем, сколько моль эквивалентов СН3СООН и NaOH надо взять:


5. После протекания реакции в растворе останется непрореагировавшей уксусной кислоты:
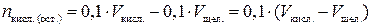 ,
,
а соли образуется столько же моль эквивалентов, сколько было взято щелочи, т. е.

Следовательно,

6. Для окончательного расчета составим систему из двух уравнений с двумя неизвестными объемами. Для удобства записи введем обозначения:
V кисл, мл = x
V щел, мл = y
Учтем, что согласно методике проведения лабораторной работы
x + y =50 мл (или x + y = 100 мл)
Тогда получим:

В результате решения системы уравнений получаем два искомых объема исходных растворов уксусной кислоты и гидроксида натрия.
Вариант 2. Приготовление аммиачного
буферного раствора
Алгоритм действий:
1. Рассчитать отношение концентраций компонентов аммиачного буфера, зная необходимое значение рН буферного раствора и табличное значение pKb аммиака. В результате получим численное значение:

2. В буферном растворе отношение концентраций компонентов всегда равно отношению количества молей компонентов, поскольку они находятся в одном и том же объеме раствора:

3. При сливании растворов гидроксида аммония и соляной кислоты протекает реакция:

Для того чтобы получился буфер, состоящий из NН4ОН и NН4Сl, основание надо взять в избытке по отношению к кислоте Þ при одинаковых концентрациях исходных растворов (0,2 моль/л) всегда
V осн. > V кисл..
4. Рассчитаем, сколько моль эквивалентов NН4ОН и HCl надо взять:


5. После протекания реакции в растворе останется непрореагировавшего NН4ОН:
 ,
,
а соли образуется столько же моль эквивалентов, сколько было взято кислоты, т. е.

Следовательно,

6. Для окончательного расчета составим систему из двух уравнений с двумя неизвестными объемами. Для удобства записи введем обозначения:
V осн., мл = x
V кисл., мл = y
Учтем, что согласно методике проведения лабораторной работы
x + y =50 мл (или x + y = 100 мл)
Тогда получим:

В результате решения системы уравнений получаем два искомых объема исходных растворов гидроксида аммония и соляной кислоты.






