1. Раствор сильной кислоты
В растворе сильной кислоты равновесие диссоциации полностью смещено вправо:
HA + H2O ® H3O+ + A–
При Скисл > 10–6 М автопротолизом воды можно пренебречь. Тогда равновесная концентрация ионов гидроксония будет равна общей концентрации одноосновной кислоты:
[H3O+] = С кисл. Þ
рН = – lg[H3O+] = – lg С кисл (3.3)
Если Скисл ≤ 10–6 М, то надо учесть автопротолиз воды, за счет которого в растворе тоже появляются ионы гидроксония. В этом случае расчет равновесной концентрации ионов гидроксония проводят по формуле:
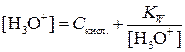 (3.4)
(3.4)
Необходимость учета автопротолиза воды можно продемонстрировать на следующем примере. Рассчитаем значение рН в растворе хлороводородной кислоты при С (HCl) = 10–8 моль/л по формуле (3.3), которая используется в теории Аррениуса независимо от концентрации кислоты:
рН = – lg10–8 = 8
Ответ является абсурдным (щелочная среда в растворе кислоты!).
Если провести расчет по теории Бренстеда-Лоури, т. е. учесть автопротолиз растворителя-амфолита H2O, то по формуле (3.4) получим ответ
рН = 6,98
2. Раствор слабой кислоты
В растворе слабой кислоты происходит неполная диссоциация:
HA + H2O «H3O+ + A–
Равновесие характеризуется константой ионизации:
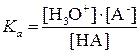
Если выполняются условия:
С кисл. > 10–4 М
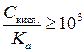
α < 5 %,
то можно пользоваться приближенными формулами для расчета рН, сделав допущение, что при указанных условиях равновесная концентрация недиссоциированной кислоты примерно равна ее общей концентрации в растворе:
[HА] ≈ С кисл.
Из уравнения реакции видно, что
[H3O+] = [A–] Þ
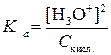
Отсюда выражаем равновесную концентрацию ионов гидроксония в растворе слабой кислоты:
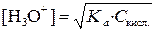
После логарифмирования с обратным знаком получаем:
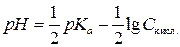 (3.5)
(3.5)
Если степень диссоциации кислоты α > 5 %, то расчетная формула получается более громоздкой:
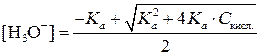 (3.6)
(3.6)
3. Раствор катионной слабой кислоты
Согласно протолитической теории, катионы слабых оснований являются катионными слабыми кислотами. Рассмотрим расчет значения рН на примере водного раствора хлорида аммония NH4Cl. Эта соль в растворе полностью диссоциирует:
NH4Cl ® NH4+ + Cl–
Ион аммония вступает в протолитическую реакцию с растворителем-амфолитом водой:
NH4+ + H2O «NH3 + H3O+
В этой реакции аммиак NH3 является молекулярным основанием, а ион NH4+ – сопряженной катионной кислотой. Следовательно, для расчета рН в растворе NH4Cl выбираем формулу (3.5). В нее входит величина рKa, в нашем случае рKa (NH4+), которой в таблицах нет. Для ее расчета используем табличное значение рKb (NH3) и формулу (3.2):
рKa (NH4+) = 14 – рKb (NH3)
Подставив это выражение в формулу (3.5), получим
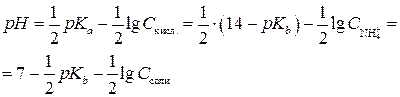 (3.7)
(3.7)
Пример расчета
Задание: рассчитать рН в 0,01 М растворе хлорида метиламмония.
Решение: хлорид метиламмония – это соль слабого основания метиламина CH3NH2. В водном растворе метиламина образуется гидроксид метиламмония:
CH3NH2 + H2O «CH3NH3ОН (рKb = 3,34)
Хлорид метиламмония имеет формулу CH3NH3+Cl–, его катион CH3NH3+ является катионной слабой кислотой, сопряженной с основанием CH3NH3ОН.
Рассчитаем рН в 0,01 М растворе хлорида метиламмония по формуле (3.7), подставив имеющиеся данные:
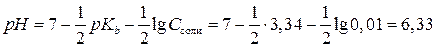
4. Раствор многоосновной кислоты
В растворе многоосновной кислоты происходит ступенчатая диссоциация, например, в растворе фосфорной кислоты:
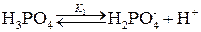

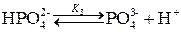
В результате образуется сложная многокомпонентная система, и расчет рН сильно усложняется. Так, даже для двухосновной кислоты получается уравнение третьей степени. Поэтому полагают, то при выполнении условия
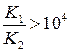 или в логарифмическом виде pK 2 – pK 1 > 4
или в логарифмическом виде pK 2 – pK 1 > 4
диссоциация кислоты по второй и третьей ступени подавляется, и рассчитывают значение рН как в растворе слабой одноосновной кислоты, используя формулы (3.5) или (3.6).






