Пример 10. Вычислить значение рН раствора, полученного при сливании 20,0 мл 0,1 М раствора NaOH и 16,0 мл 0,08 М раствора HCl.
Решение. Запишем уравнение реакции, которая протекает после сливания двух растворов:
NaOH + HCl = NaCl + H2O
С целью выяснения состава раствора, образовавшегося после сливания, рассчитаем количества веществ в исходных растворах:
n 0(NaOH) = 20,0 ∙ 10–3 ∙ 0,1 = 2,0 ∙ 10–3 моль;
n 0(HCl) = 16,0 ∙ 10–3 ∙ 0,08 = 1,28 ∙ 10–3 моль.
Так как n 0(NaOH) > n 0(HCl), то NaOH находится в избытке, следовательно, в образовавшемся после сливания растворе будут находиться NaOH и NaCl в следующих количествах:
n 1(NaOH) = n 0(NaOH) – n 0(HCl) = 2,0 ∙ 10–3 – 1,28 ∙ 10–3 =
= 0,72 ∙ 10–3 моль.
n 1(NaCl) = n 0(HCl) = 1,28 ∙ 10–3 моль.
NaCl является солью сильной кислоты и сильного основания и на pH не влияет.
Объем раствора после сливания (V) составит 20,0 + 16,0 = 36,0 мл.
Рассчитаем концентрацию NaOH в растворе:
С (NaOH) = 0,72 ∙ 10–3/ 36 ∙ 10–3 = 0,02 моль/л.
Исходя из состава раствора, выбираем формулу (3.8) для расчета рН в растворе сильного основания:
pH = 14 + lg C (NaOH) = 14 + lg(0,02) = 12,3
Пример 11. Вычислить значение рН раствора, полученного при сливании 20,0 мл 0,1 М раствора NaOH и 36,0 мл 0,08 М раствора HCl.
Решение. Запишем уравнение реакции, которая протекает после сливания двух растворов:
NaOH + HCl = NaCl + H2O
С целью выяснения состава раствора, образовавшегося после сливания, рассчитаем количества веществ в исходных растворах:
n 0(NaOH) = 20,0 ∙ 10–3 ∙ 0,1 = 2,0 ∙ 10–3 моль;
n 0(HCl) = 36,0 ∙ 10–3 ∙ 0,08 = 2,88 ∙ 10–3 моль.
Так как n 0(NaOH) < n 0(HCl), то HCl находится в избытке, следовательно, в образовавшемся после сливания растворе будут присутствовать HCl и NaCl в следующих количествах:
n 1(HCl) = n 0(HCl) – n 0(NaOH) = 2,88 ∙ 10–3 – 2,0 ∙ 10–3 =
= 0,88 ∙ 10–3 моль
n 1(NaCl) = n 0(NaOH) = 2,0 ∙ 10–3 моль
NaCl является солью сильной кислоты и сильного основания и на pH не влияет.
Объем раствора (V) составит 20,0 + 36,0 = 56,0 мл.
Рассчитаем концентрацию HCl в растворе:
С (HCl) = 0,88 ∙ 10–3/ 56 ∙ 10–3 = 0,0157 моль/л.
Исходя из состава раствора, выбираем формулу (3.3) для расчета рН в растворе сильной кислоты:
pH = lg C (HCl) = lg(0,0157) = 1,8.
Пример 12. Вычислить значение рН раствора, полученного при сливании 20,0 мл 0,12 М раствора NaCN и 15,0 мл 0,09 М раствора HCl.
Решение. Запишем уравнение реакции, которая протекает после сливания двух растворов:
NaCN + HCl = HCN + NaCl
С целью выяснения состава раствора, образовавшегося после сливания, рассчитаем количества веществ в исходных растворах:
n 0(NaCN) = 20,0 ∙ 10–3 ∙ 0,12 = 2,4 ∙ 10–3 моль;
n 0(HCl) = 15,0 ∙ 10–3 ∙ 0,09 = 1,35 ∙ 10–3 моль.
Так как n 0(NaCN) > n 0(HCl), то NaCN находится в избытке, следовательно, в образовавшемся после сливания растворе будут присутствовать NaCN и HCN в следующих количествах:
n 1(NaCN) = n 0(NaCN) – n 0(HCl) = 2,4 ∙ 10–3 – 1,35 ∙ 10–3 =
= 1,05 ∙ 10–3 моль;
n 1(HCN) = n 0(HCl) = 1,35 ∙ 10–3 моль.
Объем раствора после сливания (V) составит 20 + 15 = 35 мл.
Рассчитаем концентрации веществ в растворе:
С (NaCN) = 1,05 ∙ 10–3/ 35 ∙ 10–3 = 0,03 моль/л;
С (HCN) = 1,35 ∙ 10–3/ 35 ∙ 10–3 = 0,039 моль/л.
Исходя из состава раствора, выбираем формулу (3.15) для расчета рН буферных растворов:
pH =  – lg[ С (HCN) / С (NaCN)] = 9,3 – lg(0,039 / 0,03) = 9,18
– lg[ С (HCN) / С (NaCN)] = 9,3 – lg(0,039 / 0,03) = 9,18
Пример 13. Вычислить значение рН раствора, полученного при сливании 11,25 мл 0,12 моль/л раствора NaCN и 15,0 мл 0,09 моль/л раствора HCl.
Решение. Запишем уравнение реакции, которая протекает после сливания двух растворов, и рассчитаем количества веществ:
NaCN + HCl = HCN + NaCl
n (NaCN) = 11,25 ∙ 10–3 ∙ 0,12 = 1,35 ∙ 10–3 моль;
n (HCl) = 15,0 ∙ 10–3 ∙ 0,09 = 1,35 ∙ 10–3 моль.
Так как n (NaCN) = n (HCl), то в образовавшемся после сливания растворе будет находиться только 1,35 ∙ 10–3 моль HCN.
Объем раствора (V) составит 11,25 + 15,0 = 26,25 мл.
Рассчитаем концентрацию HCN в растворе:
С (HCN) = 1,35 ∙ 10–3/ 26,25 ∙ 10–3 = 0,051 моль/л.
Исходя из состава раствора, выбираем формулу (3.5) для расчета рН в растворе слабой кислоты:
pH = 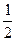
 –
– 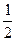 lg[ С (HCN)] =
lg[ С (HCN)] = 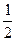 ∙ 9,3 –
∙ 9,3 – 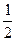 ∙ lg(0,051) = 5,3
∙ lg(0,051) = 5,3
Пример 14. Вычислить значение рН раствора, полученного при сливании 20,0 мл 0,12 моль/л раствора NaCN и 35,0 мл 0,09 моль/л раствора HCl.
Решение. Запишем уравнение реакции, которая протекает после сливания двух растворов, и рассчитаем количества веществ:
NaCN + HCl = HCN + NaCl
n 0(NaCN) = 20,0 ∙ 10–3∙ 0,12 = 2,4 ∙ 10–3 моль;
n 0(HCl) = 35,0 ∙ 10–3 ∙ 0,09 = 3,15 ∙ 10–3 моль.
Так как n 0(HCl) > n 0(NaCN), то в образовавшемся после сливания растворе будут находиться HCl и HCN в следующих количествах:
n 1(HCl) = 3,15 ∙ 10–3 – 2,4 ∙ 10–3 = 0,75 ∙ 10–3 моль;
n 1(HCN) = 20,0 ∙ 10–3 ∙ 0,12 = 2,4 ∙ 10–3 моль.
Поскольку сильная кислота HCl подавляет диссоциацию слабой кислоты HCN, то рН определяется только ее концентрацией.
Объем раствора (V) составит 20,0 + 35,0 = 55,0 мл.
Рассчитаем концентрацию HCl в растворе:
С (HCl) = 0,75 ∙ 10–3/ 55,0 ∙ 10–3 = 0,014 моль/л.
Исходя из состава раствора, выбираем формулу (3.3) для расчета рН в растворе сильной кислоты:
pH = – lg[С(HCl)] = – lg(0,014) = 1,87.
Пример 15. Вычислить значение рН раствора, полученного при сливании 10,0 мл 0,1 моль/л раствора Na2HAsO4 и 16,0 мл 0,1 моль/л раствора HCl.
Решение. После сливания растворов могут протекать следующие реакции:
Na2HAsO4 + HCl = NaH2AsO4 + NaCl (3.16)
NaH2AsO4 + HCl = H3AsO4 + NaCl (3.17)
Рассчитаем количества вещества в исходных растворах:
n (Na2HAsO4) = 10,0 ∙ 10–3 ∙ 0,1 = 1,0 ∙ 10–3 моль;
n (HCl) = 16,0 ∙ 10–3 ∙ 0,1 = 1,6 ∙ 10–3 моль.
Так как Na2HAsO4 взят в недостатке, то все количество его прореагирует с HCl согласно уравнению (3.16), и после протекания реакции (3.16) в растворе останется 1,0 ∙ 10–3 моль NaH2AsO4 и
(1,6 – 1,0) ∙ 10–3 = 0,6 ∙ 10–3 моль HCl. Аналогично после завершения реакции (3.17) в растворе будут находиться H3AsO4 и NaH2AsO4 в следующих количествах:
n (NaH2AsO4) = 1,0 ∙ 10–3 – 0,6 ∙ 10–3 = 0,4 ∙ 10–3 моль;
n (H3AsO4) = 0,6 ∙ 10–3 моль.
Объем раствора (V) после смешения составит 10 + 16 = 26 мл, или 26 ∙ 10–3 л.
Рассчитаем концентрации компонентов в растворе:
С (NaH2AsO4) = 0,4 ∙ 10–3/ 26 ∙ 10–3 = 0,015 моль/л;
С (H3AsO4) = 0,6 ∙ 10–3/ 26 ∙ 10–3 = 0,023 моль/л.
Исходя из состава раствора, выбираем формулу (3.15) для расчета рН буферных растворов:
pH = 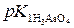 – lg(С (H3AsO4) / С (NaH2AsO4)) =
– lg(С (H3AsO4) / С (NaH2AsO4)) =
= 2,22 – lg(0,023/0,015) = 2,03.






