Пример 6. Вычислить растворимость (моль/л, г/л) оксалата кальция СаС2О4 в его насыщенном водном растворе, массовую концентрацию ионов Са2+ и массу кальция в 100 мл этого раствора.
Решение. Химическое равновесие в насыщенном растворе СаС2О4 описывается уравнением:
СаС2О4↓ D Са2+ + 
Запишем выражение для константы растворимости. Поскольку ионная сила I ® 0, то можно использовать концентрации, а не активности:
 = [Са2+] · [
= [Са2+] · [  ]
]
Находим в справочнике [1; 2, табл. 6] значение константы, равное 2,57 ∙ 10–9.
Обозначим растворимость СаС2О4 через х моль/л. При диссоциации х молей СаС2О4 образуется х молей Са2+ и x молей  . Подставляя эти значения в выражение для константы растворимости, получим:
. Подставляя эти значения в выражение для константы растворимости, получим:
 = [Са2+] · [
= [Са2+] · [  ] = х ∙ х = 2,57 ∙ 10–9
] = х ∙ х = 2,57 ∙ 10–9
Отсюда
x 2 = 2,57 ∙ 10–9
x =  = 5,1 ∙ 10–5 моль/л.
= 5,1 ∙ 10–5 моль/л.
Таким образом, растворимость СаС2О4 в его насыщенном водном растворе составляет 5,1 ∙ 10–5 моль/л.
Для перехода к другим единицам измерения (г/л) необходимо молярную растворимость (моль/л) умножить на молярную массу СаС2О4 (г/моль):

Молярная концентрация ионов Са2+ в насыщенном водном растворе соли СаС2О4 такая же, как молярная концентрация соли:
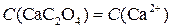
Следовательно массовая концентрация ионов Са2+ равна:

Найдем массу кальция в 100 мл насыщенного раствора соли СаС2О4:
 Иначе:
Иначе:
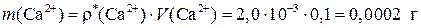
или из пропорции:
в 1000 мл раствора – 2,0 ∙ 10–3 г кальция;
в 100 мл раствора – x г кальция;
x = 2,0 ∙ 10–3 ∙100 /1000 = 0,0002 г.
Расчет растворимости МРС в присутствии разноименных ионов (солевой эффект)
Алгоритм решения задач:
1) Рассчитать ионную силу раствора I, которую создает посторонний сильный электролит (разноименные ионы).
2) Для данной ионной силы взять в справочнике [1; 2, табл. 1, 2] или рассчитать по формулам (1.4), (1.5), (1.6) коэффициенты активности ионов, входящих в состав осадка.
3) Записать равновесие, которое устанавливается в насыщенном растворе МРС, и выражение для термодинамической константы растворимости этого соединения. Взять в справочнике [1; 2, табл. 6] численное значение константы.
4) Выразить растворимость МРС из выражения для термодинамической константы растворимости и провести расчет.
Пример 7. Вычислить растворимость хлорида серебра в 0,01 М растворе Ca(NO3)2.
Решение. Рассчитаем ионную силу в 0,1 моль/л растворе Ca(NO3)2, как описано в примере 1:
I = 0,03 моль/л.
Далее найдем коэффициенты активности ионов Ag+ и Cl–. Поскольку в таблицах [1; 2, табл. 1, 2] отсутствует значение ионной силы 0,03 моль/л, то рассчитаем коэффициент активности однозарядного иона Ag+ по расширенному уравнению Дебая–Хюккеля (1.5), которое применяется при ионной силе 0,01 < I < 0,1 моль/л:

По закону ионной силы Льюиса-Рендалла коэффициент активности иона Cl– будет равен коэффициенту активности иона Ag+, поскольку оба иона имеют одинаковый заряд:

Запишем равновесие, которое устанавливается в насыщенном растворе AgCl, и выражение для термодинамической константы растворимости AgCl:
AgCl↓ D Ag+ + Cl–

Обозначим концентрацию растворенной части хлорида серебра через x моль/л и возьмем из справочника [1; 2, табл. 6] значение константы растворимости AgCl:

Следовательно, искомая растворимость AgCl:

Пример 8. Вычислить растворимость арсената бария Ba3(AsO4)2 в 0,05 М растворе KNO3.
Решение.
1. Рассчитаем ионную силу в 0,05 М растворе KNO3:
KNO3 ® K+ + NO3– Þ
С (K+) = C (KNO3) = 0,05 моль/л (α = 1 и n = 1)
C ( ) = C (KNO3) = 0,05 моль/л (α = 1 и n = 1)
) = C (KNO3) = 0,05 моль/л (α = 1 и n = 1)

 · (0,05 ∙ 12 + 0,05 ∙ 12) = 0,05 моль/л.
· (0,05 ∙ 12 + 0,05 ∙ 12) = 0,05 моль/л.
2. Возьмем в таблице [1; 2, табл. 2] коэффициенты активности ионов Ba2+ и AsO43– при I = 0,05 моль/л:


3. Запишем равновесие, которое устанавливается в насыщенном растворе Ba3(AsO4)2, и выражение для термодинамической константы растворимости Ba3(AsO4)2. Возьмем в таблице [1; 2, табл. 6] численное значение термодинамической константы растворимости Ba3(AsO4)2, равное 7,8 · 10–51:
Ba3(AsO4)2↓ D 3Ba2+ + 2AsO43–

Обозначим концентрацию растворенной части Ba3(AsO4)2 через x моль/л. Тогда:
[Ba2+] = 3 x моль/л
[AsO43–] = 2 x моль/л
Подставим эти значения в выражение для термодинамической константы растворимости Ba3(AsO4)2:

Проведем необходимые вычисления, выразим и рассчитаем x:
0,125 · 0,0441 · 27 x 3 · 4 x 2 = 7,8 · 10–51 Þ
x 5 = 1,31 · 10–50 Þ
 1,1 · 10–10 моль/л
1,1 · 10–10 моль/л
Таким образом, молярная растворимость арсената бария Ba3(AsO4)2 в 0,05 М растворе KNO3 равна 1,1 · 10–10 моль/л.






