Ионы сильных электролитов в растворе взаимодействуют между собой за счет электростатических сил притяжения или отталкивания (межионные взаимодействия). При концентрации электролита ниже чем 10–4 моль/л эти взаимодействия пренебрежимо малы. Чем выше концентрация электролита, тем сильнее проявляются межионные взаимодействия.
При высоких концентрациях может происходить ассоциация ионов, в результате чего концентрация иона становится меньше, чем следует из формулы:
С иона < С о∙α· n (для сильных электролитов α = 1) (1.1)
В этих случаях вместо понятия «концентрация» используют понятие «активность».
Активность иона (a, моль/л) – это эффективная (кажущаяся) концентрация его, согласно которой он действует в химических реакциях.
Например, в растворе хлороводородной кислоты HCl с концентрацией 0,1 моль/л:
С (Н+) = 0,1 моль/л
а (Н+) = 0,083 моль/л
за счет того, что произошла ассоциация ионов, в результате часть ионов Н+ находится в составе ионных пар с ионами Cl–.
Отношение активности иона к его концентрации называется коэффициентом активности (γ или f):
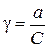 (1.2)
(1.2)
Коэффициент активности – это мера электростатических взаимодействий в растворе. Чем сильнее межионные взаимодействия, тем меньше значение γ.
Величина коэффициента активности зависит от концентрации электролита:
| Раствор | Концентрация | Коэффициент активности | Активность |
| очень разбавленный | С ® 0 | γ = 1 | а = С |
| разбавленный | С < 0,1 М | γ < 1 | а < С |
| концентрированный* | С > 1 М | γ > 1 | а > С |
* – в курсе аналитической химии этот случай не рассматривается
Значение γ для любого иона можно взять из справочника или рассчитать с помощью эмпирических уравнений. В обоих случаях необходимо знать две величины:
§ z – заряд иона, для которого ведут расчет;
§ I (μ), моль/л – ионную силу раствора.
Ионная сила – это величина, которая учитывает электростатическое влияние всех ионов в растворе. Она рассчитывается по формуле:
 (1.3)
(1.3)
где Ci и zi – концентрации и заряды всех ионов в растворе.
Эмпирические уравнения для расчета коэффициентов активности:
1. Предельный закон Дебая–Хюккеля:
 (применяется при I ≤ 0,01 моль/л) (1.4)
(применяется при I ≤ 0,01 моль/л) (1.4)
2. Расширенное уравнение Дебая–Хюккеля:
 (применяется при 0,01 < I < 0,1 моль/л) (1.5)
(применяется при 0,01 < I < 0,1 моль/л) (1.5)
3. Уравнение Дэвиса:
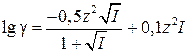 (при 0,1 < I < 0,5 моль/л) (1.6)
(при 0,1 < I < 0,5 моль/л) (1.6)
Как следует из приведенных уравнений, величина γ зависит от заряда иона z и ионной силы раствора I.
Впервые зависимость γ от I была найдена в 1921 г. американскими учеными Льюисом и Рéндаллом, которые сформулировали закон, названный в их честь законом ионной силы Льюиса и Рéндалла:
В достаточно разбавленных растворах с одинаковой ионной силой коэффициенты активности большинства одинаково заряженных ионов приблизительно одинаковы.
Следовательно, не надо считать отдельно, к примеру, коэффициенты активности ионов Zn2+ и SO42–, если они находятся в одном и том же растворе, поскольку эти величины будут практически одинаковы.
Таким образом, если концентрация сильного электролита в растворе превышает 10–4 моль/л, то при проведении точных расчетов необходимо вместо концентраций ионов использовать значения активностей, учитывающих электростатические взаимодействия между ионами. Как следует из формулы (1.2), активности ионов пропорциональны концентрациям:
а = γ · С (1.7)






