Расчет ионной силы раствора
Пример 1. Рассчитать ионную силу 0,1 моль/л раствора Ca(NO3)2.
Решение. Запишем уравнение диссоциации нитрата кальция:
Ca(NO3)2 ® Ca2+ + 2 
Найдем концентрации обоих ионов по формуле (1.1):
С (Ca2+) = C (Ca(NO3)2) = 0,1 моль/л (α = 1 и n = 1)
C ( ) = 2 · C (Ca(NO3)2) = 2 · 0,1 = 0,2 моль/л
) = 2 · C (Ca(NO3)2) = 2 · 0,1 = 0,2 моль/л
Рассчитаем ионную силу, создаваемую ионами кальция и нитрата, по формуле (1.3):
 =
=  · (0,01 ∙ 22 + 0,02 ∙ 12) = 0,03 моль/л.
· (0,01 ∙ 22 + 0,02 ∙ 12) = 0,03 моль/л.
Пример 2. Рассчитать ионную силу в растворе, содержащем 0,01 моль экв/л Al(NO3)3 и 0,01 моль экв/л BaCl2.
Решение. Запишем уравнения диссоциации солей:
Al(NO3)3 ® Al3+ + 3 
BaCl2 ® Ba2+ + 2Cl–
Перейдем от молярных концентраций эквивалента солей к молярным концентрациям:

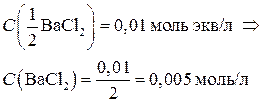
Найдем молярные концентрации всех ионов по формуле (1.1):
С (Al3+) = C (Al(NO3)3) = 0,003333 моль/л
C ( ) = 3 · C (Al(NO3)3) = 3 · 0,003333 = 0,01 моль/л
) = 3 · C (Al(NO3)3) = 3 · 0,003333 = 0,01 моль/л
С (Ba2+) = C (BaCl2) = 0,005 моль/л
C (Cl–) = 2 · C (BaCl2) = 2 · 0,005 = 0,01 моль/л
Рассчитаем ионную силу, которую создают все ионы в растворе, по формуле (1.3):

Расчет коэффициентов активности
Пример 3. Рассчитать коэффициенты активности каждого из ионов в растворе, указанном в примере 2.
Решение. Для расчета коэффициентов активности ионов необходимо знать ионную силу раствора, поэтому сначала выполним все необходимые действия, как описано в примере 2:
§ запишем уравнения диссоциации солей;
§ перейдем от молярных концентраций эквивалента солей к молярным концентрациям;
§ найдем молярные концентрации всех ионов и рассчитаем ионную силу раствора: I = 0,035 моль/л.
Обращаемся к справочнику [1 или 2] и выясняем, что такого значения ионной силы в нем нет. Следовательно, придется рассчитывать коэффициенты активности по эмпирическим уравнениям. Выбираем необходимое уравнение. Поскольку 0,01 < 0,035 < 0,1 моль/л, то надо применить расширенное уравнение Дебая–Хюккеля (1.5).
Воспользуемся им поочередно для каждого из ионов:



Рассчитывать коэффициент активности для хлорид-иона нет смысла, т. к. по закону ионной силы Льюиса-Рендалла он будет равен коэффициенту активности нитрат-иона, поскольку оба иона имеют одинаковый заряд:

Расчет активностей ионов
Пример 4. Рассчитать активность каждого из ионов в растворе, указанном в примере 2.
Решение. Для расчета активности ионов необходимо:
§ рассчитать ионную силу раствора (см. пример 2);
§ для данной ионной силы рассчитать или взять в справочнике коэффициенты активности ионов (см. пример 3);
§ воспользоваться формулой (1.7).
Активность иона алюминия в растворе, содержащем 0,01 моль экв/л Al(NO3)3 и 0,01 моль экв/л BaCl2, равна:
 .
.
Аналогично рассчитаем активности остальных ионов:


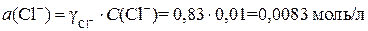
Как видно, для всех ионов величина активности меньше концентрации, что объясняется электростатическими взаимодействиями между ионами в растворе.






