Приклад 1. Які системи називаються розчинами? З яких компонентів вони складаються? (Див. додаток Д).
Відповідь:
Розчин – це гомогенна система з молекул, йонів чи інших частинок, складена двома і більше компонентами, кількісні співвідношення яких можуть змінюватись в широких межах.
Однією з головних умов, коли дану систему називають розчином є її стійкість, тобто неможливість розділення на складові компоненти при довгому стоянні. Іншою ознакою розчинів є можливість змінювати в широких межах їх хімічний склад не змінюючи агрегатного стану. Існують газові, рідкі і тверді розчини.
Розчини займають проміжне положення між механічними сумішами частинок і індивідуальними хімічними сполуками. Від сумішей розчини відрізняються тим, що будь-який мікроскопічний об’єм розчину має такий же склад, як і вся маса розчину. На відміну від хімічних сполук розчини мають змінний склад і не підлягають закону кратних відношень.
Розчини складаються із компонентів. Один з них називається розчинником, інший - розчиненою речовиною (розчинених речовин в розчині може бути як завгодно багато).
Розчинником умовно вважають компонент, агрегатний стан якого не змінюється при утворенні розчину і вміст якого переважає в даній системі.
Наприклад, повітря – це розчин кисню, карбон (ІV) оксиду, водяних парів, інертних та інших газів в азоті, поскільки його вміст в повітрі складає 78%.
Приклад 2. Які розчини називаються насиченими, ненасиченими, перенасиченими?
Відповідь:
Розчин, у якому речовина більше не розчиняється за даної температури, називається насиченими.
Наприклад, у воді масою 100 г при t0 = 200C розчиняється натрій хлорид масою 36 г. Більше натрій хлориду в такому об’ємі води розчинитися не може, тобто маємо насичений розчин.
Розчин, у якому речовина ще може розчинитися за даної температури, називається ненасиченим.
Наприклад, якщо у воді масою 100 г розчинити натрій хлорид масою 20 г при t0 = 200C, утвориться ненасичений розчин. У цьому розчині, за такої ж температури, може ще розчинитися ця сіль масою 16 г.
Поняття „насичені” і „ненасичені розчини” не слід ототожнювати з поняттям „концентровані” і „розведені розчини”. Існує багато малорозчинних речовин, насичені розчини яких мають низьку концентрацію розчиненою речовини (наприклад з Са(ОН)2, СаSO4 тощо).
Для деяких речовин можна отримати розчини, концентрація яких за даної температури вища, ніж концентрація насиченого розчину. Такі розчини називаються перенасиченим. Вони нестійкі, і якщо внести в такий розчин центр кристалізації (кристалик розчиненої речовини, пил тощо), надлишок розчиненої речовини викристалізується. Це відбувається тому, що швидкість виділення речовини з розчину більша за швидкість розчинення.
Наприклад, за нагрівання можна одержати досить концентрований розчин натрій ацетату, відділити його від твердої фази і обережно охолодити, після чого концентрація солі буде більшою, ніж в насиченому розчині, але її надлишок з розчину не виділяється.
Перенасичені розчини часто застосовують для очищення речовин (метод перекристалізації).
Приклад 3. Який процес називається розчинністю?
Відповідь:
В природі немає абсолютно нерозчинних речовин. Властивість речовини розчинятись в даному розчиннику за даних умов (температурі, тиску) чисельно характеризується розчинністю.
Розчинність – це максимальна маса речовини, яка може розчинятись в 100 г, розчинника.
При розчинності всі речовини ділять на три групи. Якщо в 100 г води розчиняється більше 10 г, то така речовина називається добре розчинною і позначається в таблиці розчинності „ р ”.
Якщо в 100 г води розчиняється менше 1 г речовини – малорозчинною (м), а коли розчиняється менше 0,01 г речовини – нерозчинною (н).
Кількісною характеристикою розчинності речовин є коефіцієнт розчинності. Коефіцієнтом розчинності називається відношення маси речовини, яка утворює при даній температурі насичений розчин, до об’єму розчинника: 

де Ks – коефіцієнт розчинності;
mp – маса речовини, яка утворює насичений при даній температурі розчин;
V – об’єм розчинника.
Для водних розчинів:

де m (H2O) – маса води.
Розчинність залежить від температури, тому коефіцієнти розчинності будуть справедливі тільки певним температурам. Наприклад, якщо при 60˚С в 100 г води може розчинитися 61 г MgCl2, то й коефіцієнт розчинності дорівнює:
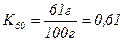 (величина безрозмірна).
(величина безрозмірна).
Приклад 4. Дайте визначення поняття „ступінь дисоціації”. Як розділяють електроліти за ступенем дисоціації?
Відповідь:
Ступінь дисоціації – визначається співвідношенням концентрацій тієї частки електроліту, що зазнала розпаду на йони, до загальної його концентрації:

де α – ступінь дисоціації;
Nдис . – молекули, що розпалися на йони;
N – вихідне число розчинених молекул.
Ступінь дисоціації виражається у відсотках, чи числом від 0 до 1. Наприклад, для 0,001М водних розчинів кислот ступінь дисоціації має такі значення:
хлоридна (HCl) – 0,993 або 99,3%
сульфатна (H2SO4)– 0,960 або 96,0%
оцтова (CH3COOH) – 0,126 або 12,6%
ціанідна (HCN) – 0,0011 або 0,11%
За величиною ступеня дисоціації електроліти поділяють на сильні (α близько 100%), слабкі (α менше 5%).
| Речовини | Сильні електроліти | Слабкі електроліти |
| Кислоти | H2SO4, HNO3, HCl, HBr, HI, HClO4, HMnO4, H2SeO4, H2TeO4 | Органічні кислоти, HCN, H2S, H2SiO3, H2CO3 |
| Основи | Луги (гідроксиди елементів І А та ІІ А підгруп крім Be(OH)2 Mg(OH)2), TlOH | NH3∙H2O(NH4OH); основи d-елементів (зокрема Fe(OH)3, Cr(OH)3, Cu(OH)2); основи p-елементів (Al(OH)3, Bi(OH)3, Sn(OH)2) |
| Солі | Майже всі | Hg2Cl2, Fe(NCS)3, Pb(CH3COO)2 |
Іноді виділяють проміжну групу речовин – це електроліти середньої (проміжної) сили (α ~3-5%). До них відносять: розчини HNO2, HF, H2SО3, H3PO4, НРО3, Ca(OH)2.
Такій розподіл є досить умовним, оскільки ступінь дисоціації залежить від багатьох факторів: від природи розчинника, температури, концентрації розчину. Так, чим більше розведення, тим більшим стає ступінь дисоціації.
Приклад 5. Чому дорівнюють константи електролітичної дисоціації сильних і слабких електролітів?
Відповідь:
Електролітична дисоціація - це рівноважний процес, який можна характеризувати константою електролітичної рівноваги.
Для прикладу дисоціації слабкого електроліту амоній гідроксиду константу електролітичної дисоціації можна записати так:
NH4OH ↔ NH4+ + ОН-
звідки:
Кд = 

де [NH4+] і [OH−] - концентрації йонів, моль/л.
Чим більше значення Kд - тим краще електроліт розпадається, на йони. Для даного електроліту значення K постійне при певній температурі і не залежить від концентрації.
Сильні електроліти мають K > 10-1, слабкі - електроліти мають значення K < 10-3.
Так для CH3COOH (t = 250C) Kд = 1,75 ∙ 10-5 вказує на те, що оцтова кислота - слабкий електроліт. Для Са(ОН)2 (t = 250C) Кд = 4,0 ∙ 10 -2 - електроліт середньої сили, який швидше можна віднести до сильних електролітів.
Багатоосновні кислоти і основи дисоціюють стадійно. Відповідно, для кожної стадії рівноважного стану існують свої значення константи дисоціації. Так для ортофосфатної кислоти Н3РО4:
І стадія Н3РО4 ↔ H+ + H2PO4 -
К1 =  = 7,1 ∙ 10-3
= 7,1 ∙ 10-3
П стадія H2PO4- ↔ H+ + HPO42 -
К2 =  = 6,2 ∙ 10-8
= 6,2 ∙ 10-8
ІП стадія HPO42 - ↔ H+ + PO43-
К3 =  = 4,4 ∙ 10-13
= 4,4 ∙ 10-13
Константа дисоціації багатоосновної кислоти для всіх стадій рівна добутку констант її окремих стадій. Наприклад, для Н3РО4 Кд рівна:
Кд = К1 ∙ К2 ∙ К3
Як видно із значень констант дисоціації для ортофосфатної кислоти (і для інших багатоосновних кислот) кожне наступне значення відрізняється від попереднього ~ в 105 раз.
Порівнюючи величини Kд різних стадій дає можливість говорити про те, що для ортофосфатної кислоти (і для інших багатоосновних кислот) дисоціація протікає в основному по першій стадії.
Таке ж співвідношення між Kд характерне і для основ.
Приклад 6. Як розраховується водневий показник?
Відповідь:
Чиста вода за звичайних умов в малій мірі проводить електричний струм. Приблизно лише одна з 10 млн. молекул дисоціює на йони:
Н2О ↔ Н+ + ОН- ΔН = 57,3 кДж
Константа дисоціації води: Кд =  = 1,8∙10-16 (за температури 298 К).
= 1,8∙10-16 (за температури 298 К).
Внаслідок незначної дисоціації можна вважати, що концентрація недисоційованої частини молекул Н2О є сталою. Розраховуємо [ Н2О ], прийнявши до уваги, що маса 1 л води ~ 1000 г:
[ Н2О] = 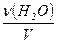 =
= 
Перенесемо сталі члени у виразі константи дисоціації в ліву частину:
К ∙ [H2O] = [H+] ∙ [OH-]
Це означає, що за певної температури добуток К ∙ [H2O] є сталою величиною. За 298 К він дорівнює
1,8 ∙ 10-16 ∙ 55,56 = 10-14 і називається йонним добутком води Кв:
Кв = [H+] ∙ [OH-] = 10-14
Йонний добуток залежить від температури. За нагрівання, згідно з принципом Ле Шательє, посилюється процес утворення йонів.
Для хімічно чистої (дистильованої) води:
[H+] = [OH-] = 10-7 моль/л
Водневий показник – це від’ємний десятковий логарифм концентрації катіонів Гідрогену:
рН = -lg[H+]
Водневий показник використовується для визначення кислотності середовища:
Шкала рН
|
|
|
|


|
|
|

На практиці` для визначення рН середовища використовують індикатори та спеціальні вимірювальні йономіри (рН -метри).
Приклад 7. Що таке йон гідроксонію і як він утворюється? Який тип зв’язку в цьому йоні?
Відповідь:
Йон гідроксонію  - це гідрат йона Гідрогену, який утворюється при дисоціації молекул кислоти у воді. Тип зв’язку в йоні гідроксонію - донорно-акцепторний. Схема утворення йону гідроксонію:
- це гідрат йона Гідрогену, який утворюється при дисоціації молекул кислоти у воді. Тип зв’язку в йоні гідроксонію - донорно-акцепторний. Схема утворення йону гідроксонію:  .
.
Приклад 8. Напишіть рівняння процесів дисоціації ортофосфатної кислоти, калій гідроксиду і алюміній сульфату.
Відповідь:
Багатоосновні кислоти дисоціюють ступінчасто:


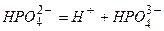
Калій гідроксид дисоціює на йон Калію і гідроксид-іон:

Алюміній сульфат дисоціює за схемою:

Приклад 9. Напишіть рівняння процесів дисоціації цинк гідроксиду, калій гідрогенсульфату і магнійгідроксо нітрату.
Відповідь:
а) дисоціація цинк гідроксиду
Дисоціація амфотерних електролітів можлива по місцях обох зв’язків. Наприклад:


б) дисоціація калій гідрогенсульфату
При дисоціації кислих солей, складні аніони кислотного залишку розкладаються (дисоціюють) з утворенням йонів  :
:

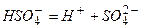
в) дисоціація магнійгідроксо нітрату
При дисоціації основних солей утворюються складні катіони, здатні дисоціювати з утворенням гідроксид-іонів


Приклад 10. Дано розчини, які містять йони 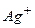 ,
,  ,
,  ,
,  . За допомогою яких реакцій можна визначити ці розчини? Напишіть рівняння реакцій.
. За допомогою яких реакцій можна визначити ці розчини? Напишіть рівняння реакцій.
Відповідь:
Розчин, який містить йони 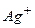 , можна визначити, доливаючи до нього розчин натрій хлориду. При цьому випадає білий осад аргентум хлориду
, можна визначити, доливаючи до нього розчин натрій хлориду. При цьому випадає білий осад аргентум хлориду

Розчин, який містить йони  , можна визначити за допомогою розчину барій хлориду. При цьому випадає білий осад барій сульфату
, можна визначити за допомогою розчину барій хлориду. При цьому випадає білий осад барій сульфату







