Фенольный гидроксил в результате химических превращений дает те же продукты, что и спиртовой гидроксил: феноляты, простые и сложные эфиры и др. На ход и направление соответствующих реакций бензольное кольцо практически не влияет. А вот реакционная способность фенольного гидроксила из-за ароматического ядра значительно снижается. Примером может послужить отрицательный результат, полученный при попытках заместить гидроксил на хлор. Концентрированные галогенводородные кислоты гидроксил в фенолах не замещают, пятихлористый фосфор вызывает хлорирование в ядро, треххлористый фосфор образует трифенилфосфат. Следует в то же время отметить, что иногда фенольный гидроксил все же удается заместить на хлор. Это случается с фенолами, содержащими в кольце, кроме гидроксила, электроноакцепторные заместители. С этими фенолами реакцию удается провести как бимолекулярное нуклеофильное замещение

14.1.2.1. Кислотность. Подобно спиртам фенолы проявляют определенную кислотность. Учитывая эту особенность самого фенола, его иногда называют карболовой кислотой, карболкой. Для того чтобы иметь возможность судить о кислотности фенолов, сопоставим константы кислотности Ка некоторых родственных им соединений.
Соединения Ка
спирты 10-16 – 10-18
фенолы 10-10
карбоновые кислоты 10-5
п -крезол 0,67 · 10-10
о -хлорфенол 77 · 10-10
о -нитрофенол 600 · 10-10
пирокатехин 1·10-10
резорцин 3 · 10-10
гидрохинон 2 · 10-10
Из этих данных видно, что кислотность фенолов на много порядков выше, чем спиртов. Это объясняется тем, что феноксид-анион, получающийся при депротонировании фенола, в значительной степени стабилизирован за счет делокализации отрицательного заряда с участием бензольного кольца

На стабильность феноксид-аниона, следовательно, и на кислотность фенола влияют и заместители в ароматическом кольце. Это влияние зависит от природы заместителя, от их числа и положения в бензольном кольце. В общем случае электронодонорные заместители снижают кислотность фенолов, а электроноакцепторные заместители повышают ее.
Будучи кислотами, фенолы с основаниями дают соли, которые называются фенолятами

При добавлении к фенолам хлористого железа в разбавленных водных или спиртовых растворах появляется фиолетовое (фенол) или синее окрашивание (крезолы). Появление окраски в этих случаях связывают с образованием фенолятов трехвалентного железа, поглощающих свет в видимой области.
14.1.2.2. Образование простых эфиров. Просто реакцией фенолов со спиртами простые эфиры фенолов не получить. Это удается только при использовании сильных алкилирующих средств (диметилсульфат) или использовании реакции Вильямсона. В обоих случаях реакция проводится в щелочной среде, в которой фенол существует в виде фенолят-аниона. Этот нуклеофил, который гораздо сильнее самого фенола, атакует галогенид или сульфат с образованием простого эфира (реакция SN 2)

Нетрудно видеть, что в реакции Вильямсона для получения одного и того же простого эфира можно использовать и другую пару реагентов – арилгалогенид и алкоголят спирта. Однако ароматически связанный галоген неспособен участвовать в этой реакции. Это удается лишь в том случае, когда в ароматическом кольце, кроме галогена, имеются активирующие группы – электроноакцепторные группы. В этом случае реакция идет как обычная реакция бимолекулярного замещения

Реакция Вильямсона используется не только как лабораторный метод, но и для получения некоторых простых эфиров в промышленном масштабе. Известным примером является синтез 2,4-дихлорфеноксиуксусной кислоты (2,4-Д) реакцией 2,4-дихлорфенолята натрия с натриевой солью монохлоруксусной кислоты
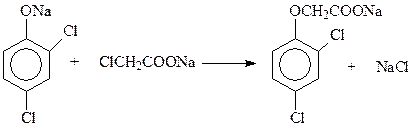
В результате реакции Вильямсона кислородный атом фенола получает алкильный заместитель, поэтому говорят, что происходит О -алкилирование. При этом практически не происходит С -алкилирования, т.е. вступления заместителя в кольцо. Объясняется это тем, что из двух конкурирующих реакций О - и С -алкилирования первая идет быстрее. Кроме того, во многих случаях продукт О -алкилирования термодинамически более устойчив. Однако это не всегда так. При 2000С аллилфениловый эфир изомеризуется в о -аллилфенол
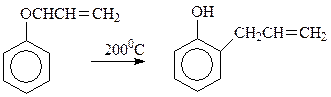
Эта реакция присуща лишь аллиловым эфирам и носит название перегруппировки Кляйзена (1912 г.). Предполагается, что реакция идет через циклическое переходное состояние

В реакции Кляйзена происходит миграция аллильной группы в о -положение с одновременной аллильной перегруппировкой этой группы. Если обе о -положения заняты, то мигрирующая аллильная группа может занять п -положение. Опыты с меченым углеродом показали

что в этом случае перемещение аллильной группы в кольцо происходит не так как в предыдущем случае. Похоже на то, что при п -миграции аллильная группа отщепляется от эфира и в виде аллильного катиона атакует свободное положение бензольного кольца. Это напоминает перегруппировку Фриса с участием сложных эфиров фенолов.
Своеобразными простыми эфирами фенолов являются так называемые оксиэтилированные алкилфенолы, оказавшиеся хорошими неионогенными моющими средствами. Их получают реакцией алкилфенолов с окисью этилена в щелочной среде при 1800С

К простым эфирам фенолов относятся и эпоксидные смолы, получаемые на основе бис -фенола и эпихлоргидрина.
Обозначим средний фрагмент бис -фенола через R
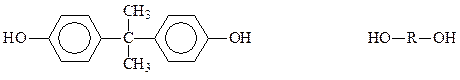
Тогда реакцию бис -фенола с двумя молекулами эпихлоргидрина можно записать так

Образовавшийся диэпоксид вступает в реакцию раскрытия эпоксидного кольца

При многократном повторении этих реакций (Вильямсона и раскрытия эпоксидного кольца) получается эпоксидная смола

Смола может быть отверждена – превращена в полимер с трехмерной структурой несколькими способами. Чаще всего при этом используются трифункциональные амины, в частности, диэтилентриамин

При отверждении каждая аминогруппа действует как нуклеофил на эпоксидную группу

По завершении раскрытия эпоксидных колец получается полимер с поперечными связями.
14.1.2.3. Образование сложных эфиров. Как от гидроксилсодержащих соединений от фенолов можно было бы ожидать участия в реакции Фишера (этерификации) с кислотами с образованием сложных эфиров. Однако этого не происходит. Для фенолов карбоновые кислоты – слишком слабые ацилирующие агенты. Поэтому для получения сложных эфиров фенолов приходится использовать ангидриды и галогенангидриды карбоновых кислот в щелочной среде (метод Шоттен-Баумана)

Сложные эфиры фенолов обладают интересным свойством – при нагревании с хлористым алюминием они претерпевают перегруппировку с миграцией ацильной части эфира в свободное о - и п -положение бензольного кольца (перегруппировка Фриса, 1908 г.)

Предполагается, что перегруппировка Фриса протекает как реакция внутримолекулярного ацилирования: вначале происходит генерация ацилий-катиона RCO +, который далее атакует бензольное кольцо.
Некоторые сложные эфиры фенолов нашли применение как полимеры полиэфирного типа.
Еще в 1953 году в Германии был получен сложный эфир бис -фенола и угольной кислоты – поли-[2,2- бис -(фенилен)-пропанкарбонат], обладающий уникальными свойствами. Полимер (лексан, мерлон, поликарбонат) оказался прозрачным как стекло и прочным как сталь. Поликарбонат обычно получают реакцией бис -фенола с фосгеном

14.1.2.4. Отщепление гидроксильной группы. В фенолах гидроксильная группа с бензольным кольцом связана достаточно прочно. Можно даже провести аналогию с ароматически связанным галогеном. Тем не менее, найдены условия элиминирования гидроксила фенолов. Это происходит при нагревании фенолов с цинковым порошком







