Атом кислорода входит в состав целого ряда функциональных групп, определяющих принадлежность соединения к тому или иному классу органических соединений. Представляется целесообразным такие классы объединить и рассмотреть в одном разделе, поскольку многие их свойства формируются общим для них атомом кислорода. Кроме того, ароматические соединения кислорода связаны между собой многочисленными взаимными превращениями.
К ароматическим соединениям кислорода относятся: фенолы, хиноны, ароматические спирты, карбонильные соединения и карбоновые кислоты.
Глава 14
Фенолы
К фенолам относятся соединения, в молекуле которых имеется гидроксильная группа, непосредственно связанная с бензольным кольцом. В зависимости от числа гидроксилов различают атомность фенолов. Кроме гидроксильных групп, в бензольном кольце могут находиться и другие замещающие группы.
Наиболее часто встречающимися фенолами являются следующие
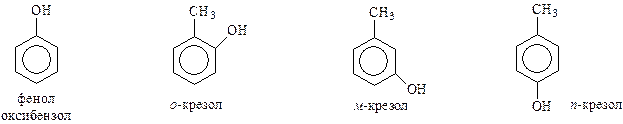
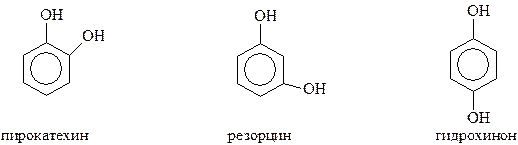
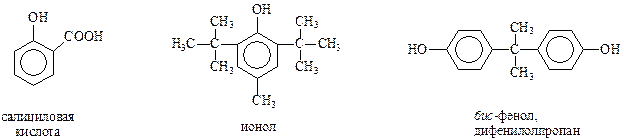
Многие фенолы имеют тривиальные названия. По систематической номенклатуре их рассматривают как производные самого фенола. Иногда, в сложных случаях, при составлении названия за основу берется боковая цепь.
Одноатомные фенолы
Многие фенолы, особенно сам фенол, имеют обширные области практического применения. Поэтому разработан целый ряд способов их получения, некоторые из них осуществлены в промышленности. В основе этих методов лежат уже рассмотренные ранее реакции, поэтому они здесь будут лишь упомянуты, а другие рассмотрены более подробно.
Методы получения
14.1.1.1. Гидролиз галогенпроизводных аренов. Гидролиз самого хлорбензола протекает с большим трудом из-за – I -эффекта атома хлора по механизму «элиминирование – присоединение». Условия гидролиза: 10-15%-ный водный раствор NaOH, 3500С, 315 атм., время реакции – 20 мин
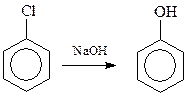
Хлорбензолы, содержащие в кольце и другие заместители электроноакцепторного типа, гидролизуются значительно легче по бимолекулярному механизму. Интересно, что в качестве таких облегчающих гидролиз заместителей могут выступать и атомы галогена. На этом основано получение хлорфенолов: 2,4,5-трихлорфенола и пентахлорфенола
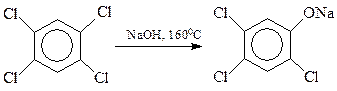
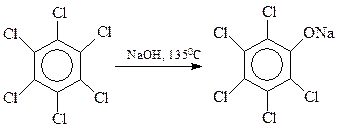
С сожалением приходиться отмечать, что процесс гидролиза тетрахлорбензола часто выходит из-под контроля. При этом быстро и самопроизвольно температура реакции повышается со 1600С до 2300С и выше, происходит соответствующее повышение давления. При таком развитии событий (Севезо, 1976 г.) две молекулы фенолята натрия трихлорфенола вступают между собой в реакцию Вильямсона с образованием 2,3,7,8-тетрахлордибензо- п -диоксина
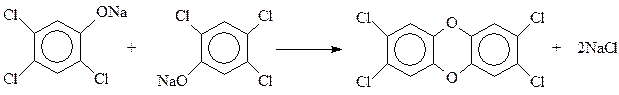
Диоксин – один из наиболее ядовитых органических соединений, созданных когда-либо руками человека. Среднесмертельная доза для человека, полученная расчетным путем, составляет при однократном оральном поступлении 0,05-0,07 микрограммов (миллионных долей грамма).
14.1.1.2. Щелочной плав солей сульфоновых кислот. Этот метод раньше, до разработки кумольного метода, широко применялся для получения фенола и крезолов. Замещение сульфогруппы на гидроксил осуществляется при нагревании солей сульфоновых кислот с едкими щелочами при 3000С и выше
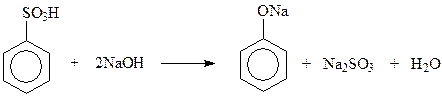
14.1.1.3. Замещение диазогруппы на гидроксил. Эта реакция протекает легко даже в водном растворе соли диазония при 5 – 100С
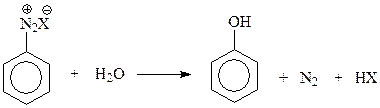
Гидролиз солей диазония – удобный и универсальный лабораторный метод получения разнообразных фенолов.
14.1.1.4. Кумольный метод. Такое название получил метод синтеза фенола разложением гидроперекисей алкилбензолов, чаще всего кумола (Сергеев, Удрис, Кружалов)
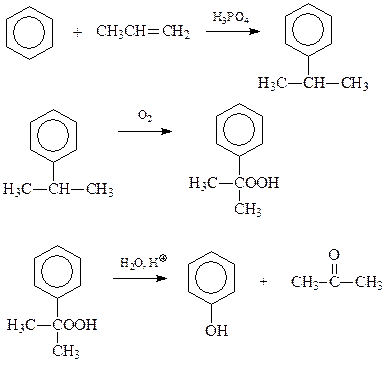
В приведенной схеме ключевым является превращение гидроперекиси кумола в фенол и ацетон.
Предложен следующий механизм кислотного разложения гидроперекиси.
В начальной стадии происходит протонирование гидроксильного кислорода гидроперекиси, который далее отщепляет молекулу воды и превращается в окисный катион
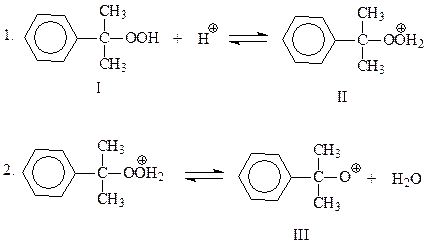
Эта промежуточная частица претерпевает перегруппировку по механизму 1,2-фенильного сдвига. Сам факт этой перегруппировки свидетельствует, что резонансный гибрид канонических структур IV и V устойчивее, чем окисный катион III. Полагают, что движущая сила перегруппировки достаточно велика и, возможно, 2 и 3 стадии рассматриваемого механизма протекают одновременно
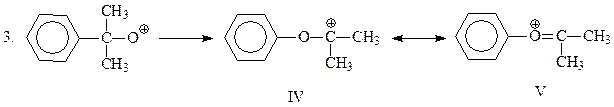
Электрофильная частица, представленная формулами IV и V, присоединяет воду и отщепляет протон. В результате получается гемикеталь VII, образованный фенолом и ацетоном
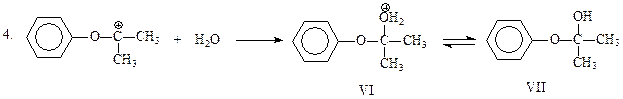
На финальной стадии имеет место гидролиз неустойчивого полукеталя
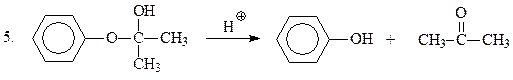
В настоящее время по кумольному методу получают основное количество фенола.
14.1.1.5. Разные реакции. В основу синтеза сложных фенолов, особенно находящих практическое применение, положены самые обычные реакции алкилирования, галогенирования и конденсации самого фенола.
Ниже приводятся примеры таких специальных синтезов.
Как известно, необходимый для синтеза гербицида 2,4-Д дихлорфенол получают хлорированием фенола
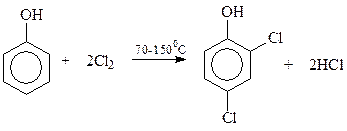
Одним из эффективных антиоксидантов, ингибирующих окисление многих веществ кислородом воздуха, оказались так называемые экранированные фенолы, особенно 4-метил-2,6-ди- трет -бутилфенол (ионол). Его можно получить алкилированием п -крезола изобутиленом
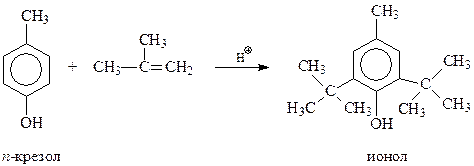
Так же с использованием реакции Фриделя-Крафтса осуществляется синтез алкилфенолов исходя из фенола и тримеров и тетрамеров пропилена и изобутилена
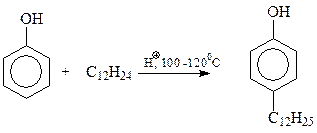
Еще один пример – синтез так называемого бис -фенола, на основе которого производится ценнейший полимер – поликарбонат, относящийся к сложным эфирам угольной кислоты
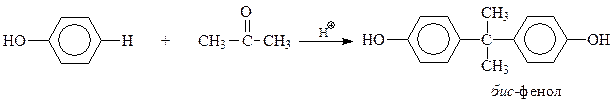
В бензольное кольцо в фенолах могут быть введены и функциональные группы. Одним из интересных примеров может послужить синтез салициловой кислоты по реакции Кольбе-Шмидта
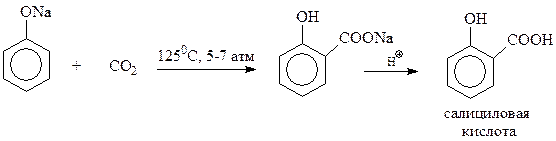
Химические свойства
В соответствии со строением молекулы фенолы вступают в химические реакции за счет бензольного кольца или гидроксильной группы. При этом указанные функциональные группы оказывают влияние друг на друга.






