Перекись водорода в кислой среде окисляется перманганатом калия. В соответствии с уравнением реакции:
Задачи для самостоятельного решения.
Пример 1
Какая масса (г) пероксида водорода содержится в пробе, если при титровании израсходовано 14,50 мл перманганата калия с Т (КMnО4/Fe) = 0,08376 г/мл?
Решение.
При прямом титровании число молей эквивалента определяемого вещества (пероксида водорода) равно числу молей эквивалента титранта (перманганата калия). При перманганатометрическом титровании пероксида водорода протекает реакция
5Н2О2 + 2МnО4- + 6Н+ → 5О2 + 2Мn2+ + 8Н2О
и соответствующие полуреакции:
МnО4- + 8Н+ + 5е → Мn2+ + 4Н2О
Н2О2 – 2e- →О2 + 2Н+
Из уравнений следует, что f э (КMnО4) = 1/5, а f э (Н2О2) = ½, поскольку один электрон химически эквивалентен условным частицам 1/5 КMnО4 и ½ Н2О2. Следовательно,
n (1/5КMnО4) = Т (KMnO4/Fe)∙ V (KMnO4)/М(Fe)
и n (1/2 H2O2) = m (H2O2)/М(1/2 Н2О2)
Поскольку n (1/5 KMnO4) = n (1/2 H2O2), то после преобразований получаем
 = Т (KMnO4/Fe)∙ V (KMnO4)/ М (Fe)∙ М (1/2 Н2О2)
= Т (KMnO4/Fe)∙ V (KMnO4)/ М (Fe)∙ М (1/2 Н2О2)
 = (0,08376∙14,50/55,847)∙17,0073=0,3699 г.
= (0,08376∙14,50/55,847)∙17,0073=0,3699 г.
1. Рассчитайте навеску KMnO4, необходимую для приготовления 1 л 0,02н раствора.
2. На титрование 4,5 мл 0,1н раствора щавелевой кислоты израсходовано 55 мл KMnO4. Рассчитайте нормальность и титр раствора KMnO4.
3. Сколько граммов KMnO4 надо взять, чтобы приготовить 1,5л 0,05Н раствора его для титрования в кислой среде?
4. До какого объема следует разбавить 500мл 0,1Н раствор K2Cr2O7 для получения раствора с титром 0,005г/мл?
5. К раствору, содержащему 0,1510г технического Na2SO3 прилили 100мл 0,0985Н раствора I2, избыток которого оттитровали 48,6мл 0,0204Н раствора Na2S2O3. Вычислить процентное содержание Na2SO3 в образце?
Тестоввые задания для самостоятельного решения.
Выберите один правильный ответ
001. СУММА КОЭФФИЦИЕНТОВ В ПРАВОЙ ЧАСТИ РЕАКЦИИ РАВНА

1) 5
2) 7
3) 8
4) 9
5) 10
002. ДЛЯ УСТАНОВЛЕНИЯ ТИРА KMnO4 ИСПОЛЬЗУЮТ
1) H2SO4, KI, I2
2) H2SO4, H2C2O4
3) NaOH, Na2SO3
4) K2Cr2O7, H2SO4
5) Na2B4O7
003. В ПЕРМАНГАНАТОМЕТРИИ ИСПОЛЬЗУЮТ ИНДИКАТОР:
1) метиловый оранжевый
2) фенолфталеин
3) крахмал
4) перманганат калия
5) эозин
004. В ХОДЕ ПЕРМАНГАНАТОМЕТРИЧЕСКОГО ТИТРОВАНИЯ ОКРАСКА РАСТВОРА МЕНЯЕТСЯ
1) от розовой до бледно-желтой,
2) от розовой до бесцветной,
3) от розовой до зеленовато-желтой
4) от бесцветной до бледно-желтой
5) от синей до розовой
005. НА ТИТРОВАНИЕ НАВЕСКИ 0,1133 Г Na2C2O4 (х.ч.) В КИСЛОЙ СРЕДЕ ПОШЛО 20,75 МЛ РАСТВОРА KMnO4. НОРМАЛЬНОСТЬ ЭТОГО РАСТВОРА СООТВЕТСТВУЕТ:
1) 0,0407 н
2) 0,0815 н
3) 0,0203 н
4) 0,015 н
5) 0,0316 н
006. МОЛЯPНАЯ МАССА ЭКВИВАЛЕНТА KMnO4 ПPИ ИСПОЛЬЗОВАНИИ ЕГО В КАЧЕСТВЕ ОКИСЛИТЕЛЯ В КИСЛОЙ СPЕДЕ РАВНА:
1) 158 г/моль
2) 79 г/моль
3) 52,6 г/моль
4) 31,6 г/моль
5) 22,6 г/моль
007. ПО МЕТОДУ ПЕРМАНГАНАТОМЕТРИИ МОЖНО ПРОВОДИТЬ КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ:
1) окислителей
2) восстановителей
3) кислот и оснований
4) окислителей и восстановителей
5) оксидов
Занятие №11
«ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОЕ ТИТРОВАНИЕ. ИОДОМЕТРИЯ»
Вопросы к занятию
1. Метод иодометрия. Сущность метода.
2. Приготовление и стандартизация рабочих растворов.
3. Применение иодометрии в медицинской практике и фармации.
Иодометрия
Иодометрия – это титриметрический метод определения окислителей и восстановителей, основанный на реакции
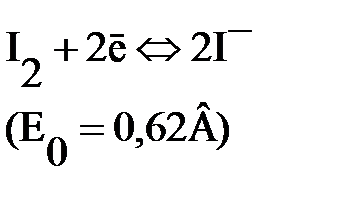
Йод плохо растворим в воде, но в присутствии йодид-ионов образуется комплекс I3-, поэтому при титровании протекает реакция

Стандартные потенциалы многих восстановителей меньше Е0(I3–/3I–), а многих окислителей – выше, поэтому система служит для определения и окислителей, и восстановителей.
Иодометрические методы основаны на применении стандартного раствора тиосульфата натрия для титрования иода, выделившегося при взаимодействии определяемого окислителя с избытком иодида калия (при титровании по замещению) или оставшегося в избытке при медленном взаимодействии определяемого восстановителя с фиксированным объемом стандартного раствора иода (в случае обратного титрования).
В иодометрии наибольшее значение имеет реакция взаимодействия йода с тиосульфатом натрия, протекающая по уравнению:

Продуктом реакции является тетратионат натрия Na2S4O6 – натриевая соль тетратионовой кислоты.
Йод в зависимости от концентрации окрашивает растворы от желтого до красно-бурого цвета. Для точного фиксирования точки эквивалентности в данной реакции применяют раствор крахмала, который добавляют перед концом титрования (когда раствор становиться бледно-желтым). Йод образует с крахмалом интенсивно синее соединение. В момент эквивалентности, когда восстанавливается весь йод, синяя окраска исчезает, и раствор становится бесцветным.
Прямая реакция восстановления йода идет быстро, но обратная реакция окисления иодида протекает во времени. Поэтому использовать для определения окислителей раствор иодида невозможно. К тому же растворы иодидов (КI) неустойчивые, поскольку иодид окисляется кислородом воздуха. Поэтому используют косвенный прием – добавляют к окислителю избыток иодида, а выделившийся йод оттитровывают стандартным раствором тиосульфатам натрия:

Непосредственное титрование тиосульфата раствором K2Cr2O7 невозможна из-за нестехиометричности реакции. Индикатором так же служит крахмал.
Йодометрические определения восстановителей проводят по методу обратного титрования. К анализируемому раствору добавляют титрованный раствор йода в избытке. С определяемым веществом реагирует эквивалентное количество йода, например

Избыток йода титруют рабочим раствором тиосульфата натрия. Зная общее количество йода и непрореагировавший избыток, рассчитывают количество йода, эквивалентное анализируемому веществу.
Прямое титрование сульфитов раствором йода обычно дает уменьшенные результаты, т.к. во время титрования часть сульфита окисляется кислородом воздуха.







