Щавелевая (этандиовая) кислота HOOC–COOH.Эта кислота очень распространена в растительном мире – в виде солей она содержится в листьях щавеля, кислицы, ревеня и т.д. Соли и эфиры это кислоты имеют тривиальное название – оксалаты (от греч. «oxalis» – щавель).
В промышленности щавелевую кислоту получают из формиата натрия:

Щавелевая кислота – одна из самых сильных карбоновых кислот, далеко превосходящая по силе свои гомологи.
Этандиовая кислота проявляет восстановительные свойства: в подкисленном растворе перманганата калия она окисляется до оксида углерода(IV) и воды.
При нагревании в присутствии серной кислоты происходит декарбоксилирование, и получается оксид углерода(IV) и муравьиная кислота:
Качественной реакцией на оксалат-ион является образование нерастворимой соли кальция:

Щавелевая кислота используется для полировки металлов, в деревообрабатывающей промышленности, при очистке урана
Малоновая (пропандиовая) кислота.

Эта кислота содержится в соке сахарной свеклы в виде кальциевой соли. В промышленности ее получают из хлоруксусной кислоты через промежуточную стадию – цианоуксусную кислоту, которая потом гидролизуется в малоновую.

Интересным свойством малоновой кислоты является способность образовывать недокись углерода  при обезвоживании фосфорным ангидридом
при обезвоживании фосфорным ангидридом  . Это вещество (
. Это вещество ( ) является своеобразным ангидридом пропандиовой кислоты. Еще одна ее особенность – декарбоксилирование при нагреве до 135℃, в результате чего образуется уксусная кислота.
) является своеобразным ангидридом пропандиовой кислоты. Еще одна ее особенность – декарбоксилирование при нагреве до 135℃, в результате чего образуется уксусная кислота.
Диэтиловый эфир этой кислоты имеет очень большое значение в промышленности – из него синтезируют различные лекарственные вещества, например барбитураты.
Янтарная (бутандиовая) кислота.

Основным отличием этой кислоты от предыдущих членов ряда является способность образовывать циклические производные – ангидриды и имиды. При длительном нагревании или при обезвоживании уксусным ангидридом эта кислота дает янтарный ангидрид, обладающий обычными свойствами ангидридов кислот. Например, при его взаимодействии с аммиаком получается имид (сукцинимид).
Впервые эта кислота была выделена из продуктов сухой перегонки янтаря, откуда она и получила свое название. Соли и эфиры этой кислоты носят название сукцинаты – от латинского «succinum» – янтарь. Янтарная кислота является промежуточным продуктом обмена веществ. Она применяется в текстильной и фармацевтической промышленности, в производстве инсектицидов, а так же смол и фотоматериалов.
Глутаровая (пентандиовая) кислота.

Впервые эта кислота была получена из глутаминовой аминокислоты, а та получила свое название от латинского «gluten» – клей, поскольку была найдена в клейковине пшеницы.Эта кислота, как и янтарная, способна образовывать при нагревании циклический ангидрид.

5. Адипиновая (гександиовая) кислота

Эта кислота образуется при окислении жиров и получила свое название от латинского «adeps» – жир, сало.
При нагревании эта кислота не образует ангидрида.
В промышленности эту кислоту получают, главным образом, путем окисления циклогексанола 50% азотной кислотой в присутствии медно-ванадиевого катализатора.
Большинство этой кислоты в промышленности идет на изготовление нейлона. Так же, благодаря кислотным свойствам, гександиовую кислоту используют для удаления накипи с эмалированной посуды.
6. Бутендиовая кислота
Это простейшая непредельная дикарбоновая кислота. Она существует в виде двух стереоизомеров – цис-изомера и транс-изомера – малеиновой и фумаровой кислот.

Эти кислоты отличаются друг от друга по физическим свойствам – имеют разные температуры плавления, кипения, значения констант диссоциации и т.д. Малеиновая кислота при нагревании легко дегидратируется, давая циклический ангидрид. Он используется при производстве пластмасс. Фумаровая же кислота не образует ангидрида из-за удаленности в пространстве друг от друга карбоксильных групп.

В природе малеиновая кислота не существует. Она получается при каталитическом окислении бензола кислородом воздуха, причем сначала образуется малеиновый ангидрид, который затем гидролизуется в кислоту.
Фумаровая же кислота, напротив, широко распространена в природе, она содержится в грибах, лишайниках и высших растениях, например дымянке. Транс-бутендиовая кислота участвует в биохимических процессах. В промышленности ее получают изомеризацией малеиновой кислоты при нагревании или УФ-облучении. Эта реакция свидетельствует о большей энергетической устойчивости фумаровой кислоты. Оба изомера используются в промышленности для производства пластических масс и лакокрасочных материалов. Благодаря своему кислому вкусу фумаровая кислота используется в качестве вкусовой добавки к пищевым продуктам.
7. Фталевая (бензол -1, 2 дикарбоновая) кислота
В промышленности эту кислоту получают гидролизом фталевого ангидрида, который в свою очередь образуется при каталитическом окислении ортоксилола или нафталина кислородом воздуха.
При нагревании фталевая кислота легко отщепляет воду и образует фталевый ангидрид.

Именно он, а не сама кислота, служит источником для получения различных производных фталевой кислоты. Более половины производимого в мире ангидрида расходуется на получение средних(полных) эфиров фталевой кислоты. Эти эфиры добавляют в качестве пластификаторов к поливинилхлориду с целью придания эластичности изделиям из него. Диметилфталат используется как средство, отпугивающее гнус.
Из фталевого ангидрида так же получают фенолфталеин – индикатор щелочной среды в аналитической химии. Он образуется про конденсации фталевого ангидрида с фенолом в присутствии безводного хлорида цинка.
Ангидриды и их свойства
Не все дикарбоновые кислоты способны образовывать ангидриды. Так, высшие двухосновные кислоты не имеют таких циклических функциональных производных. Циклические ангидриды образуют только малеиновая, фталевая, глутаровая и янтарная кислоты.
Свойства ангидридов дикарбоновых кислот похожи на свойства ангидридов монокарбоновых кислот: при гидролизе они превращаются в кислоты, при добавлении аммиака переходят в имиды соответствующих кислот.
Систематическая номенклатура двухосновных карбоновых кислот (ИЮПАК):
1. Выбирают в молекуле наиболее длинную углеродную цепь С двумя карбоксильными группами СООН.
2. Нумерацию цепи начинают с атома углерода карбоксильной группы, причем, с того конца молекулы, у которого ближе и больше радикалов.
3. Называют окружающие радикалы: в порядке возрастания, с указанием количества и положения в цепи.
4. По длине цепи называют углеводород (алкен, алкин, диен и т. д.), указывая положение ненасыщенных связей, добавляя –диовая кислота.
Пример:

Изомерия
Для двухосновных карбоновых кислот характерна структурная изомерия, связанная со строением углеводородного радикала и положением ненасыщенных связей.
Структурная изомерия, связанная со строением углеводородного радикала:
Пример:
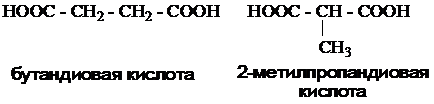
Структурная изомерия, связанная с положением ненасыщенных связей:
Пример:

Литература:
1. Зурабян, С.Э.,Лузин,А.П. Органическая химия: учебник/Под редакцией Н.А. Тюкавкиной. - М.:ГЭОТАР – Медиа, 2011.-384 с.: ил.
2. Габриелян О.С., Остроумова И.Г. Химия: учебник для студентов СПО. – 9-е изд.,стер.-М.:ИЦ.Академия, 2011.-336 с
Вопросы для самоконтроля:
1. В чем различие уксусной и щавелевой кислот?
2. Какие производные могут образовывать двухосновные кислоты?
3. Какими свойствами отличается малоновая кислота от других двухосновных кислот? Почему?
4. Получение двухосновных карбоновых кислот.
5. Специфические свойства двухосновных карбоновых кислот. Их кислые и средние соли.
6. Важнейшие представители карбоновых кислот: щавелевая, малоновая, янтарная, глутаровая кислоты.
Задания для самостоятельного выполнения:
1. Напишите формулы основных дикарбоновых кислот:
| Название кислоты | Формула кислоты |
| Щавелевая кислота | |
| Малоновая кислота | |
| Янтарная кислота | |
| Глутаровая кислота | |
| Адипиновая кислота | |
| Фталевая кислота |
1. Расставьте формулы и названия кислот: олеиновая кислота С17Н33СООН, стеариновая кислота С17Н35СООН, линолевая кислота С17Н31СООН, пальмитиновая кислота С15Н31СООН, уксусная кислота СН3СООН, бензойная кислота С6Н5СООН, муравьиная кислота НСООН – на соответствующие им места в схеме






