Перечень тем:
· Отдельные представители: этанол, метанол. Их свойства, применение.
· Отдельные представители многоатомных спиртов: глицерин.
· Непредельные спирты.
· Ароматические спирты.
· Фенол, его антисептические свойства.
· Отдельные представители двухатомных фенолов: пирокатехин.
· Рецорцин. его применение в медицине.
· Гидрохинон, его применение
Тема 3.4Строение и свойства оксосоединений.
План изучения темы:
1. Карбонильные соединения.Электронное строение карбонильной группы. Общая формула.
2. Строение альдегидов. Функциональная группа альдегидов (альдегидная), ее электронное строение.
3. Классификация альдегидов по типу углеродного радикала.
4. Гомологический ряд предельных альдегидов.
5. Номенклатура ИЮПАК, тривиальная номенклатура альдегидов.
6. Структурная изомерия (изомерия углеродного скелета), межклассовая изомерия.
8. Основные способы получения альдегидов.
9. Химические свойства альдегидов.
10 Формальдегид. Конденсация формальдегида с фенолом.
11. Строение и свойства кетонов.Ацетон.
Методические рекомендации по изучению материала
Изучить гомологический ряд, номенклатуру,способы получения, строение, физические и химические свойствакарбонильныхсоединений; механизм нуклеофильного присоединения. Обратите внимание на строение карбонильной группы. Сравните реакционные свойства альдегидов и кетонов.
Краткое изложение теоретических вопросов.
Альдегиды - органические вещества, молекулы которых содержат карбонильную группу, связанную с атомом водорода и углеводородным радикалом.
Общая формула альдегидов 
или R—CHO. Функциональная группа альдегидов (—CHO) называется альдегидной группой.
Кетоны - органические вещества, молекулы которых содержат карбонильную группу —  —, связанную с двумя углеводородными радикалами.
—, связанную с двумя углеводородными радикалами.
Общая формула кетонов  или R—CO—R'.
или R—CO—R'.
Альдегиды и кетоны называются карбонильными соединениями, их общая формула - C n H2 n O.
Химические свойства
Химические свойства альдегидов и кетонов обусловлены наличием в их молекулах сильно полярной карбонильной группы (связь  поляризована в сторону атома кислорода). Чем больше частичный заряд (
поляризована в сторону атома кислорода). Чем больше частичный заряд ( +) на атоме углерода этой группы, тем выше активность соединения.
+) на атоме углерода этой группы, тем выше активность соединения.
Горение:
2CH3CHO + 5O2  4CO2 + 4H2O
4CO2 + 4H2O
2CH3COCH3 + 9O2  6CO2 + 6H2O
6CO2 + 6H2O
Присоединение (по двойной связи карбонильной группы).
В ряду HCHO  RCHO
RCHO  RCOR' склонность к реакциям присоединения уменьшается. Это связано с наличием и числом углеводородных радикалов, связанных с атомом углерода карбонильной группы.
RCOR' склонность к реакциям присоединения уменьшается. Это связано с наличием и числом углеводородных радикалов, связанных с атомом углерода карбонильной группы.
а) Гидрирование (восстановление водородом):
HCHO + H2  CH3OH
CH3OH
CH3—CO—CH3 + H2  CH3—CH(OH)—CH3
CH3—CH(OH)—CH3
Из альдегидов при этом получаются первичные спирты, а из кетонов - вторичные.
Окисление:
CH3CHO + Ag2O 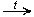 2Ag
2Ag  + CH3COOH (реакция "серебряного зеркала" - качественная реакция)
+ CH3COOH (реакция "серебряного зеркала" - качественная реакция)
HCHO + 2Cu(OH)2 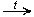 2H2O + Cu2O
2H2O + Cu2O  + HCOOH (образуется красный осадок - качественная реакция)
+ HCOOH (образуется красный осадок - качественная реакция)
Кетоны слабыми окислителями не окисляются.






