Розподільна хроматографія ґрунтується на різниці коефіцієнтів розподілення компонентів досліджуваної суміші між двома рідкими фазами, які взаємно не змішуються, причому одна фаза є нерухомою і знаходиться в порах твердого носія, який має також адсорбційні властивості.
Розподільна хроматографія, як і екстракція, ґрунтується на законі розподілення Нернста, згідно з яким відношення концентрацій речовини у двох різних фазах, які взаємно не змішуються, є величиною сталою для даної речовини і даної системи рідких фаз:
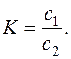
Якщо взяти ділильну лійку, внести в неї дві рідкі фази, які взаємно не змішуються, наприклад бутанол і воду, внести в лійку якусь речовину, що може розчинятися в обох фазах, але по різному, струшувати, то речовина розподілиться між цими двома фазами залежно від її спорідненості до кожної з фаз. Обов’язковою умовою при цьому є розчинність речовини в обох фазах, бо, якщо речовина розчинятиметься тільки в одній фазі, ніякого розподілення не відбудеться.
Якщо ж у ділильну лійку внести суміш речовин, струшувати, то речовини розподіляться між двома фазами по-різному залежно від їхніх коефіцієнтів розподілення.
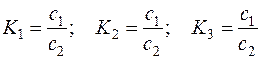 і т. д.,
і т. д.,
де с 1 і с 2 – концентрації речовини в першій і другій фазі.
Розглянемо конкретний приклад. У ділильну лійку, де знаходиться бутанол і вода, що взаємно не змішуються, внесемо, наприклад, 10 амінокислот. Перемішаємо вміст лійки. Після розділення фаз у кожній буде міститися по 10 амінокислот. Відкриємо кран лійки і зберемо окремо водну та бутанольну фазу. Водну фазу перенесемо у нову ділильну лійку і додамо чистого бутанолу. Після струшування суміші знову відбудеться розподілення 10 амінокислот між двома фазами, у бутанольній фазі буде теж 10 амінокислот. Але при цьому водна фаза відносно збагатиться тими амінокислотами, які більш споріднені до води. Бутанольну фазу з першої лійки теж перенесемо у нову ділильну лійку і додамо чистої води. Після струшування в добавлену водну фазу перейде також 10 амінокислот, а бутанольна фаза при цьому відносно збагатиться тими амінокислотами, які мають більшу спорідненість до бутанолу і яких у нову водну фазу перейшла незначна кількість.
Якщо розділити фази в кожній другій лійці, то матимемо окремо водну й бутанольну фазу з однієї лійки і водну й бутанольну фазу з другої лійки. Перенесемо ці розділені фази у нові ділильні лійки. Тепер їх буде вже чотири. Додавши в кожну з них відповідно чисті воду чи бутанол, повторимо операцію розділення.
Якщо зробити таких перенесень дуже багато, то врешті-решт можна одержати багато стаканчиків із фракціями амінокислот. Наприклад, їх уже 1000. У кожній фракції буде по 10 амінокислот. Але якщо у першому стаканчику якоїсь амінокислоти буде 99,999 %, то інших 9 амінокислот, разом узятих, – лише 0,001 %. У тисячному стаканчику якоїсь іншої амінокислоти буде, наприклад, 99,999 %, а 1-9 амінокислот, разом узятих, – лише 0,001 %. Застосовуючи при екстракції велику кількість перенесень у нові ділильні лійки, тобто здійснивши велику кількість актів розподілення, можна добре розділити суміш речовин. Проте, апаратура для екстракції дуже громіздка, і це зумовлює певні проблеми.
Щоб уникнути їх, спростити розділення, була введена розподільна хроматографія. Принциповим у цій хроматографії є те, що одна із фаз, які взаємно не змішуються, є нерухомою. Для закріплення однієї з фаз застосовують різні носії: крохмаль, алюміній оксид, силікагель, целюлозу, спеціальний хроматографічний папір. Розподільна хроматографія може бути колонковою, якщо носій поміщається в колонку, зверху наноситься суміш речовин, які потрібно розділити, і проявлення хроматограми здійснюється відповідним розчинником згори донизу; може бути тонкошаровою, паперовою. В останньому випадку носієм є спеціальний хроматографічний папір. Він являє собою особливий фільтрувальний папір, який не містить забруднюючих домішок і практично складається з чистої целюлози. Целюлозні волокна в ньому не перетинаються, цей папір має рівномірну товщину по всій довжині. Хроматографічний папір може мати різну щільність, і внаслідок цього, переміщення речовин на таких хроматограмах відбувається з різною швидкістю: чим щільніший папір, тим швидкість проявлення хроматограми менша.
Розглянемо суть хроматографії з паперовим носієм – хроматографію на папері. Зануримо кінець смужки хроматографічного паперу в систему „бутанол-вода”. Целюлоза має більшу спорідненість до води, ніж до бутанолу. Вода підніметься по капілярах паперу і змочуватиме смужку, далі, просякнувши хроматографічний папір, вона переходить у нерухому фазу, а крапельки бутанолу рухаються по поверхні змоченого паперу. Нанесемо на папір в одній точці суміш речовин, наприклад, 10 амінокислот, вище рівня рідини. (Точка або смужка нанесення на хроматограму речовин називається стартовою). Піднімаючись по хроматограмі вгору, крапелька бутанолу доходить до стартової точки, у якій є нерухома крапелька води і містяться ті ж 10 амінокислот. Відбувається акт розподілення речовин між водою і бутанолом у цій точці. Тобто, дана точка є по суті мікроскопічною ділильною лійкою. Спочатку бутанольна крапля не містила речовин, після розподілення в неї переходить теж 10 амінокислот – 10 амінокислот у стартовій точці (водна фаза) і 10 амінокислот у бутанольній краплі. Далі бутанольна крапля переміщується по хроматограмі вгору, і відбувається розподілення речовин між бутанольною краплею, що містить 10 амінокислот, і новою нерухомою краплею чистої води, у яку теж переходять 10 амінокислот. Бутанольна крапля переміщується ще вище, і відбувається розподілення між бутанольною краплею, що несе 10 амінокислот, і новою чистою нерухомою краплею води.
Отже, рухаючись уздовж хроматограми (проявлення хроматограми), бутанольна крапля переносить речовини. При цьому бутанольна фаза збагачується тими речовинами, які мають більшу спорідненість до бутанолу, а ті, що мають меншу спорідненість, залишаються у точках з водною фазою. Відбувається розподілення речовин на хроматограмі.
Таким чином, смужку паперу можна розглядати як систему з дуже великою кількістю точок, у яких відбувається акт розподілення. І, чим більше таких актів, тим краще розділення. Проте, ємність цих мікроскопічних „ділильних лійок” у випадку паперової хроматографії дуже незначна, тому паперова хроматографія непридатна для препаративного розділення речовин, а застосовується практично лише для аналітичних цілей.
Для даного прикладу, чим більше речовина має спорідненість до води і менше до бутанолу, тим менший шлях пройде вона на хроматограмі від старту. І, навпаки, чим більше вона має спорідненість до бутанолу і менше до води, тим більший її шлях на хроматограмі. Передній край речовини на хроматограмі завжди менший, ніж фронт розчинника. Якщо б речовина не мала зовсім спорідненості до води (тобто розчинялася тільки в бутанолі), то на хроматограмі вона йшла б з фронтом розчинника, а якщо мала б спорідненість тільки до води, то лишалася б на старті. Отже, суміш речовин, які розчиняються тільки в одній фазі, розділити неможливо.
Розташування речовин на хроматограмі цілком залежить від спорідненості їх до одної і другої фази, тобто від значення константи розподілення.
Таким чином, місце речовини на хроматограмі визначається за законом розподілення Нернста. Для графічної характеристики цього закону вводиться величина Rf:
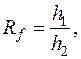
де h1 – шлях, пройдений речовиною на хроматограмі;
h2 – шлях, пройдений розчинником;
Rf – величина стала для даної речовини і даної системи рідких фаз.
Величина Rf завжди менша одиниці, бо речовина на хроматограмі знаходитися попереду розчинника не може.
Для розділення речовин за цим методом емпірично підбирають різноманітні системи рідких фаз, користуючись обов’язковим правилом: речовини, які потрібно розділити, повинні мати спорідненість до обох фаз. Значення Rf для різних речовин і різних систем рідких фаз зведені в довідниках у таблиці.
Величина Rf, хоча і є сталою (табличною) для даної речовини в даній системі рідких фаз, малопридатна для ідентифікації речовин на хроматограмах.
Положення речовини на хроматограмі залежить не тільки від значення коефіцієнта розподілення її між двома рідкими фазами. Суттєвий вплив мають інші фактори. Рівновага в точках розподілення речовин між двома фазами не настає миттєво, і речовини, які мали б більшою мірою перейти у водну фазу, не встигають цього зробити і переносяться краплею органічної речовини далі. Носій, зокрема целюлоза, адсорбує на своїй поверхні речовини, і вони затримуються носієм, не маючи змоги далі переноситися згідно з їх поведінкою за законом розподілення, величина Rf внаслідок цього буде мати занижене значення. На величину Rf впливає можлива хімічна взаємодія між рідкими фазами, між розчинником і речовинами, які розділяються, між речовинами і носієм. Змінюють значення Rf і домішки, які містяться у речовинах, що розділяються, або на носії. Особливо впливають на розділення органічних речовин мінеральні солі. Коефіцієнт розподілення набуває різних значень залежно від концентрації при застосуванні полярного розчинника, який сприяє дисоціації речовин, що розділяються; при малій швидкості проявлення хроматограми можлива дифузія речовин на носії та ін.
Для ідентифікації речовин на хроматограмах краще користуватися паралельним із сумішшю проявленням хроматограми з одною речовинию. При цьому на всіх хроматограмах заважаючі фактори будуть однаковими. У даному випадку визначати величину Rf не потрібно, слід прикласти хроматограму з індивідуальною речовиною до хроматограми із сумішшю і за положенням плям визначити речовину.
За технікою виконання паперова хроматографія може бути висхідною, коли проявлення хроматограми відбувається знизу вгору, і низхідною, коли розчинник рухається згори вниз. В останньому випадку не можна допустити стікання розчинника по хроматограмі, він, як і при висхідному способі проявлення, повинен рухатися по капілярах носія.
Висхідний та низхідний варіанти проявлення мають свої переваги та недоліки. При висхідному варіанті проявлення відбувається дуже довго, до місяця й більше без помітного розмивання плям. При цьому виключається небезпека перетікання розчинника з хроматограми, бо, коли фронт розчинника дійде до верхнього краю паперу, проявлення автоматично припиняється. При низхідному варіанті проявлення хроматограми відбувається швидко (кілька годин), але при цьому можливе стікання розчинника з хроматограми. Коли фронт розчинника дійде до кінця хроматограми, розчинник стікатиме з неї. Речовини, які мають великі значення Rf і йшли за фронтом розчинника, будуть залишати хроматограму. Проте, низхідна хроматографія дуже зручна для розділення речовин, які мають низькі та близькі значення Rf.
Наприклад, одна речовина має Rf = 0,10, інша – 0,12. Якщо розчинник пройшов 1 м, то перша речовина пройде на хроматограмі 10 см, друга – 12 см. Відстань між центрами плям буде становити 2 см. Але якщо фронт розчинника 50 см, то відстань між плямами буде лише 1см, тобто одна пляма накладається на іншу. Щоб розділити такі речовини, застосовують проточну хроматографію. До кінця хроматограми пришивають вату або картон і дають розчиннику стікати з хроматограми. Нехай стікання було таким, якби розчинник пройшов 5 метрів. Тоді відстань між речовинами з Rf =0,10 і Rf =0,12 становитиме вже 10 см, тобто вони добре розділяються. Щоб ці речовини не зійшли з хроматограми, вводять маркер–речовину, яка в даній системі рідких фаз має Rf трохи більше, ніж найбільш рухлива з тих речовин, які треба розділити. Коли кольорова пляма маркера доходить майже до кінця хроматограми, проявлення припиняється.
Якщо проявлення хроматограми здійснюють в одному напрямку (знизу вгору чи згори вниз), то така хроматографія називається одномірною. Внаслідок зазначених вище заважаючих факторів плями речовин на одномірних хроматограмах виявляються нечіткими, видовженими, з „хвостами”.
Щоб поліпшити результати, здійснюють повторне проявлення хроматограми. Після першого проявлення хроматограму виймають з камери, висушують, потім ставлять на друге проявлення. При другому проявленні речовина в „хвостах” переноситься до центра плям, оскільки розчинник раніше дійде „хвостів”, а центр плями ще буде сухим. Можна проводити і три проявлення одномірної хроматограми.
У паперовій хроматографії, як і у тонкошаровій, застосовується двомірна хроматографія. Техніка виконання аналогічна. Як носій використовується хроматографічний папір у формі квадрата.
Виявлення речовин на хроматограмах не викликає труднощів, коли вони забарвлені. Якщо вони не мають забарвлення, то проводять хімічні реакції з одержанням кольорових продуктів реакції. Якщо досліджувані речовини не дають кольорових реакцій, то інколи їх можна виявити, опромінюючи хроматограму ультрафіолетовими променями. Виявити речовини на хроматограмах можна розрізавши хроматограму на смужки, а потім кожну смужку аналізують, змиваючи з неї речовин в розчин, який досліджують іншими хімічними чи фізико-хімічними методами.






