Задача 2.1. Обчислити внутрішню енергію одного кіломоля водню, взятого при температурі -23 °С.
Рішення. Внутрішня енергія одного кіломоля водню визначається за формулою 
де i = 5 число ступінейвільності двохатомної молекули;

Обчислення: 
Відповідь: 
Задача 2.2. Скільки тепла потрібно для нагрівання 10 г водню від 300 до 350 °С при сталому тиску?
Рішення. Кількість теплоти, що потрібна для нагрівання т грамів водню на (Т2 – T1) К при сталому тиску, визначається за формулою

Питома теплоємність при сталому тиску менша від молярної в М разів, тобто

Шукана кількість теплоти

Обчислення: 
Відповідь: 
 7280 Дж.
7280 Дж.
Задача 2.3. Визначити питомі теплоємності неону та водню при сталому об'ємі і тиску, якщо вважати, що ці гази ідеальні.
Рішення. Питомі теплоємностіідеальних газів визначаються за формулою
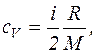

Для неону (одноатомний газ) і = 3, М= 20×10-3 кг/моль.
Підставляючи в останні формули значення величин, взятих в одиницях системи СІ, виконаємо обчислення:
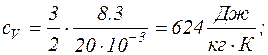

Для водню (двохатомний газ) і = 5, М = 2×10-3 кг/моль.

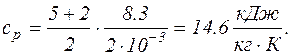
Відповідь: для неону: 

для водню: 

Задача 2.4. Визначити питому теплоємність при сталому об'ємі водню, 25% якого дисоційовані на атоми.
Рішення. Питома теплоємність суміші молекул та атомів водню обчислюється за правилом змішування з урахуванням вагового складу суміші
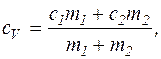
звідки

Визначимо питому теплоємність при сталому об'ємі с1 та с2 через молярні теплоємності та маси молей


а С1 та С2 - через ступені вільності та газову сталу, дістанемо: для молекулярного водню (двохатомного)

для атомарного водню (одновалентного)

Перевіримо одиницю виміру

Обчислення: 

Тоді
 .
.
Відповідь: 
Задача 2.5. Яка зовнішня робота буде виконана, якщо 200 г азоту нагріти від 20 до 100 °С при сталому тиску?
Рішення. При ізобарному нагріванні газу теплота 
 , передана газу, йде на збільшення його внутрішньої енергії
, передана газу, йде на збільшення його внутрішньої енергії  та на виконання роботи
та на виконання роботи  проти зовнішніх сил. На основі першого закону термодинаміки маємо
проти зовнішніх сил. На основі першого закону термодинаміки маємо
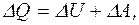
звідки 
Теплоту, передану газу, можна обчислити за формулою
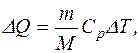
а зміну внутрішньої енергії - за формулою

тоді робота, виконана проти зовнішніх сил, дорівнює
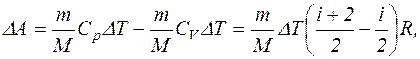
де М = 28×10-3 кг/моль - молярна маса азоту.
Перевіримо одиницю виміру

Обчислення: 
Відповідь: 
Задача 2.6. У скільки разів кінцевий тиск повітря, стисненого адіабатично, буде більшим від його тиску при ізотермічному стисненні, якщо об'єм повітря в обох випадках зменшується в 10 разів?
Рішення. Згідно з умовою задачі повітря в першому випадку стискається адіабатично, а в другому - ізотермічно. В обох випадках його початкові та кінцеві об'єми однакові, а відношення кінцевого об'єму до початкового дорівнює 10. Порівнявши тиски та об'єми повітря в обох процесах, ми знайдемо шукане відношення тисків. Позначивши початковий тиск повітря через r0, об'єм - через V0, кінцевий об'єм - через V1=0,1 V0 для обох процесів, кінцевий тиск у випадку адіабатичного процесу - через r1, ізотермічного – через r2, напишемо рівняння процесів:
адіабатичний процес

ізотермічний процес
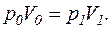
Замінивши V1 на 0,1V0 та поділивши перше рівняння на друге, дістанемо
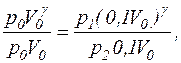
звідки знаходимо
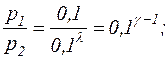

звідки

Тиск повітря при його адіабатичному стисненні виявився в 2,51 разів більшим його тиску при такому ж ізотермічному стисненні. Така зміна тиску пояснюється тим, що при адіабатичному стисненні газ нагрівається, у той час як при ізотермічному стисненні температура газу лишається сталою.
Відповідь: р1 = 2,51р2..
Задача 2.7. Азот при температурі t1 = 27 °С і тиску р =2 атм займав об'єм V1 = 4 л. Внаслідок адіабатичного розширення його температура знизилась до t2= 0 °С. Яку роботу виконав газ під час його розширення? Показник адіабати  = 1,4.
= 1,4.
Рішення За умовою задачі газ розширюється без теплообміну з оточуючим середовищем, а тому його температура повинна знизитися від початкової T1 до кінцевої Т2. Робота, виконана газом при адіабатичному розширенні, обчислюється за формулою

Оскільки в умові задачі дано об'єм газу, то число його кілограм-молей можна визначити з відношення об'єму газу за нормальних умов до об'єму одного моля газу теж за нормальних умов, тобто 
Знайдемо об'єм газу за нормальних умов

звідки
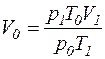
Підставляючи числові значення величин, взятих в одиницях системи СІ, та обчислюючи, одержимо

Число молів газу дорівнюватиме

Шукана робота дорівнює

Відповідь: А = - 174,1 Дж.
Задача 2.8. При ізотермічному розширенні 1 г водню його об'єм збільшився в три рази. Визначити роботу розширення газу, якщо його температура дорівнює 7 °С.
Рішення При ізотермічному розширенні газу його внутрішня енергія не змінюється, тобто  = 0. Згідно з першим законом термодинаміки
= 0. Згідно з першим законом термодинаміки
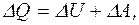
але, оскільки  = 0, то
= 0, то

а це визначає, що все передане газу тепло пішло на роботу проти зовнішніх сил.
Роботу ізотермічного розширення газу знаходять за формулою

Перевіримо одиницю виміру

Підставивши у формулу роботи числові значення величин, взятих в системі СІ та виконуючи обчислення, знаходимо

Відповідь: A= 1280 Дж.
Запитання для самоконтролю
1.Що називається ступенями вільності молекули та скільки їх мають одноатомні, двохатомні та багатоатомні молекули?
2. Як за питомою теплоємністю речовини визначити її молярну теплоємність?
3. Чому гази мають дві теплоємності: теплоємність при сталому тиску та теплоємність при сталому об'ємі?
4. У скільки разів теплоємність при сталому тиску більша теплоємності при сталому об'ємі?
Наскільки теплоємність газу при сталому тиску більша теплоємності при сталому об'ємі?
6. Який фізичний зміст газової сталої?
7. За якою формулою обчислюється робота ізотермічного розширення газу?
Який процес називається адіабатичним, яке його рівняння та графік?
9. Як обчислюється робота газу при його адіабатичному розширенні?
10. Як змінюється внутрішня енергія газу при його адіабатичному стисненні та розширенні?
11. Порівняти графіки ізотермічного та адіабатичного розширення та стиснення газу, а також пояснити їх.






