19.1. Написать уравнения реакций взаимодействия натрия с водородом, кислородом, азотом, серой. Какую степень окисления приобретают атомы окислителя в каждой из этих реакций?
19.2. Написать уравнения реакций взаимодействия с водой следующих соединений натрия: Na2O2, Na2S, NaH, Na3N.
19.3. Как получают металлический натрий? Составить уравнения процессов, происходящих на электродах при электролизе расплава NaCl.
19.4. Составить уравнения реакций получения гидрида, нитрида и карбида кальция и взаимодействия этих соединений с водой.
19.5. Закончить уравнения реакций: а) Li2O + CO2 = …;
б) Na2O2 + Na2SO3 + H2O = …; в) K2S + H2O ↔ …; г) NaCl + K[Sb(OH)6] = ….
19.6. Составить уравнения реакций, которые нужно провести для осуществления следующих превращений:
Са → СаН2 → Са(ОН)2 → СаСО3 → Са(НСО3)2.
19.7. Гидроксид какого из s -металлов проявляет амфотерные свойства? Составить молекулярные и ионные уравнения реакций взаимодействия этого гидроксида: а) с кислотой; б) со щелочью.
19.8. Составить уравнения реакций взаимодействия: а) бериллия с раствором щелочи; б) кальция с соляной кислотой; в) магния с концентрированной серной кислотой.
19.9. При сплавлении оксид бериллия взаимодействует с диоксидом кремния и с оксидом натрия. Написать уравнения соответствующих реакций. О каких свойствах ВеО свидетельствуют эти реакции?
19.10. Какая масса КОН образовалась у катода при электролизе раствора К2SO4, если на аноде выделилось 11,2 л О2 (условия нормальные)? (Ответ: 112 г).
19.11. Вычислить молярную концентрацию водного раствора КОН, полученного при растворении 1,5 г щелочи в 48,5 воды. Плотность раствора 1,027 г/мл.
(Ответ: 0,52 моль/л).
19.12. Вычислить энтальпию образования MgO, исходя из уравнения реакции MgO + C = Mg + CO, Δ H° = 491,3 кДж. (Δ fH° CO = –110,5 кДж/моль).
(Ответ: –601,8 кДж).
19.13. Вычислить количество теплоты, которое выделится при взаимодействии 8 г гидрида натрия с водой. Стандартные энтальпии образования NaH, NaOH, H2O (ж) принять соответственно равными –56,4; –425,6 и –285,8 кДж/моль. (Ответ: 27,8 кДж).
19.14. Каким объемом 35 %-го раствора КОН (ρ = 1,34 г/мл) можно заменить 10 л 4 н. раствора КОН? (Ответ: 4,78 л).
19.15. Закончить уравнения реакций: а) Na2O2 + KNО2 + H2SO4 = …;
б) L3N + H2O = …; в) K + O2 = …; г) CaCO3  ….
….
19.16. Написать уравнения реакций взаимодействия лития с водородом, кислородом, азотом, серой. Какую степень окисления приобретают атомы окислителя в каждой из этих реакций?
19.17. При электролизе водного раствора NaOH на аноде выделилось 2,8 л О2 (нормальные условия). Какой объем Н2 выделится на катоде? (Ответ: 5,6 л).
19.18. Вычислить Δ G° реакции горения магния в диоксиде углерода. Энергии Гиббса образования MgO, СО2, СО принять соответственно равными –569,6;
–394,4; –137,1 кДж/моль. Возможно ли самопроизвольное протекание этой реакции? (Ответ: –312,6 кДж).
19.19. Можно ли получить кальций восстановлением его оксида алюминием? Ответ обосновать расчетом энергии Гиббса реакции. Энергии Гиббса образования СаO и Al2O3 принять соответственно равными –604,2 и –1582 кДж/моль.
19.20. Закончить уравнения реакций: а) Be + KOH + H2O = …;
б) Li2C2 + H2O = …; в) Mg + H2O = …; г) Na2SO3 + H2O ↔ ….
Жесткость воды
Теоретическое введение
Жесткость воды обусловливается присутствием в ней солей кальция и магния. Различают временную (карбонатную) и постоянную (некарбонатную) жесткость. Временную жесткость придают воде гидрокарбонаты кальцияи магнияCa(HCO3)2, Mg(HCO3)2, постоянную − сульфаты и хлориды этих металлов CaSO4, MgSO4 и CaCl2, MgCl2 Сумма временной и постоянной жесткости составляет общую жесткость воды.
Жесткость воды выражается числом миллимолей эквивалентов ионовСа2+ и Мg2+, содержащихся в 1 л воды (ммоль/л). Один миллимоль эквивалентов жесткости отвечает содержанию 20,04 мг/л ионов кальция Са2+или 12,16 мг/л ионов магния Мg2+.
Для определения общей жесткости воды используется метод комплексонометрии. В основе этого метода лежит титрование воды раствором трилона Б в присутствии аммиачного буферного раствора и индикатора хромогена черного ЕТ-00 до перехода винно-красной окраски в синюю.
В присутствии ионов Са2 + и Мg2 + индикатор окрашивается в красный цвет, при отсутствии − в синий. При титровании жесткой воды раствором трилона Б происходит связывание ионов Са2+ и Мg2+, поэтому в конце титрования индикатор изменяет окраску и раствор становится синим.
Определение карбонатной жесткости воды сводится к определению концентрации гидрокарбонат-ионовНСО3‾ и, тем самым, эквивалентной этим ионам концентрации ионов жесткости Са2+ и Мg2+. Анализ проводят методом нейтрализации. В основе этого метода лежит титрование воды в присутствии метилоранжа раствором соляной кислоты до перехода желтой окраски индикатора в оранжевую.
Анион НСО3‾вводе гидролизуется: НСО3‾ + Н2О ↔ Н2СО3 + ОН‾,
поэтому вода имеет щелочную реакцию среды и метилоранж в ней окрашен в желтый цвет. При титровании раствором HCl такой воды протекает реакция нейтрализации: ОН‾ + Н+ ↔ Н2О.
Ионы Н+ нейтрализуют количество ионов ОН ‾, эквивалентное концентрации ионов НСО3‾.
Анализ воды на жесткость предполагает обычно:
1) определение общей жесткости Жо;
2) определение карбонатной жесткости Жк;
3) вычисление некарбонатной жесткости Жнк = Жо – Жк.
Примеры решения задач
Пример 20. 1. Вычислить жесткость воды, зная, что в 500 л ее содержится 202,5 г Ca(HCO3)2.
Решение. Для решения задачи воспользуемся формулой
 .
.
М эк (Ca(HCO3)2) = 162/2 = 81 г/моль.
Ж = 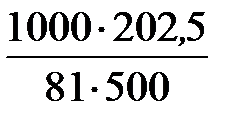 = 5 ммоль/л.
= 5 ммоль/л.
Пример 20. 2. Вычислить карбонатную жесткость воды, зная, что на титрование 100 мл этой воды, содержащей гидрокарбонат кальция, потребовалось 6,25 мл 0,08 н. раствора НCl.
Решение. Вычисляем нормальность раствора гидрокарбоната кальция. Так как вещества взаимодействуют между собой в эквивалентных количествах, то можно написать V A ∙ с эк·(А) = V B ∙ с эк(B),
6,25∙0,08 = 100∙ с эк · (Ca(HCO3)2),
отсюда (Ca(HCO3)2) =  0,005 г/моль.
0,005 г/моль.
Таким образом, в 1 л исследуемой воды содержится 0,005∙1000 = 5 ммоль гидрокарбоната кальция или 5 ммоль ионов Са2+. Карбонатная жесткость воды равна 5 ммоль/л.
Пример 20. 3. Сколько граммов CaSO4 содержится в 1 м3 воды, если жесткость, обусловленная присутствием этой соли, равна 4 ммоль/л?
Решение. Из формулы  находим
находим
 272 г,
272 г,
где 68 г/моль – М эк (CaSO4), найденная по формуле
 ,
,
где М – молярная масса соли, г/моль; n – число ионов металла, участвующих в реакции от каждой молекулы; |c.o. | – абсолютное значение степени окисления иона металла.
М эк(CaSO4) =  = 68 г/моль.
= 68 г/моль.
Пример 20. 4. Какую массу соды Na2CO3 надо добавить к 500 л воды, чтобы устранить ее жесткость, равную 5 ммоль/л?
Решение. В 500 л воды содержится 500 ∙ 5 = 2500 ммоль солей, обусловливающих жесткость воды. Для устранения жесткости следует прибавить 2500∙53 = 132500 мг = 132,5 г соды. (53 г/моль – молярная масса эквивалентов соды Na2CO3).






