15.1. а). Чему равна величина ЭДС гальванического элемента, составленного из стандартных цинкового и серебряного электродов, погруженных в растворы их солей? Привести схему гальванического элемента и реакции, протекающие на электродах при его работе. (Ответ: 1,562 В).
б ). Возможна ли электрохимическая коррозия алюминия, контактирующего со свинцом в нейтральном водном растворе, содержащем растворенный кислород? Если да, то написать уравнения реакций анодного и катодного процессов. Составить схему образующегося гальванического элемента.
15.2. а). Чему равна величина ЭДС цинкового концентрационного элемента, составленного из двух цинковых электродов, опущенных в растворы с концентрациями ионов Zn2+, равными 10–2 и 10–6 моль/л? Привести схему такого элемента и реакции, протекающие на электродах при его работе.
(Ответ: 0,118 В).
б). Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытия? Составить уравнения анодного и катодного процессов. Привести схемы образующихся гальванических элементов.
15.3. а). Имеется гальванический элемент, в котором протекает токообразующая реакция Ni + Cu2+ = Cu + Ni2+. Привести схему такого элемента, написать уравнения электродных процессов.
б). Изделие из алюминия склепано с медью. Какой из металлов будет подвергаться коррозии, если эти металлы попадут в кислую среду (HCl)? Составить уравнения происходящих при этом процессов, привести схему образующегося гальванического элемента. Определить продукты коррозии.
15.4. а). Составить схему, написать уравнения токообразующей и электродных реакций для гальванического элемента, у которого один из электродов кобальтовый (СCо2+ = 10–1 моль/л), а другой – стандартный водородный. Рассчитать ЭДС элемента при 298 К. Как изменится ЭДС, если концентрация ионов Со2+ уменьшить в 10 раз? (Ответ: 0,307 В; 0,336 В).
б ). Составить уравнения анодного и катодного процессов при коррозии пары магний – свинец в кислой среде и во влажном воздухе. Какие продукты коррозии образуются в первом и во втором случаях?
15.5. а).Каково значение ЭДС элемента, состоящего из медного и свинцового электродов, погруженных в растворы солей этих металлов с концентрациями их ионов 1 моль/л? Изменится или нет ЭДС этого элемента и почему, если концентрации ионов металлов будут составлять 0,001 моль/л? Составить уравнения электродных и токообразующей реакций. Привести схему гальванического элемента. (Ответ: 0,463 В).
б). Привести по одному примеру катодного и анодного покрытия для кобальта. Составить уравнения катодных и анодных процессов во влажном воздухе и в растворе соляной кислоты при нарушении целостности покрытия.
15.6. а). Составить схему, привести уравнения электродных процессов и вычислить ЭДС концентрационного гальванического элемента, состоящего из медных электродов, опущенных в растворы СuSO4 с концентрациями 0,01 и 0,1 моль/л. (Ответ: 0,0295 В).
б ). К какому типу покрытий относятся олово на меди и на железе? Какие процессы будут протекать при атмосферной коррозии указанных пар в нейтральной среде? Написатьуравнения катодных и анодных реакций.
15.7. а ). После нахождения в растворах каких из приведенных солей масса кадмиевой пластинки увеличится или уменьшится: а) MgCl2; б) Hg(NO3)2; в) CuSO4; г) AgNO3; д) CaCl2? Ответ обосновать.
б). Медное изделие покрыли серебром. К какому типу относится такое покрытие – к анодному или катодному? Составить уравнения электродных процессов коррозии этого изделия при нарушении целостности покрытия во влажном воздухе и в растворе соляной кислоты. Привести схемы образующихся при этом гальванических элементов.
15.8. а). Составить схему, привести уравнения электродных процессов и вычислить ЭДС гальванического элемента, состоящего из свинцовой и магниевой пластин, которые опущены в растворы своих солей с концентрацией ионов Pb2+ и Mg2+, равных 1 моль/л. Изменится ли значение ЭДС, если концентрацию каждого из ионов понизить в 100 раз? Ответ обосновать. (Ответ: 2,237 В).
б). В воду, содержащую растворенный кислород, опустили никелевую пластинку и никелевую пластинку, частично покрытую медью. В каком случае процесс коррозии никеля происходит интенсивнее? Почему? Составить уравнения анодного и катодного процессов для пластинки покрытой медью.
15.9. а).В два сосуда с голубым раствором сульфата меди поместили в первый хромовую пластинку, а во второй платиновую. В каком сосуде цвет раствора постепенно исчезает? Почему? Составить электронные и молекулярные уравнения соответствующих реакций.
б). Какой металл целесообразнее выбрать для протекторной защиты железного изделия: цинк, никель или кобальт? Почему? Составить уравнения анодного и катодного процессов атмосферной коррозии таких изделий. Каков состав продуктов коррозии?
15.10. а). Составить схемы двух гальванических элементов, в одном из которых оловянная пластинка была бы катодом, а в другом анодом. Написать для каждого из этих элементов уравнения электродных (катодных и анодных) процессов и токообразующих реакций.
б). Железо покрыто хромом. Какой из металлов будет корродировать в случае нарушения поверхностного слоя покрытия при атмосферной коррозии? Какое это покрытие катодное или анодное? Составить схему процессов, происходящих на электродах образующегося гальванического элемента.
15.11. а). Составить схему гальванического элемента, в основе работы которого лежит реакция: Ni + Pb(NO3)2 = Ni(NO3)2 + Pb. Написать уравнения электродных (катодных и анодных) процессов. Вычислить ЭДС этого элемента, если С Ni2 + = 0,01 моль/л, а С Pb2 + = 0,0001 моль/л. (Ответ: 0,065 В).
б). Рассчитать энергию Гиббса реакции 2Ме + 2Н2О (ж) + О2 = 2Ме(ОН)2
и определить, какой из металлов – магний или медь, интенсивнее будет корродировать во влажном воздухе. Стандартные энергии Гиббса образования D¦ G° Mg(OH)2, Cu(OH)2, H2O (ж) соответственно равны –833,7;
–356,9; –237,3 кДж/моль.
15.12. а). Вычислить электродный потенциал цинка в растворе ZnCl2, в котором концентрация Zn2+ составляет 0,1 моль/л. Как изменится значение потенциала при разбавлении раствора в 100 раз? (Ответ: –0,79 В; –0,85 В).
б). Какой из металлов – алюминий или золото, будет подвергаться коррозии во влажном воздухе по уравнению: 4Ме + 6Н2О (ж) + 3О2 = 4Ме(ОН)3.
Ответ обосновать, рассчитав энергию Гиббса реакции. Стандартные энергии Гиббса образования D¦ G° Al(OH)3, Au(OH)3, H2O (ж) соответственно равны
–1139,7; –289,9; –237,3 кДж/моль.
15.13. а). Составить схему гальванического элемента, электродами в котором служат пластинки из олова и меди. Исходя из величин стандартных электродных потенциалов, рассчитать значения Е° и D G°. Определить направление протекания токообразующей реакции. (Ответ: 0,473 В; –91,3 кДж).
б ). Какие из перечисленных металлов могут быть использованы для протекторной защиты железного изделия в присутствии электролита, содержащего растворенный кислород в нейтральной среде: алюминий, хром, серебро, кадмий? Привести уравнения анодного и катодного процессов атмосферной коррозии таких изделий. Каков состав продуктов коррозии?
15.14. а). Составить схему гальванического элемента, образованного железом и свинцом, погруженными в растворы их солей с концентрациями ионов металлов 0,01 моль/л. Привести уравнения токообразующих реакций и электродных процессов. Рассчитать ЭДС. (Ответ: 0,314 В).
б). Изделие из хрома спаяно свинцом. Какой из металлов будет корродировать при попадании такого изделия в кислотную среду (HCl)? Привести уравнения анодного и катодного процессов и образующиеся продукты коррозии.
15.15. а). Исходя из величин стандартных электродных потенциалов, рассчитать значения ЭДС и D G ° и определить, будет ли работать гальванический элемент, в котором на электродах протекают реакции:
Hg0 – 2ē = Hg2+,
Pb2+ + 2ē = Pb0.
(Ответ: –0,98 В; +189,1 кДж).
б). Составить уравнения анодного и катодного процессов, происходящих при коррозии железа, покрытого серебром, во влажном воздухе и в кислой среде. Определить тип покрытия – анодное или катодное? Какие продукты образуются в результате коррозии?
15.16. а). Исходя из величин стандартных электродных потенциалов, рассчитать значения ЭДС и D G° и сделать вывод о возможности протекания реакции Cu + 2Ag+ 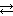 Cu2+ + 2Ag в прямом направлении.
Cu2+ + 2Ag в прямом направлении.
(Ответ: 0,462 В; –89,2 кДж).
б). Какие металлы могут быть использованы в качестве анодного покрытия сплава Zn – Cd? Привести уравнения анодного и катодного процессов при коррозии такого сплава во влажном воздухе в отсутствие анодного покрытия.
15.17. а). Как изменится масса хромовой пластинки после нахождения в растворах солей: а) CuSO4; б) MgCl2; в) AgNO3; г) CaCl2? Ответ обосновать.
б). Привести уравнения анодного и катодного процессов при коррозии сплава Fe – Sn во влажном воздухе и в кислой среде. Определить продукты коррозии.
15.18. а). Составить схемы двух гальванических элементов, в одном из которых цинк – отрицательный электрод, а в другом – положительный. Привести уравнения токообразующих реакций и электродных процессов.
б). Привести уравнения анодного и катодного процессов, происходящих при коррозии сплава Al – Ni в атмосфере влажного воздуха и в кислой среде (НС1). Определить продукты коррозии.
15.19. а). Электродные потенциалы железа и серебра соответственно равны –0,44 и +0,799 В. Какая реакция самопроизвольно протекает в железо-серебряном гальваническом элементе
Fe0 + 2Ag+ = Fe2+ + 2Ag0 или 2Ag0 + Fe2+ = Fe0 + 2Ag+?
Ответ обосновать, рассчитав энергию Гиббса каждой из приведенных реакций.
б). Хромовую пластинку и пластинку из хрома, частично покрытую серебром, поместили в раствор соляной кислоты. В каком случае процесс коррозии хрома протекает более интенсивно? Почему? Привести уравнения соответствующих процессов.
15.20. а). Вычислить ЭДС гальванического элемента, состоящего из водородного электрода, опущенного в чистую воду, и оловянного электрода, опущенного в раствор с концентрацией ионов олова (II) 1 моль/л. (Ответ: 0,16 В).
б). Составить уравнения самопроизвольно протекающих реакций при атмосферной коррозии цинка и олова, находящихся в контакте. Привести схему образующегося гальванического элемента.
Электролиз
Теоретическое введение
Электролизом называется совокупность процессов, протекающих при прохождении постоянного электрического тока через электрохимическую систему, состоящую из двух электродов и расплава или раствора электролита.
Если в раствор электролита погрузить электроды и подключить их к внешнему источнику постоянного тока, то ионы в растворе получают направленное движение. К аноду (положительному электроду) движутся анионы (кислотные остатки, OH−). К катоду (отрицательному электроду) движутся катионы (Мn+, H+). Достигнув электродов, ионы разряжаются: у анода восстановитель отдает электроны (в сеть) и окисляется; у катода окислитель присоединяет электроны (из сети) и восстанавливается.
При электролизе водных растворов, кроме ионов электролита в окислительно-восстановительном процессе принимают участие молекулы воды. Молекулы воды сильно полярны и поэтому притягиваются и к катоду и к аноду. На катоде молекулы воды могут восстанавливаться:
2Н2О + 2ē = Н2 + 2ОН– (j = –0,41 В),
а на аноде – окисляться:
2Н2О – 4ē = 4Н+ + О2 (j = +1,23 В).
Характер катодного процесса при электролизе водных растворов определяется величиной стандартного электродного потенциала металла. На катоде в первую очередь восстанавливаются катионы, имеющие наибольшее значение электродного потенциала. Если катионом электролита является металл, электродный потенциал которого значительно более отрицательный, чем –0,41 В, то на катоде металл восстанавливаться не будет, а произойдет восстановление молекул воды. Эти металлы расположены в ряду напряжений от Li по Al включительно. Если катионом электролита является металл, электродный потенциал которого значительно положительнее, чем –0,41 В, то из нейтрального раствора такого электролита на катоде будет восстанавливаться металл. Такие металлы находятся в ряду напряжений вблизи водорода (примерно от олова и после него). В случае ионов металлов, имеющих значения потенциала близкие к –0,41 В (Zn, Cr, Fe, Cd, Ni), в зависимости от концентрации электролита и условий электролиза, возможно как восстановление металла, так и выделение водорода, а нередко и их совместный разряд.
На аноде в первую очередь окисляются анионы с наименьшим значением электродного потенциала. Различают электролиз с нерастворимым (инертным) и растворимым (активным) анодами. Инертным называется анод, материал которого в ходе электролиза не окисляется (графит, уголь, платина). Активным называется анод, материал которого может окисляться в ходе электролиза.
На инертном аноде при электролизе водных растворов щелочей, растворов электролитов с кислородсодержащими анионами (SO42−, PO43−, NO3‾), а также фторид-ионами F‾ на аноде происходит электрохимическое окисление воды:
2H2O − 4ē → 4H+ + O2.
Если анионы электролита бескислородны (Cl‾, Br‾, I‾, S2−), то они и разряжаются на аноде в ходе электролиза.
Активный (растворимый) анод при электролизе окисляется – переходит в раствор в виде ионов.
Рассмотрим несколько случаев электролиза водных растворов солей.
Э л е к т р о л и з р а с т в о р а CuCl2 c и н е р т н ы м а н о д о м
Электродный потенциал меди (+0,337 В) значительно больше потенциала восстановления ионов водорода из воды (–0,41 В). Поэтому на катоде происходит процесс восстановления ионов Cu2+. У анода будут окисляться хлорид-ионы.
Схема электролиза раствора хлорида меди (II)
CuCl2 = Cu2+ + 2Cl‾
Катод (−) ← Cu2+, H2O Анод (+) ← Cl‾, H2O
Cu2+ + 2ē → Cu0 2Cl‾ − 2ē → Cl2
Суммарное уравнение реакции, протекающей при электролизе, имеет вид:
CuCl2 → Cu + Cl2.
Продукты электролиза – Cu и Cl2.
Э л е к т р о л и з р а с т в о р а KNO3 с и н е р т н ы м а н о д о м
Электродный потенциал калия (−2,924 В) значительно меньше потенциала восстановления ионов водорода из воды (–0,41 В), поэтому катионы K+ не будут восстанавливаться на катоде. Кислородсодержащие анионы NO3‾ не будут окисляться на аноде. В этом случае на катоде и аноде восстанавливаются и окисляются молекулы воды. При этом в катодном пространстве будут накапливаться ионы OH‾, образующие с ионами K+ щелочь KOH, а в анодном пространстве накапливаются ионы H+, образующие с ионами NO3‾ кислоту HNO3.
Схема электролиза раствора нитрата калия
KNO3 = K+ + NO3‾
Катод (−) ← K+, H2O Анод (+) ← NO3‾, H2O
2H2O + 2ē → H2 + 2OH‾; 2H2O − 4ē → O2 + 4H+;
у катода 2K+ + 2OH‾ → 2KOH; у анода 2H+ + 2NO3‾ → 2HNO3.
Суммарное уравнение реакции электролиза раствора KNO3
2KNO3 + 4H2O → 2H2 + О2 + 2КОН + 2HNO3.
Продукты электролиза – Н2 и О2. У катода образуется щелочь КОН
(рН > 7); у анода − кислота HNO3 и рН < 7.
Э л е к т р о л и з р а с т в о р а NiSO4 с н и к е л е в ы м а н о д о м
В этом случае сам анод окисляется, а на катоде восстанавливаются ионы никеля.
Схема электролиза раствора сульфата никеля
Катод (−) ← Ni2+, H2O Анод никелевый ← SO42−, H2O
Ni2+ + 2ē → Ni0 Ni0 – 2ē → Ni2+
Примеры решения задач
Пример 16.1. Сколько граммов никеля выделится на катоде при пропускании через раствор сернокислого никеля NiSO4 тока силой 5 А в течение 10 мин? Привести схемы электродных процессов, протекающих при электролизе с инертным анодом. Определить продукты электролиза.
Решение. В водном растворе сульфат никеля (II) диссоциирует:
NiSO4 = Ni2+ + SO42–. Стандартный электродный потенциал никеля (–0,250 В) выше значения потенциала восстановления ионов водорода из воды (–0,41 В). Поэтому на катоде будет происходить разряд ионов Ni2+ и выделение металлического никеля. При электролизе сернокислых солей на инертном аноде происходит электрохимическое окисление воды с выделением кислорода.
Катод (−) Ni2+, Н2О Анод (+) SO42–, Н2О
Ni2+ + 2ē = Ni2Н2О – 4ē = 4Н+ + О2;
у анода 4Н+ + 2SO42– = 2Н2SO4.
Продукты электролиза – Ni и О2.
Масса вещества, выделившегося на электроде при электролизе, определяется по законам Фарадея, математическое выражение которых имеет вид
 , (1)
, (1)
где m – масса вещества, выделившегося на электроде, г; М эк – молярная масса эквивалентов этого вещества, г/моль; Q – количество электричества, прошедшего через электролит, Кл; F – постоянная Фарадея, равная 96500 Кл/(моль∙экв).
Q = I∙t, где I – сила тока, А; t – время, электролиза, с. Подставляя в формулу (1) вместо Q его значение, получаем  (2).
(2).
Молярная масса эквивалентов никеля (молярная масса атомов никеля – 58,71 г/моль) равняется 58,71/2 = 29,36 г/моль. Подставляя это значение, а также силу тока и время электролиза (в секундах) в формулу (2), получаем искомую массу никеля: m = (29,36×5×600)/96500 = 0,91 г.
Пример 16.2. Сколько времени нужно пропускать через раствор кислоты ток силой 10 А, чтобы получить 5,6 л водорода при нормальных условиях?
Решение. Продукт электролиза представляет собой газообразное вещество, поэтому для решения воспользуемся уравнением
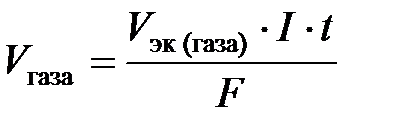 .
.
Так как 1 моль эквивалентов водорода занимает при нормальных условиях объем 11,2 л, то искомое количество времени прохождения тока 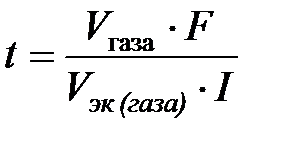
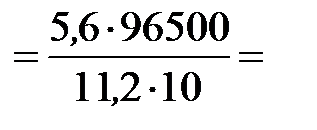 4825 c =1ч 20мин 25 с.
4825 c =1ч 20мин 25 с.
Пример 16.3. При проведении электролиза водного раствора хлорида двухвалентного металла затрачено 3561 Кл электричества. В результате процесса на катоде выделилось 2,19 г этого металла. Определить металл, водный раствор хлорида которого подвергли электролизу. Привести схему электродных процессов. Определить продукты электролиза.
Решение. Находим молярную массу эквивалентов металла: М эк 
 = 59,347 г/моль. Умножая эту величину на 2 (валентность металла) получаем 118,69 г/моль, что соответствует молярной массе атомов олова. Следовательно, электролизу подвергли раствор SnCl2. В водном растворе хлорид олова (II) диссоциирует: SnС12 = Sn2+ + 2С1–. Стандартный электродный потенциал олова (II) (–0,136 В) существенно выше значения потенциала восстановления ионов водорода из воды (–0,41 В). Поэтому на катоде будет происходить разряд ионов Sn2+ и выделение металлического олова. На аноде будут окисляться анионы хлора.
= 59,347 г/моль. Умножая эту величину на 2 (валентность металла) получаем 118,69 г/моль, что соответствует молярной массе атомов олова. Следовательно, электролизу подвергли раствор SnCl2. В водном растворе хлорид олова (II) диссоциирует: SnС12 = Sn2+ + 2С1–. Стандартный электродный потенциал олова (II) (–0,136 В) существенно выше значения потенциала восстановления ионов водорода из воды (–0,41 В). Поэтому на катоде будет происходить разряд ионов Sn2+ и выделение металлического олова. На аноде будут окисляться анионы хлора.
Катод (−) Sn2+, Н2О Анод (+) Сl–, Н2О
Sn2+ + 2ē = Sn 2Сl− – 2ē = С12.
Продукты электролиза – Sn и С12.
Пример 16.4. При электролизе раствора CuSO4 на угольном аноде выделилось 350 мл кислорода при нормальных условиях. Сколько граммов меди выделилось на катоде? Привести уравнения электродных процессов, определить продукты электролиза.
Решение. В водном растворе сульфат меди (II) диссоциирует по схеме: CuSO4 = Cu2+ + SO42−. Электродный потенциал меди (+0,337 В) значительно больше потенциала восстановления ионов водорода из воды (–0,41 В). Поэтому на катоде происходит процесс восстановления ионов Cu2+. При электролизе водных растворов сульфат-анионы не окисляются на аноде. На нем происходит окисление воды.
Катод (−) Cu2+, Н2О Анод (+) SO42–, Н2О
Cu2+ + 2ē = Сu 2Н2О – 4ē = 4Н+ + О2;
у анода 4Н+ + 2SO42– = 2Н2SO4.
Продукты электролиза – Сu и О2.
Один моль эквивалентов кислорода при нормальных условиях занимает объем 5,6 л. Следовательно, 350 мл составляют 0,35/5,6 = 0,0625 моль. Столько же молей эквивалентов выделилось на катоде. Отсюда масса меди
m = 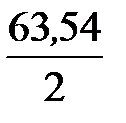 × 0,0625 = 1,98 г.
× 0,0625 = 1,98 г.
Пример 16.5. Будут ли, и в какой последовательности, восстанавливаться на катоде одновременно присутствующие в растворе (в равных концентрациях) ионы А13+, Ni2+, Sn2+, Au3+ и Mg2+? Напряжение достаточно для выделения любого металла.
Решение. На катоде сначала восстанавливаются катионы, имеющие большее значение электродного потенциала (табл. Б. 4). Поэтому, в первую очередь, на катоде будут восстанавливаться ионы Au3+ (+1,498 В), далее Sn2+ (–0,136 В) и, наконец, Ni2+ (–0,250 В). Ионы А13+ (–1,662 В) и Mg2+ (–2,363 В), имеющие значения электродного потенциала значительно отрицательнее потенциала восстановления ионов Н+ из воды (–0,41 В), при электролизе водных растворов не восстанавливаются на катоде. При электролизе их солей протекает восстановление молекул воды:
2Н2О + 2ē = Н2 + 2ОН–.






