зростання електронегативності: зростання електронегативності:
| А | Б | В | Г | Д | |
| А | Б | В | Г | Д | |
А)В; а) В;
Б) С; б) In;
В) Ве; в) Al;
Г) Li; г) Tl.
Д) F. д) Ga.
Розташуйте елементи в порядку 6. Розташуйте елементи в порядку
зростання валентності: зменшення валентності:
| А | Б | В | Г | Д | |
| А | Б | В | Г | Д | |
А) S; а) Cl;
Б) Si; б) S;
В) P; в) Al;
Г) Na; г) Na.
Д) Mg. д) Mg.
Вправа на повторення:
7. Скільки з наведених нижче речовин можуть реагувати з сульфатною кислотою: карбон (IV) оксид, купрум(ІІ) гідроксид, цинк:
а) одна; б) дві; в) три; г) чотири. Напишіть відповідні рівняння реакцій.
 Урок № 37 Взаємозв’язок між розміщення елементів у періодичній системі та властивостями хімічних елементів, простих речовин, сполук елементів з Гідрогеном та Оксигеном.
Урок № 37 Взаємозв’язок між розміщення елементів у періодичній системі та властивостями хімічних елементів, простих речовин, сполук елементів з Гідрогеном та Оксигеном.
Розташуйте елементи в порядку 2. Розташуйте елементи в порядку
зменшення металічних зменшення металічних
| А | Б | В | Г | Д | |
властивостей: властивостей:
| А | Б | В | Г | Д | |
А) Ba; а) Na;
Б) Ca; б) Mg;
В) Ве; в) Al;
Г) Mg; г) P;
Д) Sr. д) Si.
Розташуйте елементи в порядку 4. Розташуйте елементи в порядку
зменшення неметалічних властивостей: зменшення неметалічних властивостей:
| А | Б | В | Г | Д | |
| А | Б | В | Г | Д | |
А) B; а) Si
Б) C; б) C;
В) O; в) Ge;
Г) N; г) Sn;
Д) F. д) Pb.
Розташуйте елементи в порядку 6. Розташуйте елементи в порядку
зменшення основних властивостей: збільшення основних властивостей:
| А | Б | В | Г | Д | |
| А | Б | В | Г | Д | |
А) К; а) B
Б) Ca; б) Tl;
В) Ti; в) Al;
Г) Sc; г) In;
Д) V. д) Ga.
Розташуйте елементи в порядку 8. Розташуйте елементи в порядку
зменшення кислотних властивостей: збільшення кислотних властивостей:
| А | Б | В | Г | Д | |
| А | Б | В | Г | Д | |
А) Ba; а) Na
Б) Ca; б) Mg;
В) Ве; в) Al;
Г) Mg; г) P.
Д) Sr. д) Si.
| А | Б | В | Г | |
 Вправа на повторення:
Вправа на повторення:
9. Встановіть послідовність розміщення формул відповідно до схеми перетворень
кислотний оксид → кислота → сіль → основа:
а) FeSO4; б) SO3; в) Fe(OH)2; г) H2SO4.
 Урок № 38 Характеристика хімічних елементів малих періодів за їх місцем у періодичній системі та будовою атома.
Урок № 38 Характеристика хімічних елементів малих періодів за їх місцем у періодичній системі та будовою атома.
1. За планом характеристики хімічних елементів охарактеризуйте Натрій:
І. Положення в періодичній системі:
а) номер періоду________; б) номер групи __________;
В) головна чи побічна підгрупа (правильну відповідь підкресліть).
ІІ. Будова атому: а) заряд ядра_________;
б) кількість протонів, електронів, нейтронів ___________________________________;
в) кількість енергетичних рівнів ________; г) електронна формула __________________.
ІІІ. Характер елемента та його сполук:
а) відноситься до металічних чи неметалічних (правильну відповідь підкресліть);
б) характер оксиду – основний чи кислотний (правильну відповідь підкресліть);
в) характер гідроксиду - основа чи кислота (правильну відповідь підкресліть).
IV Порівняння з сусідами по періоду і групі:
А) порівняння з сусідами по періоду: ___________________________________________;
Б) порівняння з сусідами по групі: _____________________________________________.
| А | Б | В | Г | |
2. Встановіть відповідність між фрагментом періодичної системи та сукупністю елементів:
Фрагмент періодичної системи: Сукупність елементів:
а) головна підгрупа І групи; 1) Mg – Sr;
б) головна підгрупа ІІ групи; 2) Li – K;
в) головна підгрупа ІV групи; 3) S – Te;
г) головна підгрупа VІ групи; 4) Zn – Hg:
5) C – Sn
3. Заповніть пропуски в формулі електронної облонки атому Магнію, закінчить графічну та електронну формули:




 Mg
Mg
_e _e _e
формула електронної оболонки
________________
графічна формула електронна формула
4. Закінчити рівняння хімічних реакцій:
а) стронцій гідроксид + селенатна кислота;_____________________________________
б) кадмій оксид + нітратна кислота;____________________________________________
в) калій гідроксид + арсен(V) оксид; ____________________________________________
г) літій + вода;_____________________________________________________________


Вправа на повторення
5. Здійснити перетворення речовин: К 1→ КОН 2→ Cr(OH)3 3→ Cr2(SO4)3
 Урок № 39 Узагальнюючий урок
Урок № 39 Узагальнюючий урок
1. Встановіть характеристику елементу R, який утворює сполуку ROH:
а) розташований у І групі головній підгрупі;
 б) розташований в ІV групі головній підгрупі;
б) розташований в ІV групі головній підгрупі;
в) має електронну формулу атому 1s22s22p4;
г) є неметалічним елементом.
2. Встановіть відповідність між електронною формулою та атомом елемента:
Електронна формула: Атом елемента:
а) 1s22s22p3; 1. Al;
б) 1s22s22p6; 2. Mg;
в) 1s22s22p63s1; 3. N;
г) 1s22s22p63s23p1; 4. Na;
Ne.
3. Складіть формули речовин, до складу яких входять:
А) 1s22s22p63s1 i 1s22s22p63s23p4__________________;
Б) № 19 і № 8 __________________;
В) елемент ІІ групи головної підгрупи ІV періоду і елемент VІІ групи головної підгрупи ІV періоду_______________________;
Г) загальну формулу оксиду, утвореного елементами V групи________________.
| А | Б | В | Г | |
4. Встановіть послідовність зростання атомного радіуса в ряду елементів:
А) S;
Б) P;
В) Cl;
Г) Si.
5. Здійснити перетворення речовин: Zn 1→ ZnO 2→ ZnSO4 3→Zn(OH)2 4→ Na2ZnO2
6. При взаємодії 12,4 г оксиду одновалентного металу з водою добуто 16 г його гідроксиду. Визначте метал.
 Урок № 40 Електронна природа хімічного зв’язку. Поняття про електронегативність елементів.
Урок № 40 Електронна природа хімічного зв’язку. Поняття про електронегативність елементів.
1. Що енергетично вигідніше – віддати чи приєднати електрони з метою досягнення вісьмиелектронного октету для атому (заповніть пропуски):




 а) Li Li+
а) Li Li+
+ ______ →
__e __ e ___e





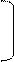

 1s22s1 1s2
1s22s1 1s2
Б)
S _____→ S
__e __e__e __e __e__e
_____________ _____________
 | |||||
 |  |


 в)
в)
Mg _____ → Mg
__e__e__e __e__e
_____________ _____________
 | |||||||||||
 |  |  |  |  |
 г)
г)
Cl ______ → Cl
__e__e__e __e __e__e
_____________ _____________
2. Встановіть послідовність зростання 3. Встановіть послідовність зростання
електронегативності у елементів: електронегативності у елементів:
| А | Б | В | Г | |
| А | Б | В | Г | |
А) I; а) Сl;
Б) Cl; б) S;
В) Br; в) Na;
Г) F. г) Mg.
4. Встановіть послідовність зменшення 5. Встановіть послідовність зменшення
електронегативності у елементів: електронегативності у елементів:
| А | Б | В | Г | |
| А | Б | В | Г | |
А) Te; а) Li;
Б) O; б) B;
В) S; в) F;
Г) Se. г) Be.
 Вправа на повторення
Вправа на повторення
6.Заповніть таблицю:
| Назва Речовини | Формула речовини | М, г/моль | N | m, г | υ, моль |
| Кальцій гідроксид | _______ | _____ | 0,6 *1023 | ||
| Ортофосфатна кислота | _______ | _____ | 0,2 |
 Урок № 41Ковалентний зв’язок, його види – полярний і неполярний.
Урок № 41Ковалентний зв’язок, його види – полярний і неполярний.
| А | Б | В | Г |
1. Виберіть твердження щодо ковалентного неполярного зв’язку;
а) ґрунтується на електростатичному механізмі;
б) зв'язок утворюється за рахунок спільної електронної пари;
в) спільна електронна пара зміщена до одного з елементів;
г) спільна електронна пара симетрична відносно обох атомів.
2.Виберіть твердження щодо ковалентного полярного зв’язку;
| А | Б | В | Г |
а) ґрунтується на електростатичному механізмі;
б) зв'язок утворюється за рахунок спільної електронної пари;
в) спільна електронна пара зміщена до одного з елементів;
г) спільна електронна пара симетрична відносно обох атомів.
3. Виберіть рядок, в якому в перелічені 4. Виберіть рядок, в якому в перелічені
сполуки з ковалентним полярним типом зв’язку; сполуки з ковалентним неполярним
типом зв’язку; типом зв’язку;
| А | Б | В |
| А | Б | В |
а) PН3, NH3, CO2, SO2; а) MgBr2, BaO, CuCl2;
б) NaCl, CaCl2, CaO, K2S; б) F2, Br2, I2;
в) N2,Cl2, H2, O2. в) H2O, CH4, Cl2O7.
5. Намалюйте схему утворення молекули Cl2. 6. Намалюйте схему утворення молекули CO2

Вправи на повторення
7. Яка маса солі утвориться при взаємодії
216 г натрій карбонату з хлоридною кислотою?
8. Встановіть відповідність між хімічним елементом та його електронною формулою:
| А | Б | В | Г | |
Хімічний елемент: Електронна формула:
а) S; 1. 1s22s22p3;
б) Ca; 2. 1s22s2;
в) Be; 3. 1s22s22p63s23p4;
г) N; 4. 1s22s22p63s23p64s2.
 Урок № 42 Йонний звязок
Урок № 42 Йонний звязок
1. «Хрестики – нулики»
а) закресліть ряд, в якому б) закресліть ряд, в якому
записані формули речовин, записані формули речовин
| Li2О | N2 | CaСl2 |
| BCl3 | O2 | I2 |
| BaS | Br2 | CO2 |
утворені ковалентним неполярним утворені ковалентним полярним
зв’язком: зв’язком:
| CO2 | N2 | Na3P |
| B2O3 | NO | FeS |
| BaO | Ar | PCl5 |
в) закресліть ряд, в якому записані формули речовин,
утворені йонним зв’язком:
| H2 | SO3 | N2O5 |
| KCl | Na2O | MgS |
| F2 | Cl2 | Br2 |
2. Закінчить речення:
а) ковалентний неполярний зв’язок утворюєься___________________________________
________;
б) ковалентний полярний зв’язок утворюється ___________________________________
________;
в) йонний звязок утворюється ________________________________________________
________.
3. Намалюйте схему утворення молекули О2. 4. Намалюйте схему утворення молекули CO.






