Классификация сложных неорганических веществ.
Неорганические вещества делятся на четыре основных класса: оксиды, кислоты, основания, соли. Представим известные нам классы соединений в виде единой схемы:
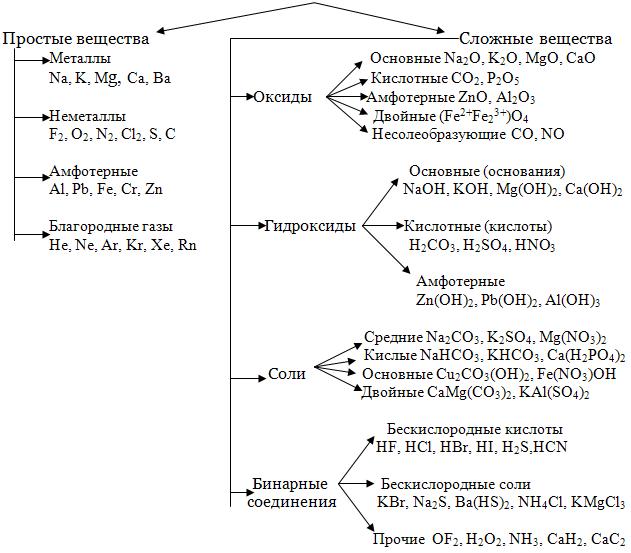
Деление веществ на классы достаточно условно. Например, мы знаем, что кислоты подразделяются на одно-, двух- и трехосновные, но их обычно не выделяют в отдельные классы соединений. Точно также не являются отдельными классами сильные и слабые кислоты. Это же справедливо и для оснований. Между классами существует важная связь, которую называют генетической. Эта связь заключается в том, что из веществ одного класса можно получить вещества других классов. Существует два основных пути генетических связей между веществами: один из них начинается металлами, другой – неметаллами. Например, сульфат кальция CaSO4 можно получить либо из металла кальция, либо другим путем – из неметалла серы:
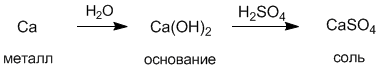
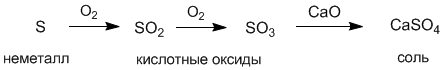
С другой стороны, из соли можно опять прийти к металлу и неметаллу:
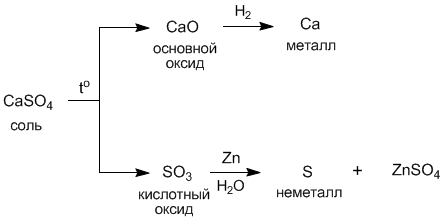
Одновременно существуют и другие пути взаимопревращений соединений разных классов. Таким образом, генетические связи между разными классами соединений очень многообразны.
Оксиды и их классификация.
Как мы уже знаем, оксиды бывают кислотные и основные. Это деление положено в основу их классификации.
Большинство кислотных оксидов хорошо реагирует с водой, давая кислоту. Например, кислый вкус простой газированной воды объясняется образованием угольной кислоты Н2СО3 из кислотного оксида СО2:
СО2 + Н2О = Н2СО3 (угольная кислота)
В простейших случаях формулу образующейся кислоты легко получить из формулы кислотного оксида простым сложением. Например:
| CO2 | + | H2O | = | H2CO3 |
| SO3 | + | H2O | = | H2CO3 |
Однако не все кислотные оксиды растворяются в воде, поэтому не все могут непосредственно с ней реагировать. Зато все кислотные оксиды реагируют с основаниями. При этом получается сразу соль. Например:
| SiO2 | + | H2O | = | реакция не идет |
| кислотный оксид (не растворим в воде) | вода |
| SiO2 | + | 2 NaOH | = | Na2SiO3 | + | H2O |
| кислотный оксид | щелочь | соль кремниевой кислоты H2SiO3 |
Полученную соль кремниевой кислоты можно превратить в саму кремниевую кислоту добавлением другой кислоты:
Na2SiO3 + 2 HCl = H2SiO3 + 2 NaCl
Таким образом, кислотному оксиду всегда соответствует определенная кислота:
CO2 (оксид углерода) – H2CO3 (угольная кислота);
SO3 (оксид серы VI) – H2SO4 (серная кислота);
SiO2 (оксид кремния) – H2SiO3 (кремниевая кислота).
Поскольку реакция с основаниями является общей для всех кислотных оксидов, им можно дать такое определение:






