¬ случае равновеси€ в растворе малорастворимого (или практически нерастворимого вещества) выражение дл€ константы равновеси€ в насыщенном растворе можно записать с использованием равновесных концентраций. Ќапример, дл€ равновеси€ в насыщенном растворе хлорида серебра
AgClкр + (n + m)H2O ⇄ [Ag(H2O) n ]++ [Cl(H2O) m ]Ц,
или в упрощенной форме
| AgClкр ⇄ Ag++ ClЦ. | (24) |
“ак как растворимость малорастворимых веществ посто€нна при данной температуре, то ее внос€т в значение константы и концентрацию твердых веществ не учитывают при записи закона действующих масс. ¬ыражение дл€ константы равновеси€ данной реакции запишетс€ так:
K– (AgCl) = [Ag+]Ј[Cl-]
“аким образом, в насыщенном растворе электролита произведение концентраций его ионов есть величина посто€нна€ при данной температуре, ее называют произведение растворимости и чаще обозначают буквами ѕ–:
| ѕ–(AgCl) = [Ag+]Ј[Cl-]. | (25) |
Ќапример, дл€ реакции
Ca(OH)2 ⇄ Ca2++ 2OHЦ
ѕ– = [Ca2+]Ј[ OHЦ]2
«начени€ произведений растворимости малорастворимых веществ €вл€ютс€ справочными величинами. «на€ произведение растворимости, легко рассчитать концентрацию вещества в насыщенном растворе, т.е. растворимость.
≈сли при проведении химической реакции в растворе по€вл€ютс€ ионы, вход€щие в состав малорастворимого вещества, то, зна€ произведение растворимости этого вещества, легко определить, выпадет ли оно в осадок. Ќапример дл€ реакции 8.2.15: если [Ag+][Cl-] > ѕ–(AgCl), то вещество выпадет в осадок; если [Ag+][Cl-] < ѕ–(AgCl), то вещество не выпадет в осадок.
ѕримеры решени€ задач
ѕример 1. —колько грамм сульфата натри€ и воды нужно дл€ приготовлени€ 300 г 5% раствора?
–ешение
m (Na2SO4) = ω (Na2SO4) / 100 = (5 ∙ 300) / 100 = 15 г,
где ω (Na2SO4) Ц массова€ дол€ в %, m - масса раствора в г,
m (H2O) = 300 г - 15 г = 285 г.
“аким образом, дл€ приготовлени€ 300 г 5% раствора сульфата натри€ надо вз€ть 15 г Na2SO4 и 285 г воды.
ѕример 2. акую массу хромата кали€ K2CrO4 нужно вз€ть дл€ приготовлени€ 1,2 л 0,1 ћ раствора?
–ешение
m (K2CrO4) = C (K2CrO4) ∙ V ∙ M (K2CrO4) =
= 0,1 моль/л ∙ 1,2 л ∙194 г/моль = 23,3 г.
“аким образом, дл€ приготовлени€ 1,2 л 0,1 ћ раствора нужно вз€ть 23,3 г K2CrO4 и растворить в воде, а объЄм довести до 1,2 литра.
ѕример 3. –ассчитайте мол€рную концентрацию и мол€рную концентрацию эквивалента 70 %-ного раствора H2SO4 (ρ = 1,615 г/мл).
–ешение
ƒл€ вычислени€ надо знать число граммов H2SO4 в 1 л раствора. 70%-ный раствор H2SO4 содержит 70 г H2SO4 в 100 г раствора. Ёто весовое количество раствора занимает объЄм
V = 100 / 1,615 = 61,92 мл
—ледовательно, в 1 л раствора содержитс€
70 ∙ 1000 / 61,92 = 1130,49 г H2SO4
ќтсюда мол€рна€ концентраци€ данного раствора равна:
1130,49 / ћ (H2SO4) =1130,49 / 98 =11,53 M
ћол€рна€ концентраци€ эквивалента этого раствора (счита€, что кислота используетс€ в реакции в качестве двухосновной) равна:
|
|
|
1130,49 / 49 =23,06 н
ѕример 4 акова мол€рна€ концентраци€ и мол€рна€ концентраци€ эквивалента 12%-ного раствора серной кислоты, плотность которого ρ = 1,08 г/см3?
–ешение
ћольна€ масса серной кислоты равна 98 г/моль. —ледовательно,
M э(H2SO4) = 98: 2 = 49 г экв./моль.
ѕодставл€€ необходимые значени€ в формулы, получим:
а) ћол€рна€ концентраци€ 12% раствора серной кислоты равна
—M = (12 ∙ 1,08∙10) / 98 = 1,32 моль/л.
б) ћол€рна€ концентраци€ эквивалента 12% раствора серной кислоты равна
—Ќ = (12 ∙ 1,08 ∙ 10) / 49 = 2,64 моль экв./л.
ѕример 5. »ногда в лабораторной практике приходитс€ пересчитывать мол€рную концентрацию в мол€рную концентрацию эквивалента и наоборот. ƒл€ пересчета из одной концентрации в другую можно использовать формулу:
—M = —Ќ ∙ f э
ћол€рна€ концентраци€ 0,5 н. Na2CO3
—M = 0,5 ∙ 1/2 = 0,25 моль/л
ѕример 6. –аствор, содержащий 3,04 г камфары —10Ќ16ќ в 100 г бензола, кипит при 80,714 ˚—. “емпература кипени€ бензола 80,2˚—. ¬ычислите эбуллиоскопическую константу бензола.
–ешение
“ак как раствор камфары в бензоле это раствор неэлектролита, то дл€ решени€ воспользуемс€ формулой 8.1.3.
Δ T кип = 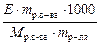 , отсюда
, отсюда
≈ = 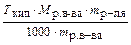 , M (—10Ќ16ќ) = 152 г/моль,
, M (—10Ќ16ќ) = 152 г/моль,
≈ = 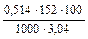 = 2,57 º.
= 2,57 º.
ѕример 7. ѕри 20 º— осмотическое давление водного раствора, в 100 мл которого содержитс€ 6,33 г гематина, равно 243,4 кѕа. ќпределите мол€рную массу гематина.
–ешение
ƒл€ решени€ воспользуемс€ формулой 8.1.4. Ќайдем из нее мол€рность раствора
—ћ = π / R“ =243,4/(8,31∙293) = 0,1 моль/л.
“еперь вычисли мол€рную массу гематина. ¬ 100 мл воды содержитс€ 6,33 г гематина, значит в 1000 мл (1 л) 63,3 г. ќтсюда 63,3 это 0,1 моль, а 1 моль составит 633 г:
ћ (гематина) = 633 г/моль.
ѕример 8. –ассчитайте рЌ 0,002 ћ раствора Ќ2—ќ3.
–ешение
ѕри расчетах рЌ слабых электролитов можно использовать формулу рЌ = Цlg — Ќ+и учитывать только первую ступень диссоциации:
Ќ2—ќ3 ⇄ Ќ++ Ќ—ќ3 Ц,
онстанту диссоциации по первой ступени дл€ угольной кислоты находим в приложении: д1= 4,45∙10-7.
–авновесную концентрацию ионов водорода можно рассчитать двум€ способами: непосредственно из выражени€ дл€ д и через степень диссоциации α.
1. ≈сли прин€ть концентрацию диссоциированных молекул за —, то равновесные концентрации — Ќ+и — Ќ—ќ3 Ц = —, а равновесна€ концентраци€ недиссоциированных молекул — Ќ2—ќ3= (0,002 Ц —). ѕодставим эти значени€ в выражение дл€ д:
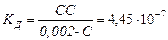 .
.
–еша€ это уравнени€ относительно —, получим: — = — Ќ+= 3∙10-5. ќткуда рЌ = -lg — Ќ+= 4,52.
2. ѕоскольку ƒ < 10-4, то в данном случае можно рассчитать по упрощенному выражению закона разбавлени€ ќствальда:
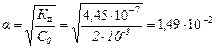 .
.
¬ соответствии с уравнением диссоциации концентраци€ ионов — Ќ+равна концентрации — Ќ—ќ3 Ц и концентрации диссоциированных по первой ступени молекул Ќ2—ќ3. “огда, по определению:
α = — / — 0 = — Ќ+/ — 0 и — Ќ+= α— 0 = 1,49∙10-2 ∙2∙10-3 = 2,98∙10Ц5.
рЌ = Цlg — Ќ+= 4,52.
ѕример 9. –ассчитайте рЌ 0,05 ћ раствора ќЌ.
–ешение
“ак как ќЌ сильный электролит, то рЌ следует рассчитывать с учетом ионной силы раствора, т.е. через активность.
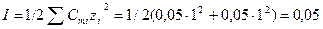 .
.
ѕо справочным данным (приложение 5) находим коэффициент активности, соответствующий этой ионной силе:
|
|
|
γ = 0,85, тогда а (ќЌЦ) = γ∙— ќЌЦ= 0,85∙0,05=0,043 и
рќЌ= Цlg — ќЌЦ=1,37, рЌ=14 Ц рќЌ = 14 Ц 1,37 = 12,63.
ѕример 10. –ассчитайте рЌ и рќЌ 0,001 ћ раствора Pb(NO3)2, учитыва€ только первую ступень гидролиза.
–ешение
рЌ = Ц lg [Ќ+].
«апишем уравнение гидролиза нитрата свинца по первой ступени:
Pb(NO3)2 + Ќ2ќ ⇄ PbOHNO3 + HNO3
Pb2+ + 2NO3Ц+ Ќ2ќ ⇄ PbOH+ + NO3Ц+ H+ + NO3Ц
Pb2+ + Ќ2ќ ⇄ PbOH+ + H+
“аким образом, концентраци€ Ќ+обусловлена диссоциацией образующего сильного электролита Ц азотной кислоты. „тобы найти концентрацию Ќ+необходимо знать степень гидролиза нитрата свинца. ¬оспользуемс€ упрощенной формулой закона ќствальда:
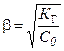 ;
; 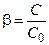
¬ приложении находим ƒќ2= 3,0 ∙10Ц8. ќбратите внимание, что в данном случае используетс€ константа диссоциации основани€ по второй ступени.
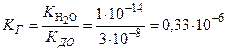 ,
,
отсюда
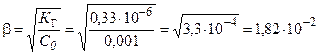 ;
;
— = β — 0 = 1,82∙10Ц2 ∙0,001 = 1,82∙10Ц5.
рЌ = Ц lg [1,82∙10Ц5] = 5 + 0,26 = 5,26,
рќЌ = 14 Ц 5,26 = 8,74.
ѕример 11. ¬ыпадет ли осадок гидроксида меди при добавлении 100 мл 0,01 ћ раствора гидроксида кальци€ к равному по объему 0,001 ћ раствору сульфата меди?
Cu2++ 2OHЦ⇄ Cu(OH)2↓
–ешение
ќсадок гидроксида меди образуетс€, если произведение концентраций ионов Cu2+и OHЦбудет больше произведени€ растворимости этого малорастворимого гидроксида. ѕосле сливани€ равных по объему растворов общий объем раствора станет в два раза больше, чем объем каждого из исходных растворов, следовательно начальна€ концентраци€ каждого из реагирующих веществ уменьшитс€ вдвое. онцентраци€ в полученном растворе ионов меди
C( Cu2+) = (0,001 моль/л): 2 = 0,0005 моль/л.
онцентраци€ гидроксид ионов Ц
c (OH-) = (2.0,01 моль/л): 2 = 0,01 моль/л.
ѕроизведение растворимости гидроксида меди
ѕ–[Cu(OH)2] = [Cu2+][OH-]2 = 5,6 ∙10 Ц20 моль3/л3.
ѕроизведение концентраций ионов в растворе
[Cu2+]∙[OH-]2 = 0,0005 моль/л ∙ (0,01 моль/л)2 = 5∙10 Ц8 моль3/л3.
ѕроизведение концентраций больше произведени€ растворимости, следовательно, осадок выпадет.
4.4. «адачи дл€ самосто€тельного решени€ 61. 19 мл 11% раствора ќЌ (ρ = 1,01 г/см3) смешали с 200 мл воды. –ассчитайте мол€рную долю полученного раствора.
ќтвет: ω = 0,31 %.
62 Ќа нейтрализацию 50 см3 раствора кислоты израсходовано 25 см3 0,5 н раствора щелочи. „ему равна мол€рна€ концентраци€ эквивалента (нормальность) кислоты?
ќтвет: — Ќ = 0,25 моль экв/л.
63. акой объем 50% раствора ќЌ (ρ = 1,538 г/см3) требуетс€ дл€ приготовлени€ 3 л 0,1 ћ раствора ќЌ?
ќтвет:V = 21,85 мл.
64. ¬ычислите мол€рную концентрацию 20%-ного раствора хлорида кальци€ (ρ =1,178 г/см3)
ќтвет: —ћ = 2,12 моль/л.
65. 3 г H2SO4 растворено в 50 мл воды. „ему равна мол€рна€ концентраци€ эквивалента данного раствора, если его плотность составл€ет 1,01 г/см3?
ќтвет: —Ќ = 1,17 моль экв/л.
66. ќпределите массу 3 %-ного раствора пероксида водорода, если он получен при разбавлении 50 г 30 %-ного раствора.
ќтвет:m = 500 г.
67. ќпределите массы исходных растворов с массовыми дол€ми гидроксида натри€ 5 % и 40 %, если при их смешивании образовалс€ раствор массой 210 г с массовой долей гидроксида натри€ 10 %.
ќтвет: m (40 % р-ра) = 30 г, m (5 % р-ра) = 180 г.
68. —колько граммов хлористого кали€ надо растворить в 90 г 8 %-ного раствора этой соли, чтобы полученный раствор стал 10 %-ным?
ќтвет: m = 2 г.
69. ¬ычислите мол€льную концентрацию 20 %-ного раствора хлорида лити€.
ќтвет: —m = 7,3 моль/кг.
”парили 100 г 15 %-ного раствора сульфата кали€ до 80 г. ќпределите массовую долю соли в полученном растворе. ќтвет: ω = 18,75 %.70. –ассчитайте мол€рность и нормальность 7 %-ного раствора H3–O4 (ρ = 1,15 г/мл).ќтвет: —Ќ = 2,46 моль экв/л, —ћ = 0,82 моль/л.
71. 10 г Na3PO4 растворили в 590 мл воды. ρ раствора составила 1,07 г/см3. ќпределите мол€рную концентрацию и титр полученного раствора.
|
|
|
ќтвет: —ћ = 0,1 моль/л, “ = 0,018 г/мл.
72. ¬ каком объеме 0,1 н раствора содержитс€ 8 г сульфата меди?
ќтвет: V = 1 л.
73. Ќеобходимо получить 0,1 г серебра. акой объем 0,001 ћ раствора нитрата серебра дл€ этого потребуетс€?
ќтвет: V = 1 л.
74. —колько миллилитров 2 ћ раствора нитрата натри€ (ρ = 1,05 г/мл) необходимо вз€ть дл€ приготовлени€ 1 литра раствора с мол€льностью 0,01 моль/кг?
ќтвет: V = 4,42 мл.
75. ¬ычислите массовую концентрацию водного раствора сахара —12Ќ22ќ11, зна€, что температура кристаллизации раствора Ц0,93 ˚—. риоскопическа€ константа воды 1,86˚.
ќтвет: ω = 14,6 %
76. –аствор, содержащий 0,15 г неэлектролита в 100 г бензола, кристаллизуетс€ при 5,296 º—. “емпература кристаллизации бензола 5,5 º—. риоскопическа€ константа бензола 5,1º. ¬ычислите мол€рную массу растворенного вещества.
ќтвет: ћ = 37,5 г/моль.
77. ¬ычислите температуру кристаллизации раствора мочевины (NH2)2CO, содержащего 5 г мочевины в 150 г воды. риоскопическа€ константа воды 1,86˚.
ќтвет: “ = Ц1,03 º—.
78. –аствор, содержащий 3,04 г камфары —10Ќ16ќ в 100 г бензола, кипит при 80,714 º—. “емпература кипени€ бензола 80,2 º—. ¬ычислите эбуллиоскопическую константу бензола.
ќтвет:≈ = 2,57 º.
79. ¬ычислите мол€рную массу неэлектролита, зна€, что раствор, содержащий 2,25 г этого вещества в 250 г воды, кристаллизуетс€ при 0,279˚—. риоскопическа€ константа воды 1,86˚.
ќтвет: ћ = 60 г/моль.
80. ¬ычислите температуру кипени€ 5 % раствора нафталина —10Ќ8 в бензоле. “емпература кипени€ бензола 80,2 º—. Ёбуллиоскопическа€ константа его 2,57º..
ќтвет: “ = 81,257 º—
онтрольные вопросы
1. „то такое концентраци€ раствора?
2. ћожет ли твердый сплав быть раствором?
3. акие свойства растворов называют коллигативными.
4. Ѕудет ли отличатьс€ способ расчета температуры замерзани€ дл€ раствора сахара и раствора хлорида натри€? ѕочему?
5. „ем отличаютс€ электролиты от неэлектролитов?
6. ѕрименим ли закон разбавлени€ ќствальда дл€ растворов электролитов? ѕочему?
7. ƒайте определение водородного показател€.
8. ¬ каком случае дл€ расчета среды раствора используют коэффициент активности?






