Електронна будова катіонів першої аналітичної групи наступна: Na+ − [Ne]; K+ − [Ar].
4.1.1. Реакції виявлення катіонів Na+
Дослід 1. При дії на розчин, що містить катіони Na+, розчином калій дигідроантимонату утворюється білий кристалічний осад натрій дигідроантимонату:
Na+ + KH2SbO4 → NaH2SbO4↓ + K+;
Na+ + H2SbO4− → NaH2SbO4↓.
Для проведення цієї реакції у пробірку вносять 5-6 крапель розчину солі Натрію і додають стільки ж розчину KH2SbO4.
Реакція дуже малочутлива. Осад як такий майже не утворюється. Спостерігається лише помутніння вмісту пробірки і лише тоді, коли потерти скляною паличкою внутрішні стінки пробірки для того, щоб створити центри кристалізації NaH2SbO4. Розчин для виявлення йонів Na+ повинен містити значну кількість цих йонів, а середовище має бути нейтральним чи слабколужним. У кислому середовищі KH2SbO4 перетворюється у малорозчинну метастибійну кислоту, що являє собою аморфний осад білого кольору:
KH2SbO4.+ Н+→ H3SbO4 + K+;
H3SbO4 → HSbO3↓ + Н2О.
Якщо йони Na+ визначати цим реагентом у кислому середовищі, то поява білого аморфного осаду ще не свідчить про наявність у розчині йонів Na+.
Для покращення утворення осаду NaH2SbO4 реакцію потрібно проводити при охолодженні.
Дослід 2. Пірохімічна реакція виявлення йонів Na+
Платинову чи ніхромову дротинку, на кінці якої є петля, занурюють у розчин, що містить йони Na+, чи на петлю набирають сухої речовини, а потім вносять у безбарвне полум’я пальника. Полум’я пальника за наявності сполук Натрію забарвлюється в жовтий колір. Реакція дуже чутлива, але у присутності у досліджуваному середовищі інших йонів забарвлення полум’я може спотворюватись. Тому пірохімічний спосіб виявлення йонів Na+ не можна вважати цілком достовірним.
Дослід 3. Найбільш специфічною реакцією виявлення йонів Na+ є мікрокристалоскопічна реакція з цинк-ураніл ацетатом.
На предметне скло мікроскопа наносять краплю розчину, що містить йони Na+. Обережно випарюють краплину досуха над полум’ям пальника. Після охолодження на місце сухого залишку наносять краплю розчину цинк-ураніл ацетату Zn(UO2)3(CH3COO)8. Утворюються правильні кристали тетраедричної чи октаедричної форми блідо-жовтого кольору натрій-цинк-ураніл ацетату NaZn(UO2)3(CH3COO)9∙9Н2О.
Якщо на предметному склі виявиться товстий шар кристалів, то значну частину їх змивають водою, залишивши лише дуже малу кількість їх. Розглядають під мікроскопом форму та забарвлення кристалів натрій-цинк-ураніл ацетату. Йони Na+ за цією реакцією краще виявляти з розведених розчинів. Заважають виявленню Na+ катіони Ag+ та йони Sb3+ і аніони AsO43–, які з
цинк-ураніл ацетатом утворюють осади, аналогічні як з катіоном Na+.

4.1.2. Реакції виявлення катіонів К+
Дослід 1. Йони К+ з гідротартрат-аніонами з солі NaHC4H4O6 утворюють білий кристалічний осад калій гідротартрату:
K+ + HC4H4O6− → KHC4H4O6↓.
Для проведення цієї реакції у пробірку вносять 5-6 крапель розчину солі Калію і додають такий же об’єм розчину гідротартрату. Вміст пробірки перемішують скляною паличкою, потираючи нею внутрішні стінки пробірки. Випадає білий кристалічний осад калій гідротартрату. Ця реакція дуже малочутлива і не специфічна. Для виявлення йонів К+ за цією реакцією необхідна значна концентрація їх у досліджуваному розчині. Мала чутливість реакції пояснюється досить значною розчинністю калій гідротартрату. ДР(KHC4H4O6)=3,4∙10–4.
Для проведення реакції замість NaHC4H4O6 можна брати винну кислоту. Якщо осад не випадає, то треба знизити концентрацію гідроген-іонів шляхом додавання розчину натрій ацетату.
Перед проведенням реакції осадження йонів К+ у вигляді KHC4H4O6 попередньо необхідно видалити з розчину йони амонію, оскільки NH4+ з аніонами HC4H4O6− утворюють подібний осад NH4HC4H4O6.
Осад калій гідротартрату розчиняється як в концентрованих розчинах лугів, так і концентрованих кислот, оскільки в кислому середовищі утворюється добре розчинна у воді винна кислота:
| KHC4H4O6 + Н+ → | 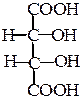
| + K+ |
Константа дисоціації винної кислоти К1=1,0∙10–3; К2=4,6∙10–10.
У лужному середовищі утворюється середня розчинна у воді сіль винної кислоти:
| KHC4H4O6 + NaOH → | 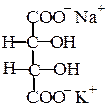
| + H2O. |
| сегнетова сіль |
При нагріванні осад KHC4H4O6 теж розчиняється, а також розчиняється при додаванні до осаду значної кількості холодної води.
Дослід 2. Більш чутливою реакцією на катіони К+ є взаємодія їх з розчином натрій гексанітро(ІІІ) кобальтатом:
2К+ + Na3[Co(NO2)6] → K2Na[Co(NO2)6]↓ + 2Na+.
Утворюється оранжево-жовтий осад комплексної солі
натрій-калій гексанітро(ІІІ) кобальтату, який розчинний в сильних кислотах. У лужному середовищі відбувається руйнування комплексної солі Na3[Co(NO2)6] і утворюється темно-бурий осад Co(OH)3.
Слід мати на увазі, що Na3[Co(NO2)6] швидко розкладається при зберіганні, тому для проведення реакції виявлення йонів К+ слід користуватись свіжоприготовленим розчином цього реагенту. Якщо розчин реагенту має рожеве забарвлення, то такий розчин вже не придатний для аналізу.
Реагент також розкладається у лужному та дуже кислому середовищах.
Аналогічну реакцію з Na3[Co(NO2)6] дають також йони NH4+.
2NH4+ + Na3[Co(NO2)6] → (NH4)2Na[Co(NO2)6]↓ + 2Na+.
Утворюється оранжево-червоне забарвлення розчину. Осаду (NH4)2Na[Co(NO2)6] утворюється значно менше, ніж осаду K2Na[Co(NO2)6] і забарвлення його є більш темним.
Дослід 3. Мікрокристалоскопічна реакція виявлення йонів К+
З катіонами К+ натрій-плюмбум гаксанітро(ІІ) купрат Na2Pb[Cu(NO2)6] утворює кубічні кристали чорного чи коричневого кольору калій-плюмбум гексанітро(ІІ) купрату:
2К+ + Pb2+ + [Cu(NO2)6]4– → K2Pb[Cu(NO2)6]↓.
Для проведення цієї реакції краплю розчину, що містить йони К+, наносять на предметне скло мікроскопа і випарюють її над полум’ям пальника. Після охолодження скла на сухий залишок наносять краплю розчину натрій-плюмбум гаксанітро(ІІ) купрату. Утворюються характерні кубічні кристали. Реакцію проводять у середовищі рН=6-7.
Виявленню йонів К+ за цією реакцією заважають йони амонію.
Реагент з йонами NH4+ утворює аналогічні кристали
амоній-плюмбум гексанітро(ІІ) купрату:
2NH4+ + Pb2+ + [Cu(NO2)6]4– → (NH4)2Pb[Cu(NO2)6]↓.
Рис. … Кристали калій-плюмбум гексанітро(II) купрату
Дослід 4. Пірохімічна реакція виявлення йонів К+
Платинову чи ніхромову дротинку з кільцем на кінці змочують хлоридною кислотою та прожарюють у полум’ї пальника для видалення слідів солей до повного зникнення забарвлення полум’я. Розжареною дротинкою торкаються кристалів солі калію. Кристалики солі, які прилипли до дротинки, вносять у безбарвну частину полум’я пальника. Полум’я забарвлюється у блідо-фіолетовий колір. Забарвлення полум’я краще спостерігати крізь синє скло для поглинання жовтих променів, обумовлених йонами Натрію.
4.1.3. Реакції виявлення катіонів NH4+
Дослід 1. При дії лугів на середовище, що містить йони NH4+, виділяється амоніак: NH4+ + ОН− → NH3↑ + Н2О, який можна виявити за допомогою універсального індикаторного паперу.
Для проведення цього досліду у пробірку вносять декілька крапель розчину, що містить йони NH4+, додають такий же об’єм концентрованого розчину лугу і нагрівають. Над отвором пробірки тримають змочену водою смужку універсального індикаторного паперу. За наявності амоніаку індикаторний папір набуває синього забарвлення.
Дослід 2. Виявлення йонів NH4+ з реактивом Неслера
Реактив Неслера є сумішшю комплексної солі K2[HgI4] з КОН.
При взаємодії цього реактиву з сіллю амонію утворюється нерозчинна комплексна сполука червоно-бурого кольору:
| NH4Cl + 2K2[HgI4] + 4KOH → | 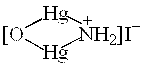
| + KCl + 7KI +3H2O; |
NH4+ + 2[HgI4]2– + 4OH– → [OHg2NH2]I↓ + 7I– +3H2O.
У пробірку вносять 3-4 краплі розчину, що містить йони NH4+, додають таку ж кількість або трохи більше реактиву Неслера. При цьому випадає осад червоно-бурого забарвлення. Реакція є дуже чутливою. Утворений осад розчиняється в солях амонію, тому реактив Неслера має бути у надлишку.
Виявленню йонів NH4+ за цією реакцією заважають йони Fe3+, Cr3+, Co2+, Ni2+ та інші, які з реактивом Неслера утворюють осади різного забарвлення. Для маскування йонів, що заважають, додають розчин калій-натрій тартрату KNaC4H4O6, який зв’язує ці йони у комплексні сполуки.
Виявлення йонів NH4+ реактивом Неслера краще проводити в газовій фазі. Для цього досліджуваний на йони NH4+ розчин вносять у пробірку, додають декілька крапель концентрованого розчину лугу. Над отвором пробірки тримають смужку фільтрувального паперу, змоченого реактивом Неслера. Суміш у пробірці нагрівають. Амоніак, що при цьому виділяється, реагує з реактивом Неслера і смужка паперу набуває цегляно-червоного забарвлення.
Дослід 3. Йони амонію утворюють з натрій гідротартратом чи винною кислотою осад амоній гіфдротартрату, схожий на осад KНC4H4O6, про що вже було зазначено вище.
Дослід 4. Як вже зазначалося, йони NH4+ утворюють з натрій-плюмбум гексанітро(ІІ) купратом кубічні кристали чорного кольору (NH4)2Pb[Cu(NO2)6] схожі на кристали K2Pb[Cu(NO2)6].
Дослід 5. Як і йони К+, йони NH4+ утворюють з Na3[Co(NO2)6] схожий оранжевий осад (NH4)2Na[Co(NO2)6].
Дослід 6. Солі амонію термічно нестійкі. Так, амоній гідрокарбонат NH4HCO3 помітно розкладається вже при кімнатній температурі і у зв’язку із цим тхне амоніаком. При нагріванні до 4000С всі амонійні солі розкладаються:
NH4Cl → NH3↑ + HCl↑;
(NH4)3PO4 → 3NH3↑ + H3PO4;
(NH4)2CO3 → 2NH3↑ + CO2↑+ H2O.
У амоніачних солях кислот-окисників при нагріванні відбуваються окисно-відновні процеси:
NH4NO3 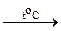 N2O↑ + 2H2O;
N2O↑ + 2H2O;
NH4NO2 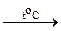 N2↑ + 2H2O;
N2↑ + 2H2O;
(NH4)2Cr2O7 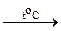 N2↑ + Cr2O3 + 4H2O.
N2↑ + Cr2O3 + 4H2O.
За цими реакціями можна виявити тверді амонійні солі. Для цього в суху пробірку вносять сухі досліджувані речовини і нагрівають. Тверді продукти розкладу досліджують на відсутність йонів амонію, а у випадку NH4Cl – на стінках пробірки осаджується ця сіль при охолодженні у вигляді білого нальоту:
NH3 + HCl → NH4Cl.






