Зрительный пигмент родопсин, так же как и бактериородопсин, — практически единственный белок в фоторецепторной мембране зрительной клетки сетчатки глаза (на его долю приходится до 80% всего белка в мембране).
Пурпурные мембраны, локализованные в цитоплазме клеток некоторых экстремально галофильных бактерий, содержат единственный гидрофобный пигмент — белковый комплекс бактериородопсин, молекулы которого располагаются в ПМ строго упорядоченно.
ПМ в интактных клетках и в изолированных препаратах представляют собой дискообразные образования диаметром около 0,5 мкм и толщиной 5—6 нм. Бр расположен в ПМ симметричными группами по три молекулы, причем каждый такой тример стабилизирован 12—14 молекулами структурных липидов. Данные спектров кругового дихроизма в УФ-области свид-ют о высокой степени аспирализации белковой цепи Бр. Хромофор белка — ретиналь — содержится в белке в молярном соотношении 1:1, т. е. на каждую белковую цепь приходится один ретиналь.
Трехмерная структура молекулы Бр в ПМ расшифрована с помощью метода дифракции электронов. Одна молекула Бр содержит 7 аспиральных участков, пронизывающих ПМ. С помощью комплекса физико-химических и биохимических методов определено, что ретиналь ковалентно связан с опсином и образует связь с одним из остатков лизина в белковой цепи (так называемое шиффово основание).
Макромолекулы Бр гораздо менее подвижны, чем другие мембранные белки. Из темпер-ой зависимости спектров кругового дихроизма ПМ видно, что при температурах выше 30°С взаимодей-е мол-л Бр внутри триммеров практ-ки исч-т и в ПМ сущ-т мономерная форма Бр.
В модельных системах максимум поглощения шиффова основания в протонированной форме находится около 440 нм, в непротонированной — около 360 нм. Однако в Бр максимумы, соответствующие протонированной форме шиффова основания, расположены около 560—570 нм, а непротонированной — около 412 нм. Бр в ПМ может находиться в двух различных состояних: после адаптации к темноте или к свету. Эти состояния отличаются по спектрам поглощения Бр. Максимум полосы, поглощения Бр в образцах, адаптированных к темноте, расположен около 560 нм. После освещения максимум сдвигается до 570 нм. Изомеры Бр при возбуждении светом вовлекаются в различные циклы превращений. В темноте наблюдается медленный процесс релаксации части Бр до достижения темноадаптированного состояния.
27. Каковы основные электрокинетические явления в биологических объектах. Методы их регистрации и измерения. ξ - потенциал дрожжевых клеток.
Электрокинетические явления явления возникающие в сложных системах при движении дисперсных сред относительно дисперсионной (водные растворы белков и солей) среды возникают. Если наблюдается движение одной из фаз по отношению к другой под действием внешнего электрического поля, то эта группа явлений называется электроосмосом или электрофорезом. В частности, электрофорез - это движение дисперсной фазы по отношению к дисперсионной среде во внешнем электрическом поле, а электроосмос движение дисперсионной среды относительно неподвижной дисперсной фазы (в капиллярах, в пористых перегородках) под действием электрического поля.
Потенциал течения возникают в результате движения жидкости под действием гидростатического давления через капилляры или поры, стенки которых обладают электрическим зарядом. Это явление, обратное электроосмосу.
Потенциал седиментации возникают между верхними и нижними слоями гетерогенной системы при оседании (седиментации) частиц дисперсной фазы под действием силы тяжести. Потенциал седиментации возникает, например, при стоянии крови. Форменные элементы (эритроциты, лейкоциты, тромбоциты), удельный вес которых больше, чем плазмы, оседают на дно сосуда. Противоионы диффузионного слоя - катионы-отстают от движения форменных элементов. В результате этого нижние слои приобретают отрицательный заряд, а верхние-положительный.
В основе всех наблюдаемых явлений находится относительное движение ионных слоев и пространственное разделение зарядов (поляризация) в направлении движения фаз. Для электрокинетических явлений (ЭКЯ) характерно возникновение на границе фаз избыточных зарядов, которые образуют два противоположно заряженных слоя т.н. двойной электрический слой (ДЭС), в котором электрический потенциал изменяется скачком. Это явление имеет место во многих случаях. Заряд центральной частицы и ионной атмосферы всегда противоположен, поэтому под действием электрического поля на частицу и её атмосферу влияют силы противоположной направленности.
Механизм образования ДЭС в разных системах различен. Например, на поверхности металлов часть электронов несколько выходят за пределы решетки, состоящей из положительных ионов и ДЭС в этом случае вносит свой вклад в работу выхода электронов из металла. Если металл поместить в электролит, содержащие ионы этого металла, то образуется дополнительный ионный ДЭС возникающий в результате ориентации полярных молекул растворителя (например, Н2О) у поверхности металла.
Двойной электрический слой может образоваться и на поверхности биологических мембран (БМ).
Наружные полярные (гидрофильные) молекулы создают на поверхности БМ некоторый заряд (преимущественно отрицательный), который препятствует их слипанию, а в самой БМ возникает межфазный скачек потенциала того же знака, что и заряд на мембране. Поверхностная концентрация одновалентных заряженных групп s (измеряется кмоль/м2) связана с межфазным потенциалом 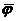 уравнением Гуи – Чепмена
уравнением Гуи – Чепмена

где R- газовая постоянная, NА- число Авогадро, F- число Фарадея, С- молярная концентрация одновалентного электролита в среде (KСl или NaCl), e- относительная диэлектрическая проницаемость, `j- потенциал в безразмерной форме (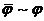 ). Естественно, что заряд на БМ из электролита притягивает ионы противоположного знака, что приводит к образованию ДЭС.
). Естественно, что заряд на БМ из электролита притягивает ионы противоположного знака, что приводит к образованию ДЭС.
В реально функционирующей БМ существует ассиметрия распределения ионов внутренней среды за счет активного и пассивного транспорта ионов и картина выглядит значительно сложней. В простейшем случае распределение потенциалов вблизи мембраны по обе стороны от нее имеет вид рис.6., т.е. для БМ характерны скачки потенциалов, причем по мере удаления от границы раздела потенциал уменьшается по экспоненте

где x- координата точки пространства, а LD- радиус экранировки Дебая.
Таким образом, возникающий в биологических объектах и в любых других дисперсных системах Д.Э.С. приводит к возникновению потенциала на поверхности раздела фаз - x-потенциала, который можно зарегистрировать и величина его будет зависеть как от свойств среды, так и от функционального состояния биологических объектов.
В лабораторной работе определялась величина x- потенциала дрожжевых клеток имеющих сферическую форму, движущихся под действием внешнего электрического поля (электрофорез).
Величина потенциала на поверхности дрожжевой клетки, которую мы будем называть x- потенциалом определится по формуле
 (5).
(5).
Подставляя вместо h=10-2 и e=81 для воды p=3,14 и, переводя все единицы измерения в СИ, будем иметь расчетную формулу
 (6).
(6).
Иногда вместо  пишут
пишут  , где `v называется электрофоретической скоростью или подвижностью. Легко видеть, что подвижность частицы
, где `v называется электрофоретической скоростью или подвижностью. Легко видеть, что подвижность частицы  есть отношение ее линейной скорости v к градиенту потенциала электрического поля. Поэтому (6) можно записывать в виде
есть отношение ее линейной скорости v к градиенту потенциала электрического поля. Поэтому (6) можно записывать в виде
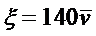 (7).
(7).
Зная x-потенциал и радиус частицы можно определить поверхностную плотность зарядов  , где q=jer(СГС), а S- площадь сфероида (S=4pr2). Эта величина зависит от свойств биологической мембраны и может меняться при изменении функционального состояния организма (патология) или условий внешней среды, например, действие радиации.
, где q=jer(СГС), а S- площадь сфероида (S=4pr2). Эта величина зависит от свойств биологической мембраны и может меняться при изменении функционального состояния организма (патология) или условий внешней среды, например, действие радиации.






