ДНК-содержащими вирусами являются возбудители герпетической вирусной инфекции. Герпесвирусные заболевания вызываются вирусами герпеса 1-го, 2-го, 3-го, 4-го и 5-го (цитомегаловирус) типов.
Универсальным представителем аномальных нуклеозидов, используемых для лечения герпетических инфекций, является ацикловир. Препарат показан для лечения герпетической инфекции и профилактики заболевания. Несомненным достоинством ацикловира является широкий спектр противогерпетической активности. Однако тяжелые побочные эффекты, развивающиеся при резорбтивном действии ацикловира, ограничивают его применение.
Ацикловир выпускается в форме 5% крема и мази для местного и наружного применения, 3% глазной мази, таблеток для приема внутрь по 200 и 400 мг, а также в виде порошка для приготовления раствора для инфузий по 250 мг. Кратность применения препарата составляет 3-4 раза в сутки. Побочные эффекты: диспепсические расстройства, головная боли и головокружение, сыпь, фотосеснсебилизация, лихорадка.
Валацикловир по своим основным характеристикам близок к ацикловиру, но отличается от него большей биодоступностью при энтеральном приеме. Валацикловир является пролекарством и в организме человека превращается в ацикловир. Валацикловир активен в отношении всех типов герпесвирусов.
Ганцикловир назначатся только при цитомегаловирусной инфекции, так как его прием часто приводит к тяжелым нарушениям фунций различных органов и систем.
Ингибиторы обратной транскриптазы.
Обратная транскриптаза (ревертаза) - это фермент, участвующий в репродукции вирусов семейства Retroviridae. Она обеспечивает обратную направленность потока генетической информации - не от ДНК к РНК, а, наоборот, от РНК к ДНК, в связи с чем семейство получило свое название. К ретровирусам относится вирус иммунодефицита человека (ВИЧ). Поздней стадией ВИЧ-инфекции является СПИД (синдром приобретенного иммунодефицита человека). Для ВИЧ-инфекции характерны прогрессирующие нарушения иммунного реагирования в результате длительного циркулирования вируса в лимфоцитах, макрофагах и клетках нервной ткани человека. Как мы отмечали выше представлены нуклеозидными и ненуклеозидными ингибиторами. Нуклеозидные ингибиторы конкурентно подавляют ревертазу, в результате чего нарушается синтез дочерней РНК вируса. Ненуклеозидные ингибиторы прямо взаимодействуют с каталитическим центром фермента, инактивируя его.
Ламивудин характеризуется высокой биодоступностью (80-88%) и активен в отношении штаммов ВИЧ, устойчивых к зидовудину. Ламивудин применяется также для лечения вирусного гепатита В. Выпускается в форме таблеток для приема внутрь по 150 и 300 мг. Схема лечения подбирается индивидуально. Побочные эффекты: диспепсические расстройства, головная боль, инфекции дыхательных путей.
Ингибиторы протеаз.
По принципу конкурентного антагонизма угнетают ВИЧ-протеазы. В результате вирусные ферменты теряют способность расщеплять полипротеины-предшественники, необходимые для репликации вируса. Это приводит к формированию неактивных вирусных частиц.
Саквинавир выпускается в форме таблеток для приема внутрь по 500 мг. Кратность приема препарата составляет 2 раза в сутки. Побочные эффекты: диспепсические расстройства, липодистрофия, головная боль, спазм мышц, анемия, одышка, сахарный диабет, повышение активности печеночных ферментов.
Интерфероны и индукторы интерферонов.
Интерфероны - низкомолекулярные белки, синтезируемые клетками человека в процессе защитной реакции на чужеродные агенты. Интерфероны (ИФН) имеют выраженную видовую специфичность и являются одним из важнейших факторов защиты организма при первичной вирусной инфекции. Синтезировать интерфероны способны все клетки человека, но основным их источником являются иммунные клетки. Механизм действия интерферонов включает следующие моменты: подавление транскрипции вирусных белков, угнетение трансляции вирусных белков, подавление белкового метаболизма, нарушение сборки и созревание вирусной частицы. Важным свойством интерферонов является их способность активировать в клетках человека синтез защитных ферментов, блокирующих репликацию вирусной ДНК и РНК. Сложный механизм действия обеспечивает интерферонам широкий спектр антивирусной активности. Более того, считается, что резистентности к интерферону у вирусов не возникает. Иммуномодулирующая активность интерферонов усиливает их противовирусный эффект.
Интерфероны (интерферон альфа, интерферон альфа-2a, интерферон альфа-2b) выпускаются в форме порошка для приготовления раствора для интраназального введения по 1000 и 50000 МЕ, назальных и глазных капель по 10000 МЕ в 1 мл, в форме порошка для приготовления раствора для внутримышечного введения по 10000 МЕ, в виде готового раствора для инъекций по 1000000, 3000000, 5000000, 6000000, 9000000 и 10000000 МЕ, в виде геля и мази для наружного применения по 36000 и 40000 МЕ в 1 г соответственно, в виде ректальных суппозиториев по 150000, 500000, 1000000 и 3000000 МЕ. Схема лечения подбирается индивидуально. Наиболее частые побочные эффекты - аллергические реакции.
Индукторы интерферона - вещества природного и синтетического происхождения, вызывающие продукцию эндогенного ИФН в клетках макроорганизма.
К индукторам интерферона относятся: "Актипол", "Арбидол", "Полудан", "Амиксин", "Копаксон", "Изопринозин", "Галавит", "Гепон", "Деринат", "Иммуномакс", "Ликопид", "Полиоксидоний", "Декарис".
Фитопрепараты: "Эхиноцея", "Синупрет", "Тонзилгон".
Несмотря на достаточно обширный список препаратов, вирусные заболевания остаются плохо контролируемыми инфекциями. Это связано с отсутствием радикальных способов терапии и развитием резистентности вирусов. Поэтому максимальная эффективность противовирусной терапии достигается при комплексном характере лечения.
Лекция №9.
Средства, влияющие на афферентную иннервацию.
Известно, что иннервация органов и систем человеческого организма подразделяется на афферентную (восходящую от периферических рецепторов и нервных окончаний к ЦНС) и эфферентную (нисходящую от ЦНС к внутренним органам и скелетной мускулатуре). Лекарственные средства, изменяющие иннервацию, занимают очень важную нишу в фармакологии, поскольку имеют достаточно широкий спектр действия на организм. В данной лекции мы подробно остановимся на лекарственных средствах, влияющих на афферентную иннервацию.
Лекарственные средства, влияющие на афферентную иннервацию, делятся на две группы:
1. ЛС, блокирующие чувствительные нервные окончания или препятствующие их возбуждению:
- анестезирующие средства (местные анестетики);
- вяжущие средства;
- адсорбирующие средства;
- обволакивающие средства.
2. ЛС, возбуждающие чувствительные нервные окончания:
- раздражающие средства.
Среди указанных групп препаратов наибольшее значение для практической медицины, несомненно, имеют анестезирующие средства.
Анестезирующие средства (местные анестетики) - (от греч. sthesis - боль, ощущение, а n - приставка отрицания) группа лекарственных средств, обладающих способностью обратимо ослаблять чувствительность окончаний афферентных нервных волокон и/или угнетать проведение возбуждения по афферентным нервным волокнам.
Местные анестетики классифицируют по двум важным признакам: по химическому строению и по виду вызываемой ими анестезии.
Классификация по химическому строению.
1. Сложные эфиры ароматических кислот:
- Бензокаин
- Прокаин
- Кокаин (в настоящее время не применяется)
- Тетракаин
2. Замещенные амиды ароматических кислот:
- Лидокаин
- Тримекаин
- Бупивакаин
- Артикаин
Сложные эфиры подвергаются гидролизу псевдохолинэстеразой крови и действуют в
течение 30 — 60 мин. Их эффект пролонгируют антихолинэстеразные средства (прозерин).
Следует отметить, что местная анестезия может быть нескольких видов. Так, выделяют поверхностную (терминальную), инфильтрационную и проводниковую анестезию. Все эти виды анестезии независимо от их особенностей обусловлены местным действием препаратов, поэтому зависят не от дозы, а от действующей концентрации анестетика.
Поверхностная (терминальная анестезия) характеризуется снижением чувствительности нервных окончаний на поверхности слизистой оболочки, раны или язвенной поверхности и достигается нанесением анестетика на поверхность кожи или слизистых в определенной концентрации. Достаточной эффективностью и низкой токсичностью при терминальной анестезии обладают бензокаин, бупивакаин, лидокаин, мепивакаин, пиромекаин, тримекаин. Средства для терминальной анестезии используются для обезболивания роговицы глаза при кератите, оперативных вмешательствах; полости рта для стоматологических воздействий; носовых ходов при интраназальной интубации, для прокола гайморовой пазухи; дыхательных путей при бронхоскопии, пищевода при зондировании, уретры при цистоскопии.
Бензокаин выпускается только в составе комбинированных лекарственных препаратов. Бензокаин - высокоактивный и малотоксичный анестетик. Однако он практически нерастворим в воде, что не позволяет использовать его в инъекционных лекарственных формах. Поэтому его используют только для терминальной анестезии. Применяется местно и внутрь. Местно (в виде мазей, паст, присыпок, ректальных свечей, спиртовых растворов) - при остром воспаление среднего уха, заболеваниях кожи, сопровождающихся зудом, геморрое и др. Внутрь (в виде порошков и таблеток) - при гастрите и язвенной болезни желудка и двенадцатиперстной кишки, болях в желудке, спазмах желудка.
Ректальные суппозитории "Релиф адванс" применяются для анальгезии при геморрое, трещинах заднего прохода и т.п. Кратность применения составляет до 4 раз в сутки.
Суспензия для приема внутрь "Алмагель-А" используется для лечения язвенной болезни желудка и двенадцатиперстной кишки, дуоденита, энтерита, колита, гастрита и т.д. Кратность приема суспензии составляет 3-4 раза в сутки за 30 минут до еды и перед сном.
Таблетки для приема внутрь "Беллалгин" и "Белластезин" применяются для лечения гиперацидного гастрита и спазмах гладкой мускулатуры органов желудочно-кишечного тракта. Кратность приема составляет 2-3 раза в сутки.
"Меновазин" представляет собой спиртовой раствор для наружного применения и используется при миалгиях, артралгиях, невралгиях и зудящих дерматозах. Кратность применения составляет 2-3 раза в сутки.
Кроме того, бензокаин входит в состав аэрозолей и таблеток для рассасывания, применяемых для лечения инфекционно-воспалительных заболеваний полости рта и горла "Стопангин 2А", "Гексорал табс", "Септолете плюс".
При инфильтрационной анестезии происходит последовательное пропитывание раствором анестетика кожи и более глубоких тканей, через которые пройдет операционный разрез. Инфильтрационная анестезия представляет собой анестезию чувствительных нервных окончаний и афферентных волокон. Для инфильтрационной анестезии используются новокаин, лидокаин, артикаин, бупивакаин, тримекаин.
Для пролонгирования местного действия и уменьшения резорбтивных эффектов к растворам местных анестетиков добавляют сосудосуживающие средства группы адреномиметиков — эпинефрин, фенилэфрин, ксилометазолин, нафтизин.
Бупивакаин выпускается в форме раствора для инъекций по 5 мг в 1 мл во флаконах по 4, 10 и 20 мл. Режим дозирования зависит от вида обезболивания. Используется для спинномозговой анестезия в хирургии; в абдоминальной хирургии - длительностью до 60 минут.; при блокадах тройничного нерва, крестцового, плечевого сплетений, срамного нерва, межреберная, каудальная анестезия и эпидуральная анестезия при кесаревом сечении; для анестезии при вправлении вывихов суставов верхних и нижних конечностей. Бупивакаин, длительно блокируя натриевые каналы, нарушает вход ионов натрия в клетки миокарда во время систолы. Это сопровождается недостаточностью сердечной деятельности. Бупивакаин может также вызывать желудочковую тахикардию.
Проводниковая анестезия определяется подавлением чувствительности по ходу афферентного нервного волокна и нарушением проведения болевых импульсов в ЦНС из региона, иннервируемого блокированным нервом. Ее используют в стоматологии, при ограниченных операциях в общехирургической практике, с целью блокады нервных стволов при заболеваниях, сопровождающихся болью (вагосимпатическая, межреберная, паранефральная блокады). Для проводниковой анестезии выбирают препараты с наименьшей токсичностью — новокаин, лидокаин, артикаин, бупивакаин, ропивакаин, тримекаин.
Артикаин выпускается в форме раствора для инъекций по 10, 20 и 40 мг в 1 мл в ампулах по 1, 2, 5, 10 или 20 мл, а также в виде раствора для инъекций в комбинации с эпинефрином. Применяется однократно в качестве анестетика для проведения хирургических и диагностических вмешательств, в акушерстве, при болевых синдромах. Побочные эффекты: головная боль, нарушение зрения и дыхания, судороги.
В педиатрической практике применяют проводниковую анестезию в сочетании с поверхностным наркозом. Это обеспечивает полное устранение боли, выключение сознания и рефлексов из операционного поля, вегетативную блокаду. Местные анестетики вызывают региональную миорелаксацию. При операции не развиваются типичные осложнения наркоза, укорачивается период
пробуждения.
Проводниковая анестезия включает в себя несколько частных случаев, а именно:
- спинномозговая (спинальная) анестезия - проводниковая анестезия на уровне спинного мозга (анестетики вводятся в субарахнаидальное пространство);
- эпидуральная (перидуральная) анестезия - проводниковая анестезия в пространстве над твердой мозговой оболочкой.
При этом блокируется проведение чувствительных импульсов по задним корешкам спинного мозга. Одновременно возникает региональная миорелаксация, не требующая искусственной вентиляции легких.
В настоящее время для спинномозговой анестезии применяют местные анестетики группы амидов — лидокаин, артикаин, бупивакаин, ропивакаин, тримекаин. Микрокатетерная техника позволяет пролонгировать обезболивание независимо от продолжительности действия анестетика.
Спинальная анестезия развивается через 2 — 10 мин, обеспечивает большую глубину сенсорного и моторного блока, для нее требуется в 10 — 15 раз меньше местного анестетика, чем для эпидуральной анестезии. Эпидуральная анестезия наступает спустя 30 — 40 мин. В некоторых случаях эпидуральной анестезии возникает мозаичное или одностороннее обезболивание вследствие анатомических особенностей эпидурального пространства.
Осложнением спинномозговой анестезии, особенно в ее спинальном варианте, является артериальная гипотензия, так как местные анестетики блокируют проведение эфферентных импульсов по преганглионарным симпатическим волокнам, входящим в состав передних корешков спинного мозга. Снижение АД наиболее выражено у больных с гиповолемией. При спинномозговой анестезии не исключен риск инфекции, травмы и ишемии спинного мозга.
Большинство анестезирующих средств обладают избирательностью в отношении того или иного вида местной анестезии. Поэтому данные препараты классифицируют в зависимости от вида вызываемой ими анестезии.
1. Средства для терминальной (поверхностной) анестезии:
- Бензокаин
- Тетракаин
2. Средства для инфильтрационной анестезии:
- Прокаин
- Тримекаин
- Артикаин
3. Средства для проводниковой анестезии:
- Тримекаин
- Артикаин
- Прокаин
- Тримекаин
- Бупивакаин (преимущественно для спинномозговой анестезии)
4. Средства для всех видов местной анестезии:
- Лидокаин
Механизм анестезирующего действия местных анестетиков заключается в том, что они конкурентно блокируют быстрые натриевые каналы на мембране нервных клеток, нарушая тем самым поступление ионов натрия внутрь клетки, и как следствие возбуждение нервной клетки. При этом важно понимать, что анестезирующие средства вызывают блокаду натриевых каналов только с внутренней стороны мембраны, проникнув внутрь клетки. В этой связи решающее значение для возникновения анестезирующего эффекта имеет pH (кислотность) тканевой среды, в которую вводится анестетик, поскольку от данного параметра зависит степень ионизации молекулы анестетика, а значит и его способность проникать внутрь клетки.
Любой импульс, возникающий в нейроне или передаваемый им по нервному волокну (аксону), в том числе и болевой (возникший при возбуждении болевых рецепторов), представляет собой потенциал действия (ПД). ПД, в свою очередь, это не что иное как изменение заряда клеточной мембраны во времени. В состоянии покоя клеточная мембрана нейрона внутри заряжена отрицательно. Это достигается благодаря тому, что все ионы могут проникнуть в клетку только через специальные белковые поры (каналы). В состоянии покоя каналы для положительно заряженных ионов натрия закрыты в отличие от каналов для отрицательно заряженных ионов хлора, которые могут проникать внутрь нейрона, обеспечивая разность потенциалов.
Потенциал действия нейрона.
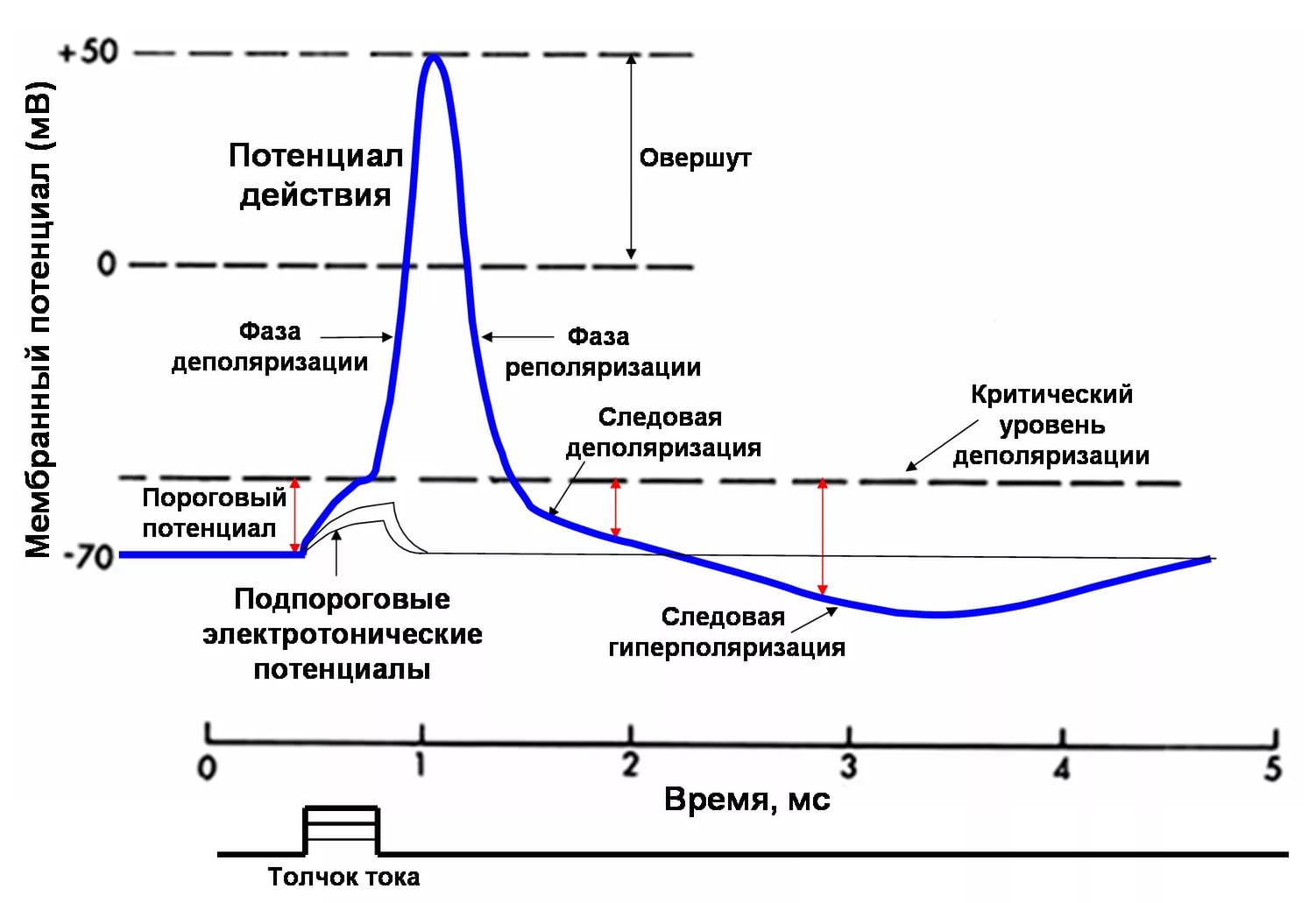
При воздействии какого-либо стимула (например, электрический ток) на мембране нейрона открываются "медленные" натриевые каналы, по которым ионы натрия по градиенту концентрации входят внутрь клетки. Заряд клеточной мембраны начинает увеличиваться. Но в это же время клетка включает натриевые насосы, выводящие ионы натрия наружу. Если стимул оказался достаточно слабым (подпороговые электрические потенциалы), благодаря работе натриевых насосов заряд клеточной мембраны возвращается в состояние покоя и ничего не происходит. Если импульс имеет достаточную силу (открывает много "медленных" натриевых каналов), заряд мембраны повышается до определенного уровня (критический уровень деполяризации), при котором открываются "быстрые" натриевые каналы. "Быстрые" каналы потенциалзависимы, т.е. открываются только при определенном заряде мембраны. При их открытии натрий входит в клетку практически мгновенно и в таком количестве, которое приводит к изменению заряда мембраны с отрицательного на положительный (деполяризация). Нейрон возбужден и это возбуждение он способен передать другому нейрону или клеткам исполнительного органа. При смене заряда мембраны натриевые каналы закрываются, и клетка включает натриевые и калиевые насосы, выводящие положительно заряженные ионы наружу (реполяризация), чтобы восстановить равновесное состояние покоя и подготовиться к воздействию следующего импульса. При этом насосы работают "с запасом" и выводят положительно заряженные ионы до изменения заряда мембраны ниже, чем он был в состоянии покоя (следовая гиперполяризация). В это время клетка становится невосприимчивой к раздражителям. Окончательное восстановление заряда мембраны достигается выключением ионных насосов и проникновением ионов калия внутрь клетки.
Напомню, что преодолеть мембранный барьер и попасть внутрь клетки могут только неионизированные липофильные вещества. В силу того, что практически все местноанестезирующие средства по своей химической структуре являются основными соединениями, липофильность они приобретают только в слабощелочной или нейтральной среде, а в кислой среде вещества ионизируются и становятся гидрофильными. Вследствие такой модификации они теряют способность проходить через мембраны, а значит, не способны блокировать натриевые каналы. Именно этой особенностью анестетиков объясняется отсутствие их действия в кислой среде при воспалении, гнойных ранах. Таким образом, местная анестезия может оказаться неэффективной при удалении зуба в случае тяжелого периодонтита.
Следует также отметить, что для повышения эффективности анестезии и снижения ее системной токсичности назначение анестетиков требует сочетания с вазоконстрикторами (норэпинефрин, эпинефрин и другие α-адреномиметики). Дело в том, что при сужении кровеносных сосудов в области введения анестезирующего средства уменьшается его всасывание в общий кровоток. В результате большее количество действующего вещества остается в месте применения (поэтому возрастает эффективность) и меньшее его количество распространяется по организму (снижается токсичность).
Резорбтивное действие местных анестетиков.
Местные анестетики (кроме кокаина) уменьшают возбудимость нейронов ЦНС, при этом угнетение тормозящих нейронов происходит в первую очередь. Действие местных анестетиков на головной мозг состоит из двух стадий: возбуждения и торможения. В стадии возбуждения, когда подавлена функция тормозящих нейронов, возникают беспокойство, тремор, клонико-тонические судороги. Для стадии торможения характерны сонливость, потеря сознания, угнетение дыхательного центра. В больших концентрациях местные анестетики сразу вызывают торможение, подавляя
одновременно функции всех нейронов.
При резорбтивном действии дикаина может наступить паралич дыхательного центра без предварительного возбуждения ЦНС.
Лидокаин и реже тримекаин и пиромекаин используют как противоаритмические средства при желудочковых формах тахиаритмии. Они не уменьшают проводимость, вызывают умеренную артериальную гипотензию.
Лидокаин выпускается в форме 1, 2 и 10% раствора для инъекций в ампулах по 2, 5 и 10 мл, в форме пластыря по 700 мг, 2 и 4% глазных капель, 10% спрея для местного применения, а также в виде 1, 2 и 5% геля для местного применения и в комбинации с другими лекарственными веществами в виде ушных капель, мазей, гелей, суспензий и таблеток для рассасывания. Пластырь наклеивается на 12 часов с последующим 12 часовым перерывом. Гель применяется для анестезии при проведении различных диагностических и лечебных процедур. Применение раствора в качестве анальгетического средства зависит от клинической ситуации. В качестве противоаритмического средства 10% раствор разводится до концентрации 2% физиологическим раствором и вводится внутривенно медленно. Глазные капли применяются 2-3 раза с интервалом 30 секунд перед проведением исследований или оперативным вмешательством на роговице или конъюнктиве. Спрей применяется для анестезии слизистых оболочек ротоглотки. Побочные эффекты: головокружение и головная боль, сонливость, судороги, зритедбные и слуховые нарушения, остановка дыхания, онемение языка, нарушение АД, тошнота, рвота, аллергические реакции.
Местные анестетики расширяют бронхи, угнетают перистальтику кишечника, расслабляют матку. Местные анестетики-эфиры вызывают у чувствительных больных аллергические реакции — дерматит, астматические приступы. Препараты группы амидов лишены этого недостатка, но в их растворы иногда добавляют консервант метилпарабен, обладающий свойствами аллергена.
Некоторые представители группы местных анестетиков имеют целый ряд важных индивидуальных особенностей.
Кокаин стал первым лекарственным средством, введенным в научную медицину для местного обезболивания. Применение кокаина гидрохлорида в медицине весьма ограничено, потому что, помимо выраженной местноанестезирующей активности, у препарата есть резорбтивное действие, которое проявляется сильным психостимулирующим эффектом. Возникает эйфория, беспокойство, психомоторное возбуждение, уменьшается ощущение утомления и голода и др. При хроническом употреблении кокаина развивается психическая лекарственная зависимость, получившая название кокаинизм. Симпатомиметическое действие кокаина проявляется и на периферии, в связи с чем применение данного препарата не требует сочетания с вазоконстрикторами. Учитывая вышесказанное, кокаина гидрохлорид применяется в медицине только в офтальмологической практике для поверхностной анестезии (в виде глазных капель и мази).
Тетракаин - высокоэффективное, но крайне токсичное анестезирующее средство. По силе действия превосходит кокаин в 10-12 раз, но при этом в 2-5 раз токсичнее. Поэтому в настоящее время тетракаин используется только в составе комбинированных лекарственных форм в виде спрея, пастилок и таблеток для рассасывания для лечения инфекционно-воспалительных заболеваний полости рта и глотки.
Прокаин - широко распространенный анестетик с умеренной анестезирующей активностью. Наряду с основным действием, имеет целый ряд резорбтивных эффектов, нашедших свое применение в медицине. После попадания в общий кровоток, прокаин проникает в ЦНС, где оказывает умеренное угнетающее влияние на кору и подкорковые структуры, в том числе на центры продолговатого мозга: центры n.vagus и сосудодвигательный центр. Кроме того, на периферии прокаин блокирует вегетативные ганглии. Совокупным следствием таких эффектов является ослабление парасимпатической и симпатической иннервации внутренних органов. Учитывая вышесказанное, прокаин может быть полезен при гипертонической болезни, спазме кровеносных сосудов, а также язвенной болезни желудка и двенадцатиперстной кишки. Показаниями для применения прокаина являются: инфильтрационная, проводниковая, эпидуральная и спинномозговая анестезия, внутрикостная анестезия, анестезия слизистых оболочек (в ЛОР-практике); внутривенно для купирования болевого синдрома различного генеза; внутримышечно для растворения пенициллина с целью удлинения срока его действия; ректально при геморрое, спазмах гладкой мускулатуры кишечника, анальных трещинах.
Прокаин выпускается в форме 0,25%, 0,5% и 2% раствора для инъекций в ампулах по 2,5 мл, 5 мл и 10 мл, 0,25% и 0,5% раствор - во флаконах по 100, 200 и 400 мл, в форме ректальных суппозиторий по 100 мг, а также входит в состав комбинированных лекарственных средств. Режим дозирования подбирается индивидуально. Побочные эффекты: артериальная гипотензия, головокружение, аллергические реакции.
Вяжущие средства - это химические соединения, обладающие способностью при взаимодействии с белком клеток, тканей, тканевых жидкостей организма вызывать поверхностную коагуляцию белков и образовывать плотные альбуминаты, предохраняющие нервные окончания от раздражения и дальнейшего появления боли. При этом поверхность ткани уплотняется, секреция желез понижается, сосуды суживаются, уменьшается выход лейкоцитов из кровеносного русла в ткани, что положительно сказывается на уменьшении воспалительного процесса. Эффект вяжущих средств непродолжителен и обратим, поэтому их применяют длительно и повторно.
Классификация вяжущих средств:
1. Органические вяжущие средства (танин, кора дуба (содержит танин), танальбин, трава зверобоя, листья шалфея, плоды черемухи и др.).
2. Неорганические вяжущие средства (соли тяжелых металлов):
- висмута нитрат основной
- висмута цитрат
- ксероформ
- квасцы алюмокалиевые
- жидкость Бурова (алюминия ацетат)
- цинка сульфат
- меди сульфат
- серебра нитрат
- протаргол
Органические вяжущие средства применяются при воспалении желудка, кишечника, желудочно-кишечных кровотечениях, при катарах слизистых оболочек рта, горла и глотки. Наружно их назначают для лечения ожогов кожи, для полоскания полости рта и горла при стоматитах, фарингитах, ларингитах и т.д.
Соли тяжелых металлов, помимо вяжущего действия, имеют и другие виды фармакологической активности, которые напрямую зависят от действующей концентрации вещества.
Спектр фармакологической активности солей тяжелых металлов.
| Действующая концентрация | Эффект | Механизм эффекта | Цель применения |
| 0,5-1 % | Антибактери альный | Блокада тиоловых ферментов метаболизма бактериальной клетки | Антисептические мероприятия |
| 1-2% | Вяжущий | Обратимая коагуляция поверхностных белков с образованием защитной пленки | Воспалительные поражения слизистых поверхностных тканей |
| 3-5 % | Раздражаю щий | Химическая стимуляция нервных окончаний | Отвлекающее действие |
| 5-10% | Прижигаю щий | Необратимая коагуляция белков, проникающая в глубокие слои ткани | Удаление папиллом, бородавок и др. новообразований на коже |
Адсорбирующие средства - это тончайшие измельченные нерастворимые индифферентные порошки с большой адсорбционной способностью, связывающие на своей поверхности различные вещества, уменьшая всасывание последних, механически защищая слизистую оболочку и находящиеся в ней окончания чувствительных нервов.
К числу адсорбирующих средств относятся:
- тальк
- уголь активированный
- карболен
- белая глина
- кремния диоксид коллоидный
- полиметилсилоксан и др.
Адсорбирующие средства в медицине применяются для защиты
поврежденной поверхности кожи от механического раздражения при ранах, ушибах, ожогах и т.д.; для детоксикации при отравлении химическими соединениями; при диарее, метеоризме.
Обволакивающие средства, покрывая слизистые оболочки и воспаленные ткани, препятствуют раздражению окончаний чувствительных нервов.
Собственно процесс обволакивания осуществляется коллоидными растворами, которые образуются в результате набухания высокомолекулярных органических соединений растительного происхождения (крахмал и др.) в горячей воде. Эти вязкие субстанции не пропускают через себя раздражающие вещества, что позволяет избежать контакта последних с пораженной поверхностью. К обволакивающим средствам относятся крахмальная слизь, слизь из семян льна и др. Их применяют при воспалительных процессах желудочно-кишечного тракта, а также с веществами, которые обладают раздражающими свойствами.
Раздражающие средства - это вещества, стимулирующие чувствительные нервные окончания (болевые, температурные, химические) и вызывающие местные и рефлекторные реакции, которые определяют фармакологический эффект препарата (улучшаются кровоснабжение и трофика тканей, ослабляется боль).
Эти средства возбуждают рецепторы, расположенные в коже
и слизистых оболочках, импульсы с которых поступают в ЦНС.
Этим вызывается реакция со стороны органов, имеющих сопряженную иннервацию в ЦНС с участками, подвергшимися действию раздражающих веществ, в результате чего улучшается кровоснабжение органа и его трофика, что благоприятно сказывается при различных воспалительных процессах. Эффект раздражающих средств усиливает и местная реакция, которую они вызывают и которая связана с выделением биологически активных веществ.
Местное действие раздражающих средств проявляется болью, гиперемией и отеком на месте нанесения препаратов. Раздражающие средства непосредственно возбуждают нервные окончания, а также освобождают гистамин, серотонин, брадикинин и простагландины. Гиперемия развивается не только в области приложения раздражающих средств, но и распространяется на прилежащие участки кожи.
При длительном контакте сильных раздражающих средств с кожей, попадании их на слизистые оболочки и поврежденные участки кожи появляются сильная боль и воспалительная реакция.
Раздражающие средства применяют при невралгии, радикулите, люмбаго, ишиасе, артрите, миозите, бурсите, тендовагините, травмах мышц и связок, нарушении периферического кровообращения, трахеите, бронхите. Иногда раздражающие средства втирают в кожу для разогревания мышц перед физическими упражнениями и спортивными соревнованиями.
Подразделяются на несколько групп: средства, содержащие эфирные масла; горечи; средства, содержащие аммиак; синтетические раздражающие средства.
Ментол (Mentholum).
Оказывает избирательное возбуждающее влияние на холодовые рецепторы, вызывает ощущение холода, сменяемое местной анестезией. Раздражение ментолом холодовых рецепторов полости рта сопровождается седативным, противорвотным эффектами и рефлекторным расширением коронарных сосудов при стенокардии. Применяют наружно как болеутоляющее (отвлекающее) средство, внутрь в качестве успокаивающего средства ("Валидол"). Входит в состав многих комбинированных препаратов ("Пектусин", "Меновазин", "Эфкамон", "Капли зубные").
Горчичиник— бумага, покрытая тонким слоем обезжиренной горчицы. После смачивания горчичника водой при температуре 37 — 40 °С высвобождается активное раздражающее вещество эфирного горчичного масла (аллилизотиоцианат). Обладают сильным раздражающим действием и применяются при заболеваниях органов дыхания, невралгиях, миалгиях и др.
Горечи (amara) — препараты растительного происхождения, содержащие вещества, обладающие сильным горьким вкусом. Раздражая вкусовые рецепторы слизистых оболочек полости рта и языка, они вызывают рефлекторным путем усиление секреции желудочного сока, повышение аппетита, улучшение пищеварения. Назначают при гипоацидных и хронических атрофических гастритах, при анорексии на почве нервных заболеваний, после перенесенных оперативных вмешательств.
Раствор аммиака 10%.
Применяется как средство скорой помощи для возбуждения дыхания и выведения больных из обморочного состояния, иногда - внутрь в качестве рвотного средства (по 5—10 капель на 100 мл воды). При укусах насекомых — наружно в виде примочек.
К мазям раздражающего действия относят "Эфкамон", "Капсикам", "Финалгон", "Апизартрон". Эти препараты применяются как отвлекающие и улучшающие трофику тканей при заболеваниях опорно-двигательного аппарата (миалгии, невралгии, боли в суставах, ревматизм).
Лекция №10.
Средства, влияющие на M - N -холинорецепторы.
Все функции в организме человека находятся под контролем центральной и периферической нервных систем. Центральный отдел нервной системы включает головной и спинной мозг, а периферический - вегетативную и соматическую нервную системы. Вегетативная нервная система иннервирует внутренние органы, сосуды и железы и функционирует автономно (непроизвольно). Соматическая нервная система обеспечивает произвольную работу скелетной мускулатуры. Эфферентный путь соматической нервной системы представлен одним нейроном, тогда как вегетативные нервы имеют двухнейронную структуру. Вегетативные нервы прерываются (образуют синаптическое соединение) в нервных узлах (ганглиях), поэтому состоят из двух волокон (преганглионарного и постганглионарного). Отростки первых нейронов, расположенных в центральном отделе нервной системы, направляются к ганглиям и называются преганглионарными. Ганглии представляют собой скопление тел вторых нейронов, образующих контакты (синапсы) с преганглионарными нейронами. Отростки вторых нейронов разветвляются в иннервирумых органах и называются постганглионарными.
Схематическое изображение эфферентной иннервации:
| а/х |
| Двигательная иннервация |
| н |
| а/х |
| н |
| Адреналин |
| а/х |
| н |
| н/а |
| α, β |
| Мозговое в-во надпочечников |
| Симпатическая иннервация |
| а/х |
| н |
| а/х |
| м |
| Парасимпатическая иннервация |
| - нейрон |
| - клетки эффекторного органа |
| - эффекторный орган |
а/х – медиатор ацетилхолин
н/а – медиатор норадреналин
н – никотиночувствительные холинорецепторы
м – мускариночувствительные холинорецепторы
α, β - адренорецепторы
Симпатическая и парасимпатическая системы часто оказывают противоположное влияние на функции органов и систем. Именно на управлении балансом между этими влияниями основаны правила применения ЛС, действующих в области окончания эфферентных нервов.
Симпатические нервные волокна берут начало от специальных клеток грудного и поясничного отделов спинного мозга. Парасимпатические нервные волокна берут начало от клеток стволовой части головного мозга и от клеток крестцовой части спинного мозга. Парасимпатические нервы входят в состав трех пар черепно-мозговых нервов: глазодвигательного (иннервирует внутренние мышцы глаза), лицевого (иннервирует слюнные железы), блуждающего (иннервирует бронхи, сердце и ЖКТ). Крестцовый отдел парасимпатической нервной системы иннервирует нижний отдел кишечника и тазовые органы.
Ганглии парасимпатических нервов располагаются в основном вблизи иннервируемых органов или внутри них, а симпатические – рядом с местом выхода из ЦНС, образуя симпатический ствол.
Преганглионарные и постганглионарные волокна контактируют между собой и клетками иннервируемых органов посредством специального структурного образования (синапса).
Межнейрональная передача импульса в ганглиях и в нейроэффекторных синапсах
осуществляется через синапсы с помощью биологически активных
веществ - медиаторов.
Схема работы холинергического синапса:
| Передача возбуждения |
| Состояние покоя |

В синапсах различают две контактирующие мембраны:
- передающая пресинаптическая мембрана аксона;
- воспринимающая постсинаптическая мембрана нервной клетки (тело, дендрит, аксон) или клетки исполнительного органа.
Между пресинаптической и постсинаптической мембранами находится синоптическая щель шириной 20 — 40 нм. Она заполнена полисахаридным гелем, имеет каналы для диффузии медиатора. Синапс ограничен соединительной тканью, препятствующей выходу медиатора в кровь. Низкомолекулярные медиаторы синтезируются в окончаниях аксона и депонируются в связи с белком в синаптических пузырьках.
Основным медиатором в симпатических и парасимпатических вегетативных ганглиях является ацетилхолин. В зависимости от медиатора, выделяющегося в нейроэффекторных синапсах, вегетативную нервную систему подразделяют на холинергическую, или парасимпатическую (медиатор - ацетилхолин), и адренергическую, или симпатическую (медиатор - норадреналин).
Особо отметим, что иннервация мозгового вещества надпочечников осуществляется по однонейронному пути с участием только преганглионарных (холинергических) нейронов. Обусловлено это тем, что хромаффинные клетки эмбриогенетически родственны нейронам симпатических ганглиев. При раздражении этих нейронов из клеток мозгового вещества надпочечников высвобождается адреналин.
Холинергические лекарственные средства.
В холинергических синапсах передача возбуждения осуществляется с помощью ацетилхолина. Холинергические синапсы локализованы в ЦНС (ацетилхолин регулирует моторику, пробуждение, память, обучение), а также в вегетативных ганглиях, мозговом слое надпочечников, каротидных клубочках, скелетных мышцах и внутренних органах, получающих постганглионарные парасимпатические волокна. Ацетилхолин депонируется в синаптических пузырьках и выделяется при деполяризации пресинаптической мембраны (импульсе). Выделившийся ацетилхолин достигает рецепторов, находящихся на постсинаптической мембране и возбуждает их (соединяется с рецептором, вызывая временное изменение его структуры). Рецепторы представляют собой сложные белковые молекулы, встроенные в клеточную мембрану. Результат возбуждения рецепторов различен. Если рецепторы находятся на постсинаптической мембране нейрона (синапс предназначен для межнейрональной передачи возбуждения) или клетках скелетной мышцы, то они функционально связаны с ионными каналами и возбуждение таких рецепторов приведет к открытию натриевых ионных каналов и деполяризации постсинаптической мембраны. Если же рецепторы находятся на постсинаптической мембране исполнительных органов (сердце, бронхи и др.), то тогда их возбуждение приведет к передаче изменения структуры рецепторов внутрь клетки и активации определенной ферментной системы, что и вызовет определенные изменения в клетках органа, т.е. изменит работу органа в целом.
Такой механизм определяет работу холин- и адренергических синапсов.
Весь ацетилхолин, находящийся в синаптической щели, подвергается гидролизу ферментом ацетилхолинэстеразой с образованием холина и уксусной кислоты. Холин в тысячи раз менее активен по сравнению с ацетилхолином; 50 % его молекул подвергается нейрональному захвату (возвращается в пресинаптическую мембрану) и вновь участвует в синтезе ацетилхолина. Уксусная кислота утилизируется в цикле трикарбоновых кислот. Ацетилхолинэстераза необходима для регуляции работы синапса (для устранения эффектов перевозбуждения рецепторов и необратимого изменения работы органов).
ЛС, возбуждающие рецепторы (вызывающие те же эффекты, что и медиатор) называют миметиками, а блокирующие их (нарушающие передачу возбуждения) – литиками.
В соответствии с химической чувствительностью холинорецепторы классифицируют на мускариночувствительные (М) и никотиночувствительные (N). М-холинорецепторы возбуждаются ядом мухомора мускарином и блокируются атропином. Они локализованы в нервной системе и внутренних органах, получающих парасимпатическую иннервацию (вызывают угнетение сердца, сокращение гладких мышц, повышают секреторную функцию экзокринных желез.
Выделяют несколько типов М-холинирецепторов:
1. М1-холинорецепторы ЦНС (лимбическая система, базальные ганглии, ретикулярная
формация) и вегетативных ганглиев;
2. М2-холинорецепторы сердца (снижают частоту сердечных сокращений, атриовентрикулярную проводимость и потребность миокарда в кислороде, ослабляют сокращения предсердий);
3. М3-холинорецепторы:
- гладких мышц (вызывают сужение зрачков, спазм аккомодации, бронхоспазм, спазм
желчевыводящих путей, мочеточников, сокращение мочевого пузыря, матки, усиливают перистальтику кишечника, расслабляют сфинктеры);
- желез (вызывают слезотечение, потоотделение, обильное отделение жидкой, бедной белком слюны, бронхорею, секрецию кислого желудочного сока).
Внесинаптические М3-холинорецепторы находятся в эндотелии сосудов и регулируют
образование сосудорасширяющего фактора — окиси азота (NО).
N-холинорецепторы возбуждаются алкалоидом табака никотином в малых дозах, блокируются никотином в больших дозах.
N-холинорецепторы находятся в симпатических и парасимпатических ганглиях, каротидном клубочке, мозговом веществе надпочечников, нервно-мышечных синапсах и ЦНС. N-холинорецепторы вегетативных ганглиев и N-холинорецепторы скелетных мышц характеризуются разной чувствительностью к лекарственным средствам, что дает возможность избирательно заблокировать ганглии (ганглиоблокаторы) или нервно-мышечную передачу (курареподобные препараты).
В организме человека преобладают М-холиностимулирующие эффекты ацетилхолина.
Классификация холинергических лекарственных средств:






