Рассмотрим поведение слабого электролита в растворе: КА ↔ К+ + А-.
Запишем константу равновесия (ионизации):  введем обозначение:
введем обозначение:
С - исходная молярная концентрация электролита;
[KA] - равновесная концентрация после распада части молекул электролита на ионы;
a - степень диссоциации.
[K+] = aC; [A-] = aC; [KA] = C - aC = C(1 - a)
Подставим в константу ионизации:
 ,
,
или, если учесть, что a → 0, то Кион. = a2С, откуда
a2 = Кион./С; 
полученное выражение называют законом разведения Оствальда. Он связывает константу ионизации и степень диссоциации. Физический смысл закона: с разбавлением раствора (уменьшением его концентрации) степень диссоциации увеличивается. Чем сильнее разбавляют слабый электролит, тем больше его степень диссоциации (a).
4.2. Ионизация воды. Ионное произведение воды.
Водородный и гидроксильный показатели (рН и рОН)
Вода – очень слабый электролит. Запишем уравнение ионизации воды: Н2О + Н2О ↔ Н3О+ + ОН-
Или упрощенно: Н2О ↔ Н+ + ОН-
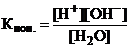 .
.
Известно, что при температуре 22-25оС в 1 л на ионы распадается 10-7 моль молекул Н2О. Следовательно, [H+] = [OH-] = 10-7 моль/л. Концентрацию молекул воды можно считать величиной постоянной, равной: [H2O] = 1000/18 = 55,56моль/л. Следовательно, константа ионизации воды при 22-25оС будет равна Ки= 1,82·10-16.
Произведение равновесных концентраций ионов Н+ и ОН- называется ионным произведением воды:
КW = [H+][OH-]
КW = 10-7∙10-7 = 10-14. КW = 10-14 при Т = 22-25оС.
Характер среды в водном растворе любого вещества определяется тем ионом Н+ или ОН-, концентрация которого преобладает.
[H+] = [OH-], т.е. [H+] = 10-7 моль/л - среда нейтральная;
[H+] > [OH-], т.е. [H+] > 10-7 моль/л - среда кислая;
[H+] < [OH-], т.е [H+] < 10-7 моль/л - среда щелочная.
Важно отметить, что в любом водном растворе – нейтральном, кислотном, щелочном имеются водородные и гидроксильные ионы. При этом произведение концентрации этих ионов величина постоянная, равная ионному произведению воды.
Зная ионное произведение воды и концентрацию одного из ионов, можно вычислить концентрацию другого:
 .
.
Водородный показатель
На практике принято оценивать ионное равновесие в водных растворах значением водородного показателя рН.
Водородным показателем рН называют отрицательный десятичный логарифм концентрации ионов водорода в водном растворе. рН = -lgСН+.
Гидроксильным показателем рОН называют отрицательный десятичный логарифм концентрации ионов ОН- в водном растворе. рОН = -lg СОН-.
Ранее было показано, что в любом водном растворе при 22-25оС: СН+∙СОН- = 10-14.
Логарифмируя это выражение, получаем:
-lg (CH+∙COH-) = -lg10-14.
Десятичный логарифм – это показатель степени, в которую нужно возвести 10:
1g10x = х, lg10-x = -х.
Логарифм произведения равен сумме логарифмов:
-lgCH+ -lgCOH- = 14
рН + рОН = 14 Т = 22-25оС
рН + рОН = 13,6 при 37оС
рОН = 14 – рН или рН = 14 – рОН при 22-25оС
выразим рН слабого электролита, если даны Кион., a, Ск-ты или Сосн. или отрицательные логарифмы этих величин.
Для слабой кислоты:
СН+ = aСк
-lgСН+ = -lga - lgСк
рН = рa + рСк-ты, где р = -lg, следовательно
рa = -lga; рСк = - lgСк
или через константу ионизации:
СН+ = aСк-ты.
По закону разведения Оствальда: 
Подставим a: 
Внесем Ск-ты под корень: 

Возьмем отрицательный логарифм этого выражения. Получим для слабой кислоты:
рН = ½ (рК + рСк-ты),
где рК = -lgК; рСк-ты = -lgСк-ты.
Для сильной кислоты:
a = 1 и уравнение рН = рa + рСк-ты, т.к. рa = -lga = -lg1 = 0 преобразуется к виду:
рН = рСк-ты
Для слабого основания
СОН- = aСосн.
-lgCOH- = -lga – lgСосн.
рОН = рa + рСосн., где рa = -lga; рСосн. = - lgСосн.
или через константу ионизации:
СОН- = aСосн.
 Логарифмируя это выражение, получим:
Логарифмируя это выражение, получим:
рОН = ½ (рК + рСосн.) - для слабого основания,
где рОН = -lgCOH-
рК = -lgК
рСосн. = -lgСосн.
Для сильного основания
a = 1, значит lga = 0, рОН = рСо.
Для наглядности приведем шкалу значений рН и СН+ при 22оС.

Водородный показатель широко используется для характеристики кислотно-основных свойств различных биологических жидкостей. Значение рН среды оказывает влияние на физико-химические свойства и биологическую активность белков, ферментов, нуклеиновых кислот.
Значение рН некоторых биологических жидкостей
организма при 37оС
| Биологическая жидкость | Кровь | Желудочный сок | Кишечный сок | Слюна | Желчь |
| Значение рН | 7,36 ± 0,05 | 1,0 ± 0,1 | 6,4 ± 0,4 | 6,6 ± 0,3 | 6,9 ± 0,4 |
Как видно из таблицы рН различных жидкостей изменяется в довольно широких пределах в зависимости от их природы.
При патологических процессах наблюдается нарушение кислотно-щелочного равновесия: смещение рН биологической жидкости в кислую область, получило название ацидоз, а в щелочную область – алкалоз.






