Выберите один правильный ответ
1. буфернОЙ системОЙ I типа ЯВЛЯЕТСЯ
1) пиридиновая
2) ацетатная
3) аммиачная
2. буфернОЙ системОЙ II типа ЯВЛЯЕТСЯ:
1) фосфатная
2) ацетатная
3) аммиачная
4) гемоглобиновая
3. буфернОЙ системОЙ II типа ЯВЛЯЕТСЯ
1) фосфатная
2) гидрокарбонатная
3)гемоглобиновая
4) анилиновая
4. БУФЕРНЫЕ СВОЙСТВА МОЖЕТ ПРОЯВЛЯТЬ СМЕСЬ ЭЛЕКТРОЛИТОВ
1) NaHCO3, CO2 ∙H2O
2) NH3 ∙H2O, NaCl
3) Na3PO4, K3PO4
4) CH3COOH, HNO3
5. к буферным системам первого типа относит-ся Каждая из двух буферных систем
1) аммиачная и гемоглобиновая
2) белковая и фосфатная
3 ) оксигемоглобиновая ипиридиновая
4) фосфатная и анилиновая
6. БУФЕРНЫЕ СВОЙСТВА МОЖЕТ ПРОЯВЛЯТЬ СМЕСЬ ЭЛЕКТРОЛИТОВ
1) КСl, СН3СООК
2) СН3СООН, СН3COONa
3) КСl, НСl
4) Na2СO3, NaOH
7. к буферным системам ВТОРОГО типа относит-ся Каждая из двух буферных систем
1) аммиачная и пиридиновая;
2) гемоглобиноваяи оксигемоглобиновая
3 ) фосфатная и аммиачная
4) белковая и анилиновая
8. буферная система второго типа состоит из
1) слабого основания и соли этого основания и сильной кислоты
2) сильного основания и соли этого основания и сильной кислоты
3) сильного основания и соли этого основания и слабой кислоты
4) слабой кислоты и соли этой кислоты и сильного основания
9. К буферным системам 1 типа не относится
1) аммиачная 2) гемоглобиновая
3) белковая 4) фосфатная
10. буферная система первого типа состоит из
1) сильного основания и соли этого основания и сильной кислоты
2) слабой кислоты и соли этой кислоты и сильного ос-нования
3) слабого основания и соли этого основания и сильной кислоты
4) сильной кислоты и соли этой кислоты и сильного ос-нования
11. Водородный показатель гидрокарбонатного буфера, состоящего из 50 мл с концентрацией 0,2 моль/л раствора  и 100 мл с концентрацией 0,1 моль/л раствора
и 100 мл с концентрацией 0,1 моль/л раствора  РАВЕН
РАВЕН
1) 8,2 2) 5,8 3) 6,4 4) 6,8
12. Водородный показатель фосфатной буферной системы 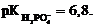 , состоящей из 100 мл раствора гидрофосфата натрия с концент-рацией 0,03 моль/л и 100 мл раствора дигидро-фосфата натрия с концентрацией 0,3 моль/л РАВЕН
, состоящей из 100 мл раствора гидрофосфата натрия с концент-рацией 0,03 моль/л и 100 мл раствора дигидро-фосфата натрия с концентрацией 0,3 моль/л РАВЕН
1) 7,8 2) 6,9 3) 5,8 4) 6,8
13. Водородный показатель оксигемоглобино-вой буферной системы 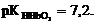 , состоя-щей из 50 мл раствора
, состоя-щей из 50 мл раствора  с концентрацией 1 моль/л и 5 мл раствора
с концентрацией 1 моль/л и 5 мл раствора  с концентра-цией 1 моль/л.
с концентра-цией 1 моль/л.
1) 8,12 2) 7,2 3) 6,2 4) 8,2
14. Водородный показатель фосфатной буферной системы РАССЧИТЫВАЕТСЯ ПО ФОРМУЛЕ
1) рН = рК + lg 
2) 
3) рН = ½ (рКк-ты + рС)
4) рН = рα + рС
15. ФОРМУЛОЙ ДЛЯ РАСЧЕТА ВодороднОГО показа-телЯ буферного раствора II типа ЯВЛЯЕТСЯ
1) 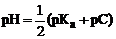
2) 
3) 
4) 
16. Водородный показатель аммиачной буфер-ной системы  , состоящей из
, состоящей из
100 мл раствора  с концентрацией
с концентрацией
0,2 моль/л (0,2М) и 10 мл раствора 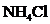 с кон-центрацией 0,2 моль/л (0,2М) РАВЕН
с кон-центрацией 0,2 моль/л (0,2М) РАВЕН
1) 10,26 2) 3,74 3) 8,26 4) 5,74
17. Водородный показатель анилиновой буферной системы  , состоя-щей из 50 мл раствора
, состоя-щей из 50 мл раствора  с кон-центрацией 0,2 моль/л (0,2М) и 50 мл раствора
с кон-центрацией 0,2 моль/л (0,2М) и 50 мл раствора  с концентрацией 0,02 моль/л (0,02М) РАВЕН
с концентрацией 0,02 моль/л (0,02М) РАВЕН
1) 10,38 2) 8,38 3) 4,62 4) 5,62
18. Водородный показатель аммиачной буфер-ной системы  , состоящей из 20 мл 0,1М
, состоящей из 20 мл 0,1М  и 100 мл 0,2 М
и 100 мл 0,2 М 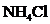 .
.
1) 10,24 2) 8,24 3) 5,76 4) 3,76
19. ФОРМУЛОЙ ДЛЯ РАСЧЕТА ВодороднОГО пока-зателЯ АММИАЧНОЙ БУФЕРНОЙ СИСТЕМЫ ЯВЛЯЕТСЯ
1) 
2) pH=14- 
3) рН = ½ (рКосн+ рС)
4) рН = рα + рС
20. роль протолитической кислоты В гидрокарбо-натной буферной системе выполняет
1)  2)
2)  3) H2CO3
3) H2CO3
21. роль протолитического основания В фосфат-ной неорганической системе выполняет
1)  2)
2)  3)
3)  4)
4) 
22. При добавлении постороннего сильного основания к аммиачной буферной системе протекает процесс
1) 
2) 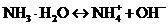
3) 
4) NH4+ +OH-  NH3·H2O
NH3·H2O
23. роль протолитической кислоты В фосфатной неорганической буферной системе выполняет:
1) H3PO4 2 ) Na2HPO4 3) NaH2PO4 4) Na3PO4
24. При добавлении постороннего сильного основания к гемоглобиновой буферной системе протекает процесс
1) H3O+ + Hb- ↔ H2O + HHb
2) HHb + OH- ↔ Hb- + H2O
3) HHb + H2O ↔ Hb- + H3O+
4) Hb- + H2O ↔ HHb + OH-
25. роль протолитической кислоты В аммиачной буферной системе выполняет
1) NH3∙H2O 2) NH4Cl 3) NH3 4) H2O
26. При добавлении посторонней сильной кис-лоты к аммиачной буферной системе протекает процесс
1) NH4+ + OH- ↔ NH3∙H2O
2) NH4+ + H2O ↔ NH3∙H2O + H+
3) H3O+ + NH3∙H2O ↔ NH4+ + 2H2O
4) NH3∙H2O ↔ NH4+ + OH-
27. роль протолитической кислоты В оксигемо-глобиновой буферной системе выполняет
1) KHb 2 ) HHbO2 3) HHb 4) KHbO2
28. При добавлении посторонней сильной кисло-ты к фосфатной буферной системе протекает процесс:
1) OH- + H2PO4- ↔ H2O + HPO42-
2) H3O+ +H2PO4- ↔ H3PO4 + H2O
3) H3O+ + HPO42- ↔ H2O + H2PO4-
4) OH- + HPO42- ↔ H2O + PO43-
29. роль протолитического основания В гидро-карбонатной буферной системе выполняет:
1) H2СО3 2 ) NаНСО3 3) Na2СО3 4) Н2О
30. При добавлении постороннего сильного основания к гидрокарбонатной буферной системе протекает процесс
1) Н2СО3 + ОН- ↔ НСО3- + Н2О
2) НСО3- + ОН- ↔ СО32- + Н2О
3) Н3О- + ОН- ↔ 2Н2О
4) НСО3- + Н3О+ ↔ Н2СО3 + Н2О
31. К аммиачной буферной системе объемом 30 мл добавили 3 мл 0,1 М НСl. При этом рН изменился на 0,1. Буферная емкость по кислоте (В МОЛЬ ЭКВ/Л) равна
1) 0,01 2) 0,1 3) 0,09 4) 10
32. К гидрокарбонатной буферной системе объемом 50 мл добавили 5 мл 1 М NaOH. При этом рН изменился на 0,1. Буферная емкость по основанию (В МОЛЬ ЭКВ/Л) равна
1) 0,01 2) 0,1 3) 1 4) 10
33. Для ацетатной буферной системы, состоя-щей из 100 мл 0,1 М  и 100 мл 0,2 М
и 100 мл 0,2 М 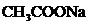
1) Bk>Bo
2) 
3) Bk=Bo
34. буферное отношение для оксигемоглоби-новой буферной системы, если она обладает большей буферной емкостью по кислоте
1)  2)
2)  3)
3) 
35. буферное отношение для аммиачной буферной системы, если она обладает большей буферной емкостью по кислоте
1) 
2) 
3) 
36. Для ацетатной буферной системы С буфернЫМ отношениеМ 
1)  2) Bk < Bo 3)
2) Bk < Bo 3) 
37. Для гидрокарбонатной буферной системы, обладающей большей емкостью по основанию, чем по кислоте справедливо соотношение:
1) nс/nк > 1 2) nc/no > 1 3) nc/nк < 1 4) nc/nк = 1
38. При равных концентрациях компонентов буфера большей емкостью по основанию обладает ацетатная буферная система
1) 200 мл CH3COOH; 100 мл CH3COONa
2) 100 мл СН3СООН; 200 мл СН3СООNa
3) 150 мл СН3СООН; 150 мл СН3СООNa
4) 200 мл СН3СООН; 300 мл СН3СООNa
39. Для фосфатной буферной системы, обладающей большей емкостью по кислоте, чем по основанию справедливо соотно-шение
1) nс/nк < 1 2) nc/no < 1 3) nc/no = 0 4) nc/nк >1
40. При равных концентрациях компонентов буфера большей емкостью по кислоте обладает ацетатная буферная система
1) 200 мл CH3COOH; 100 мл CH3COONa
2) 100 мл СН3СООН; 200 мл СН3СООNa
3) 150 мл СН3СООН; 150 мл СН3СООNa
4) 300 мл СН3СООН; 200 мл СН3СООNa
41. Большей емкостью по кислоте обладает система
1) 100 мл Н2СО3 С = 0,1 М; 200 мл NaHCO3 С = 0,1 М
2) 200 мл Н2СО3 С = 0,2 М; 200 мл NaHCO3 С = 0,1 М
3) 100 мл Н2СО3 С = 0,1 М; 50 мл NaHCO3 С = 0,1 М
4) 100 мл Н2СО3 С = 0,1 М; 50 мл Na2НРО4 С = 0,2 М
42. Для аммиачной буферной системы, состо-ящей из равных объемов 0,1 М раствора NH3∙H2O и 0,2 М раствора NH4Cl
1) Во < Вк 2) Вк = Во 3) Вк < Во.
43. Возможное ЗНАЧЕНИЕ рН Для ацетатной буферной системы (рКа=4,76)
1) 3 2) 5 3) 6 4) 8
Ответы к тесту на стр. 224






