1.1. Единицы измерения
При решении задач по теме «Осмос» используются две системы единиц: СИ международная система измерений и СГСЕ – советская государственная система единиц.
| Система единиц | Давление: Р – газов π – жидкостей | Объем, V | Молярная концентрация, С | Темпера-тура, Т | Универсал. газовая постоянная, R |
| СИ | Па | м3 | моль/м3 | К | 8,31 Дж/моль∙К |
| СГСЕ | атм | л | моль/л | К | 0,082 л∙атм/моль∙К |
Примечание: Па = Н/м2; Дж = Н∙м; 1 атм = 101,3 кПа = 101300 Па = 760 мм рт.ст.
Для того чтобы перевести температуру в Кельвины (К) нужно к температуре в оС прибавить 273, т.е. ОоС = 273 К: Т(К) = (tоС + 273)К
Переходить из одной системы единиц в другую не обязательно. Достаточно перевести все имеющиеся в задаче данные в ту систему единиц, в которой дано давление. Если давление дано в Па (Н/м2), то объем берется в м3, молярная концентрация в моль/м3, температура переводится в К и берется универсальная газовая постоянная R, равная 8,31 Дж/моль∙К. Если давление дано в атмосферах, то объем берется в литрах, молярная концентрация в моль/л и универсальная газовая постоянная R берется равной 0,082 л∙атм/моль∙К. Если давление берется в мм рт.ст., то для расчета берется универсальная газовая постоянная R = 82,4 л∙мм рт.ст./моль∙К.
1.2. Законы осмотического давления
Осмос – это проникновение молекул растворителя через полупроницаемую мембрану из раствора с низкой концентрацией в раствор с высокой концентрацией. Изучение законов осмотического давления выявило их полную аналогию с газовыми законами.
Вант-Гоффом был предложен объединенный закон для осмотического давления в растворах (аналогично объединенному газовому закону Менделеева-Клапейрона pV = n RT): осмотическое давление разбавленных растворов неэлектролитов прямо пропорционально молярной концентрации и абсолютной температуре:
πнеэл. = CRT (1)
где π – осмотическое давление жидкости – это избыточное гидростатическое давление, которое нужно приложить к раствору, чтобы осмос прекратился;
R – универсальная газовая постоянная;
С – молярная концентрация.
Т.к. С = n/V, где n - число моль вещества, а V – объем раствора, то: πнеэл. = 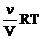 (2)
(2)
Закон Вант-Гоффа справедлив и для растворов электролитов. Однако в растворах электролитов осмотическое давление будет больше, это связано с диссоциацией электролитов. В результате нее в растворах оказывается большее число кинетически активных частиц (молекул и ионов суммарно), чем в растворах неэлектролитов с такой же концентрацией. Чтобы законы, применимые для неэлектролитов, можно было использовать и для растворов электролитов, Вант-Гофф ввел поправку – коэффициент i.
i – изотонический коэффициент Вант-Гоффа. Он показывает истинную концентрацию кинетически активных частиц и, следовательно, осмотическое давление в растворе электролита больше, чем в растворе неэлектролита такой же концентрации.

Величину i можно вычислить по формуле:
i = 1 + α(n – 1) (3)
α – степень диссоциации электролита, выраженная в долях единицы. Если ничего не сказано в условии задачи, для сильных электролитов α принимается равной 1 (например, для HCl, NaOH, KOH α обычно считается равно 1);
n – число ионов, на которое диссоциирует электролит.
Например: NaOH → Na+ + OH- n = 2
Na2SO4 → 2Na+ + SO42- n = 3
Fe2(SO4)3 → 2Fe3+ + 3SO42- n = 5.
Таким образом, осмотическое давление для разбавленных растворов электролитов вычисляется по уравнению:
πэл. = iCRT (4)
Осмотическое давление в растворах ВМС не подчиняется закону Вант-Гоффа, оно значительно увеличивается с ростом концентрации и может быть рассчитано по формуле Галлера:
 , (5)
, (5)
где С – весовая концентрация ВМС г/см3;
М – молярная масса;
К – константа.
В КДС также как в истинных растворах возникает осмотическое давление. коллоидные частицы, по сравнению со структурными единицами истинных растворов НМС, имеют значительно большие размеры и массу. Поэтому число частиц, содержащихся в растворах КДС, значительно меньше, следовательно, меньше и осмотическое давление.
Для расчета осмотического давления коллоидных растворов (КДС) также используют уравнение Вант-Гоффа:
πКДС = СdRT, (6)
где Cd – концентрация частиц ДФ.
1.3. Изотонические растворы. Изоосмия
Растворы с осмотическим давлением, равным осмотическому давлению раствора, взятого за стандарт, называются изотоническими. В медицине и фармации под изотоническими понимают растворы, имеющие осмотическое давление, равное осмотическому давлению плазмы крови (π = 7,4 атм). Растворы, имеющие более высокое осмотическое давление - гипертонические (вызывают обезвоживание и сморщивание эритроцитов), а более низкое - гипотонические (вызывают увеличение объема эритроцитов и разрыв оболочек). Помещая животные или растительные клетки в гипотонический раствор, можно наблюдать перемещение воды внутрь клетки, что ведет к их набуханию, а затем к разрыву оболочек и вытеканию клеточного содержимого. Подобное разрушение клеток путем разрыва их оболочек называют лизисом, а в случае эритроцитов – гемолизом.
В крепких растворах солей (гипертонических) отмечается наоборот сморщивание клеток (плазмолиз), обусловленное потерей воды, перемещающейся из них в более концентрированный внешний раствор.
Человеческий организм характеризуется большим постоянством ряда физико-химических показателей внутренней среды, в т.ч. и осмотического давления крови. Постоянство этого показателя называют изоосмией.
Изотонические растворы содержат одинаковое количество осмотически активных частиц. Количество осмотически активных частиц в растворе выражают через осмомоляльность. Эта величина определяется как суммарная концентрация всех растворенных веществ в растворе (моль/кг) и вычисляется по законам осмотического давления.
Осмотическое давление цельной крови равно 7,63 атм. Рассчитаем, какая будет молярная концентрация и массовая доля раствора глюкозы и раствора NaCl, изотоничных цельной крови. Эти растворы называют физиологическими.
| πр-ра глюкозы = πкрови =7,63 атм Т = 37оС = 310 К R = 0,082 л∙атм/моль∙К Сглюкозы -? ωглюкозы -? | Т.к. глюкоза неэлектролит используем закон Вант-Гоффа: π = CRT; πр-ра глюкозы = πкрови |

Рассчитаем массу глюкозы в растворе объемом 1 л:
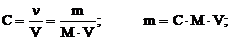 mглюкозы = 0,3×180×1 = 54 г
mглюкозы = 0,3×180×1 = 54 г
ρр-ра глюкозы = 1,08 г/мл; mр-ра глюкозы = 1,08×1000 мл = 1080 г;
 ; запомним:
; запомним:
Сглюкозы = 0,3 моль/л;  5 % - растворы глюкозы с такой концентрацией изотоничны цельной крови. πр-ра глюкозы = πкрови.
5 % - растворы глюкозы с такой концентрацией изотоничны цельной крови. πр-ра глюкозы = πкрови.
| πр-ра NaCl = πкрови = 7,63 атм Т = 37оС = 310 К R = 0,082 л∙атм/моль∙К Сглюкозы -? ωглюкозы -? | Хлорид натрия – это электролит. Для расчета используем уравнение Вант-Гоффа для электролитов:
π = iCRT;  .
Посчитаем, чему равен изотонический .
Посчитаем, чему равен изотонический
|
коэффициент. NaCl → Na+ + Cl- - диссоциирует на два иона,
n = 2. Т.к. NaCl – сильный электролит, то принимаем α = 1:
i = 1 + α(n – 1); i = 1 + 1(2-1) = 2.
Подставляем в формулу для концентрации:

рассчитаем массу NaCl в растворе объемом 1 л:
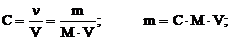
mNaCl = 0,15×58,5×1 = 8,77 г
ρр-ра NaCl = 1,01 г/мл; mр-ра NaCl = 1,01×1000 мл = 1010 г;
 ; запомним:
; запомним:
СNaCl р-р = 0,15 моль/л;  0,9 % - растворы NaCl с такой концентрацией изотоничны цельной крови. πр-ра NaCl = πкрови.
0,9 % - растворы NaCl с такой концентрацией изотоничны цельной крови. πр-ра NaCl = πкрови.






