Описание механизма буферного действия производится по следующему алгоритму:
· записывается состав буферной системы
 ;
;
· состояние компонентов буферной системы в водной среде отражают уравнения ионизации или диссоциации компонентов БС.  – слабая кислота, процесс ее распада на ионы обратим – ионизация (ставим знак
– слабая кислота, процесс ее распада на ионы обратим – ионизация (ставим знак 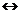 ).
).  – сильный электролит, диссоциирует нацело (ставим знак
– сильный электролит, диссоциирует нацело (ставим знак 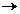 ). Ионизация двухосновной угольной кислоты идет по первой ступени:
). Ионизация двухосновной угольной кислоты идет по первой ступени:


· при добавлении посторонней сильной кислоты, например, НСl в действие вступит соль буфера, т.к. она содержит анион, выполняющий роль протолитического основания. 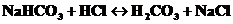


Таким образом, посторонняя сильная кислота заменяется эквивалентным количеством слабой протолитической кислоты, входящей в состав буфера, и рН раствора незначительно уменьшается;
· при добавлении постороннего сильного основания, например NaOH в действие вступит кислота буфера, т.к. с точки зрения протолитической теории кислота, как донор протонов, служит для связывания 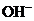 посторонней щелочи; при этом образуется анион соли, входящей в состав буфера, выполняющий роль слабого протолитического основания.
посторонней щелочи; при этом образуется анион соли, входящей в состав буфера, выполняющий роль слабого протолитического основания.



Таким образом, постороннее сильное основание заменяется эквивалентным количеством соли (слабого протолитического основания), входящей в состав буфера, и рН раствора незначительно увеличивается.
Пример 2. Механизм буферного действия фосфатной буферной системы:
· состав фосфатной буферной системы:
 ;
;
· уравнения ионизации или диссоциации компонентов буферной системы:



· при добавлении посторонней сильной кислоты, например, НСl в действие вступит та соль буфера, анион которой содержит меньше ионов водорода. Анион 
 выполняет роль протолитического основания.
выполняет роль протолитического основания. 
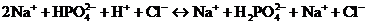
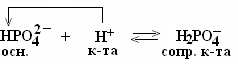
Вывод: посторонняя сильная кислота заменяется эквивалентным количеством слабой протолитической кислоты (соли 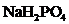 ), входящей в состав буфера, и рН раствора незначительно уменьшается.
), входящей в состав буфера, и рН раствора незначительно уменьшается.
· при добавлении постороннего сильного основания, например NaOH в действие вступит та соль буфера (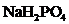 ),анион которой выполняет роль протолитической кислоты. Эта соль содержит больше ионов водорода.
),анион которой выполняет роль протолитической кислоты. Эта соль содержит больше ионов водорода.
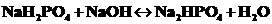
(Обязательно один компонент буфера превращается в другой, ставится знак 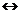 ).
).
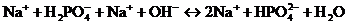

Вывод: постороннее сильное основание заменяется эквивалентным количеством соли  (слабого протолитического основания), и рН раствора незначительно увеличивается.
(слабого протолитического основания), и рН раствора незначительно увеличивается.
Пример 3. Механизм буферного действия аммиачной буферной системы:
· состав: это буферная система II типа, состоит из слабого основания и его соли
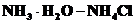
· уравнения ионизации или диссоциации компонентов буферной системы:


· при добавлении посторонней сильной кислоты, например, НСl в действие вступит основание буфера:



Вывод: посторонняя сильная кислота заменяется эквивалентным количеством соли 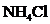 (слабой протолитической кислоты), входящей в состав буфера, и рН раствора незначительно уменьшается.
(слабой протолитической кислоты), входящей в состав буфера, и рН раствора незначительно уменьшается.
· при добавлении постороннего сильного основания, например NaOH в действие вступит соль буфера, содержащая катион  , выполняющий роль протолитической кислоты:
, выполняющий роль протолитической кислоты:



Вывод: постороннее сильное основание заменяется эквивалентным количеством слабого протолитического основания  , входящего в состав буфера, и рН раствора незначительно увеличивается.
, входящего в состав буфера, и рН раствора незначительно увеличивается.
Расчет буферной емкости
Для оценки способности буферной системы поддерживать постоянство рН при добавлении посторонних кислот и щелочей используются величины буферной емкости. Буферная емкость является количественным выражением буферного действия.
Буферная емкость по кислоте  измеряется числом моль эквивалентов посторонней сильной кислоты, добавленных к 1 л раствора, чтобы изменить его рН на единицу.
измеряется числом моль эквивалентов посторонней сильной кислоты, добавленных к 1 л раствора, чтобы изменить его рН на единицу.

Буферная емкость по основанию измеряется числом моль эквивалентов постороннего сильного основания, которые нужно добавить к буферу объемом 1 л чтобы изменить его рН на единицу.

Чем выше емкость, тем больше кислоты или основания можно добавить к буферу, не вызывая сдвига рН.






