Таблица 4 - Контрольная работа № 3
| № варианта | Спирты | Фенолы, эфиры | Карбонильные соединения | Карбоновые, сульфоновые кислоты | Амины | |||||
Алканы
1. Напишите механизм хлорирования 2,2,3,3-тетраметилбутана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните, почему реакция хлорирования протекает при комнатной температуре, а реакция бромирования - при +127 оС.
2. Напишите уравнения реакций, назовите все соединения. Рассмотрите механизм реакции (2). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните причину более низкой реакционной способности иода в реакции с этим углеводородом.
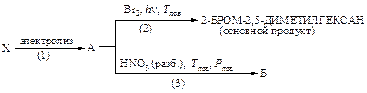
3. Приведите механизм бромирования 2,2,3,3-тетраметилбутана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию реакции. Какой из галогенов: хлор или бром - более реакционноспособен по отношению к этому углеводороду? Дайте объяснение.
4. Установите строение алкилхлорида, который при взаимодействии с (Zn + HCl) дает изобутан, а при взаимодействии с Na образует по реакции Вюрца 2,5-диметилгексан. Рассмотрите механизм хлорирования изобутана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните причину более низкой реакционной способности брома в реакции с этим углеводородом.
5. Какой углеводород образуется при электролизе натриевой соли пропионовой кислоты CH3CH2COONa? Рассмотрите механизм реакции бромирования этого углеводорода. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Какой из галогенов: хлор или бром - более реакционноспособен по отношению к этому углеводороду? Дайте объяснение.
6. Напишите механизм бромирования 2,2-диметилпропана. Рассчитайте теплоты реакций стадии развития цепи, укажите более медленную стадию. Объясните причину более низкой реакционной способности иода в реакции с этим углеводородом.
7. Рассмотрите механизм хлорирования этана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Приведите ряд изменения реакционной способности галогенов в реакции с этаном. Дайте объяснение.
8. Напишите уравнения реакций. Рассмотрите механизм реакции (1). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Какой из галогенов: хлор или бром - более реакционноспособен по отношению к этому углеводороду? Дайте объяснение.

9. Представлен следующий механизм хлорирования метана:

Стадию обрыва цепи напишите самостоятельно. Рассчитайте теплоты реакций стадии развития цепи. Сравните этот механизм с общепринятым. Почему предложенный механизм менее вероятен?
10. Напишите уравнения реакций, назовите все соединения. Рассмотрите механизм реакции (2). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Приведите ряд изменения реакционной способности галогенов в реакции с этим углеводородом. Дайте объяснение.
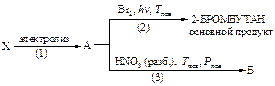
11. Приведите механизм хлорирования бутана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию реакции. Какой из галогенов: хлор или бром - более реакционноспособен по отношению к этому углеводороду? Дайте объяснение.
12. Установите строение алкилбромида, который при взаимодействии с (Zn + HCl) дает этан, а при взаимодействии с Na образует по реакции Вюрца бутан. Рассмотрите механизм бромирования бутана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Какой из галогенов: фтор или бром - более реакционноспособен по отношению к этому углеводороду? Дайте объяснение.
13. Рассмотрите механизм бромирования пропана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Приведите ряд изменения реакционной способности галогенов в реакции с пропаном. Дайте объяснение.
14. Напишите цепочку превращений. Рассмотрите механизм реакции (4). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните, почему реакция хлорирования протекает при комнатной температуре, а реакция бромирования - при повышенной температуре.

15. Рассмотрите механизм реакции иодирования метана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию реакции. Сделайте выводы относительно возможности протекания этой реакции.
16. Напишите цепочку превращений. Рассмотрите механизм реакции (1). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Приведите ряд изменения реакционной способности галогенов в реакции с этаном. Дайте объяснение.

17. Приведите механизм реакции бромирования метана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Сравните реакционную способность брома и хлора в реакции с метаном. Объясните, почему бромирование замедляется при добавлении бромоводорода, а добавление хлороводорода почти не влияет на скорость реакции хлорирования метана.
18. Приведите механизм реакции хлорирования 2,2-диметилпропана (неопентана). Рассчитайте теплоты реакций стадии развития цепи, укажите реакцию, определяющую скорость хлорирования. Объясните, почему не протекает хлорирование по механизму, включающему стадию:
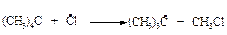
19. Рассмотрите механизм бромирования бутана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Приведите ряд изменения реакционной способности галогенов в реакции с бутаном. Дайте объяснение.
20. Установите строение алкилбромида, который при взаимодействии с (Zn + HCl) дает пропан, а при взаимодействии с Na образует по реакции Вюрца гексан. Рассмотрите механизм хлорирования гексана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Сравните реакционную способность брома и хлора к этому углеводороду.
21. Приведите механизм хлорирования этана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию реакции. Какой из галогенов: хлор или бром - более реакционноспособен по отношению к этому углеводороду? Дайте объяснение.
22. Напишите цепочку превращений. Рассмотрите механизм реакции (3). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните, почему реакция хлорирования протекает при комнатной температуре, а реакция бромирования - при повышенной температуре.
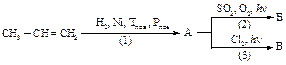
23. Приведите механизм реакции бромирования этана. Рассчитайте теплоты реакций стадии развития цепи. Укажите медленную стадию реакции. Сравните реакционную способность брома и иода к этому углеводороду.
24. Напишите цепочку превращений. Рассмотрите механизм реакции (2). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните, почему бромирование замедляется при добавлении бромоводорода, а добавление хлороводорода почти не влияет на скорость реакции хлорирования соединения А.
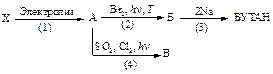
25. Напишите цепочку превращений. Рассмотрите механизм реакции (4). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Какой из галогенов: фтор или хлор - более реакционноспособен по отношению к этому углеводороду? Дайте объяснение.

26. Напишите уравнения реакций, назовите все соединения. Рассмотрите механизм реакции (2). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните причину более высокой реакционной способности хлора в реакции с этим углеводородом.

27. Рассмотрите механизм бромирования 2,2-диметилбутана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Приведите ряд изменения реакционной способности галогенов в реакции с 2,2-диметилбутаном. Дайте объяснение.
28. Приведите механизм хлорирования неопентана (2,2-диметилпропана). Рассчитайте теплоты реакций стадии развития цепи. Укажите медленную стадию реакции. Какой из галогенов: бром или хлор - будет более реакционноспособным в этой реакции? Дайте объяснение.
29. Установите строение алкилбромида, который при взаимодействии с (Zn + HCl) дает неопентан, а при взаимодействии с Na образует по реакции Вюрца 2,2,5,5-тетраметилгексан. Рассмотрите механизм хлорирования 2,2,5,5-тетраметилгексана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните причину более низкой реакционной способности иода в реакции с этим углеводородом.
30. Напишите цепочку превращений. Рассмотрите механизм реакции (4). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните причину более высокой реакционной способности хлора в реакции с этим углеводородом.

31. Рассмотрите механизм хлорирования этана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните, почему реакция хлора с этаном не протекает по механизму:
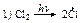
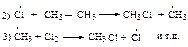
Стадии обрыва цепи напишите для этого случая самостоятельно.
32. Напишите цепочку превращений. Рассмотрите механизм реакции (3). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните, почему реакция хлорирования протекает при комнатной температуре, а реакция бромирования - при повышенной температуре.

33. Напишите уравнения реакций, назовите все соединения. Рассмотрите механизм реакции (2). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните причину более низкой реакционной способности иода в реакции с этим углеводородом.
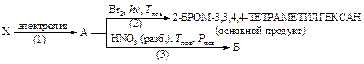
34. Рассмотрите механизм бромирования 3,3,4,4-тетраэтилгексана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Приведите ряд изменения реакционной способности галогенов в реакции с 3,3,4,4-тетраэтилгексаном. Дайте объяснение.
35. Приведите механизм хлорирования пропана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию реакции. Какой из галогенов: хлор или бром - более реакционноспособен по отношению к этому углеводороду.
36. Напишите механизм хлорирования этана. Рассчитайте теплоты реакций стадии развития цепи. Назовите стадию, определяющую скорость реакции. Укажите причину более высокой реакционной способности фтора по сравнению с хлором в реакции с этаном.
37. Приведите механизм хлорирования 2,5-диметилгексана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию реакции. Какой из галогенов: хлор или бром - более реакционноспособен по отношению к этому углеводороду.
38. Рассмотрите механизм бромирования 2,2,3,3-тетраметилбутана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Приведите ряд изменения реакционной способности галогенов в реакции с 2,2,3,3-тетраметилбутаном. Дайте объяснение.
39. Напишите уравнения реакций, назовите все соединения. Рассмотрите механизм реакции (2). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Укажите причину более низкой реакционной способности иода по сравнению с бромом в реакции с этим углеводородом.
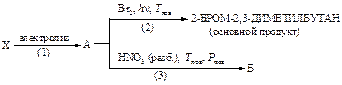
40. Приведите механизм хлорирования изобутана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию реакции. Какой из галогенов: хлор или бром - более реакционноспособен по отношению к этому углеводороду.
41. Рассмотрите механизм реакции иодирования этана. Рассчитайте теплоты реакций стадии развития цепи, укажите реакцию, определяющую скорость иодирования. Сделайте выводы относительно возможности протекания этой реакции.
42. Приведите механизм реакции бромирования этана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Сравните реакционную способность брома и хлора в реакции с этаном. Объясните, почему бромирование замедляется при добавлении бромоводорода, а добавление хлороводорода почти не влияет на скорость реакции хлорирования этана.
43. Установите строение алкилбромида, который при взаимодействии с (Zn + HCl) дает пентан, а при взаимодействии с Na образует по реакции Вюрца декан. Рассмотрите механизм хлорирования пентана. Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните причину более низкой реакционной способности брома в реакции с этим углеводородом.
44. Напишите уравнения реакций, назовите все соединения. Рассмотрите механизм реакции (3). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Приведите ряд изменения реакционной способности галогенов в реакции с этим углеводородом. Дайте объяснение.

45. Напишите цепочку превращений. Рассмотрите механизм реакции (4). Рассчитайте теплоты реакций стадии развития цепи, укажите медленную стадию. Объясните, почему реакция хлорирования этого углеводорода протекает при комнатной температуре, а реакция бромирования - при повышенной температуре.
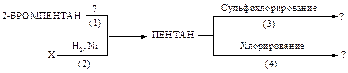
46. Какие свободные алкильные радикалы могут образовываться в реакции бромирования из молекулы пропана? Сравните их устойчивость и легкость образования. Укажите наиболее прочную C-H связь в молекуле пропана. Рассчитайте процентный состав монобромпроизводных, образующихся в реакции.
47. Какие алкильные радикалы могут образовываться в реакции хлорирования из молекулы 4-пропилгептана? Сравните их устойчивость, легкость образования. Укажите наиболее прочную C-H связь в данном соединении. Рассчитайте процентный состав монохлорпроизводных, образующихся в реакции.
48. Какие свободные алкильные радикалы могут образовываться в реакции бромирования из бутана? Сравните их устойчивость и легкость образования. Укажите наиболее прочную C-H связь в бутане. Рассчитайте процентный состав монобромпроизводных, образующихся в реакции.
49. Какие алкильные радикалы могут образовываться в реакции хлорирования из молекулы 3,5-диэтилгептана? Сравните их устойчивость, легкость образования. Укажите наиболее прочную C-H связь в данном соединении. Рассчитайте процентный состав монохлорпроизводных, образующихся в реакции.
50. Какие алкильные радикалы могут образовываться в реакции бромирования из молекулы изобутана? Сравните их устойчивость, легкость образования. Укажите наиболее прочную C-H связь в данном соединении. Рассчитайте процентный состав монобромпроизводных, образующихся в реакции.






