Величина  не залежить від напрямку швидкості, тому давайте краще перейдемо до розподілу за абсолютними значеннями. Позначимо ймовірність знайти швидкість за абсолютним значенням між
не залежить від напрямку швидкості, тому давайте краще перейдемо до розподілу за абсолютними значеннями. Позначимо ймовірність знайти швидкість за абсолютним значенням між  та
та  як
як  .
.  в досить простий спосіб пов’язана із
в досить простий спосіб пов’язана із  .
.
Введемо поняття простору швидкостей. Якщо відкласти вздовж осей  ,
,  ,
,  прямокутної системи координат проекції швидкості
прямокутної системи координат проекції швидкості  ,
,  ,
,  будь-якої молекули газу, то можна побудувати простір швидкостей, кожна точка в якому буде відповідати визначеному наборові проекцій швидкості молекули газу (рис. 2).
будь-якої молекули газу, то можна побудувати простір швидкостей, кожна точка в якому буде відповідати визначеному наборові проекцій швидкості молекули газу (рис. 2).
На рис. 2 оберемо точку з координатами 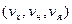 і до цієї точки проведемо радіус-вектор
і до цієї точки проведемо радіус-вектор  .
.  - елементарний об’єм у просторі швидкостей, обраний поблизу заданої швидкості
- елементарний об’єм у просторі швидкостей, обраний поблизу заданої швидкості  . (Скільки точок в ньому? -
. (Скільки точок в ньому? - 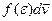 .)
.)
Точки, що визначають швидкості, величина яких лежить в інтервалі  поблизу обраного значення
поблизу обраного значення 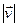 , знаходяться в області між сферами радіусів
, знаходяться в області між сферами радіусів  та
та  . Проінтегрувавши
. Проінтегрувавши  (при
(при 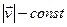 ) по всім можливим напрямкам
) по всім можливим напрямкам  у просторі швидкостей, отримаємо відносне число молекул
у просторі швидкостей, отримаємо відносне число молекул 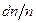 , швидкості яких лежать в одиничному інтервалі
, швидкості яких лежать в одиничному інтервалі  поблизу даної швидкості
поблизу даної швидкості 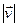 (тобто розподіл за абсолютними значеннями швидкостей молекул). Ми інтегрувати не будемо. Це шар із середнім радіусом
(тобто розподіл за абсолютними значеннями швидкостей молекул). Ми інтегрувати не будемо. Це шар із середнім радіусом  і товщиною
і товщиною  . Отже його об’єм
. Отже його об’єм  . Об’ємна густина в цьому шарі постійна, оскільки залежить тільки від
. Об’ємна густина в цьому шарі постійна, оскільки залежить тільки від  . Тому шукана ймовірність
. Тому шукана ймовірність  . Порівнюємо із
. Порівнюємо із  і маємо
і маємо
 . (3)
. (3)
Формула (3) являє собою закон Максвела розподілу молекул за абсолютними значеннями швидкостей. Нагадаємо ще раз, що величина  дає нам ймовірність того, що величина швидкості будь-якої молекули газу має значення в інтервалі від
дає нам ймовірність того, що величина швидкості будь-якої молекули газу має значення в інтервалі від  до
до  .
.
* Спробуйте дома отримати з функцію розподілу за значеннями кінетичної енергії.
 Крива на рис. 4 є графіком функції
Крива на рис. 4 є графіком функції  . При збільшенні швидкості
. При збільшенні швидкості  множник вигляду
множник вигляду  спадає швидше ніж зростає множник
спадає швидше ніж зростає множник  . Функція починається в нулі (через те, що
. Функція починається в нулі (через те, що 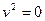 ), досягає максимального значення, а потім прямує до нуля.
), досягає максимального значення, а потім прямує до нуля.
При цьому, 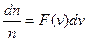 - частина молекул, швидкості яких лежать у інтервалі від
- частина молекул, швидкості яких лежать у інтервалі від  до
до  , числено дорівнює площі заштрихованої смуги з основою
, числено дорівнює площі заштрихованої смуги з основою  і висотою
і висотою  .
.
Для того, щоб визначити ймовірність виявити швидкість молекул в інтервалі  необхідно обчислити інтеграл
необхідно обчислити інтеграл
 .
.
Функція розподілу Максвела  , як видно з рис. 4, обертається в нуль при
, як видно з рис. 4, обертається в нуль при  і
і  . Це цілком зрозуміло, оскільки у газі немає ані нерухомих молекул, ані тих, що мають нескінчено великі швидкості. Нарешті, функція
. Це цілком зрозуміло, оскільки у газі немає ані нерухомих молекул, ані тих, що мають нескінчено великі швидкості. Нарешті, функція  має максимум при деякому значенні швидкості
має максимум при деякому значенні швидкості  . Це значення називають найбільш ймовірним. Ймовірність виявити у молекули швидкість
. Це значення називають найбільш ймовірним. Ймовірність виявити у молекули швидкість  - найбільша тому, що найбільша частина молекул має швидкості в інтервалі
- найбільша тому, що найбільша частина молекул має швидкості в інтервалі  поблизу
поблизу  .
.
Вигляд кривої  залежить від природи газу (оскільки формула (3) включає в себе
залежить від природи газу (оскільки формула (3) включає в себе  - масу молекули) та вд абсолютної температури
- масу молекули) та вд абсолютної температури 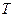 . Звичайно, з підвищенням
. Звичайно, з підвищенням 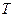 (або зменшенням маси молекули) частина молекул, які мають більш високі швидкості збільшуються. В результаті вся крива зміщується разом із своїм максимумом у бік більших швидкостей, при цьому найбільш ймовірну швидкість має менша кількість молекул (максимум стає меншим). Площа, обмежена новою кривою і віссю
(або зменшенням маси молекули) частина молекул, які мають більш високі швидкості збільшуються. В результаті вся крива зміщується разом із своїм максимумом у бік більших швидкостей, при цьому найбільш ймовірну швидкість має менша кількість молекул (максимум стає меншим). Площа, обмежена новою кривою і віссю  , не змінюється і залишається рівною одиниці. На рис. 5 представлені криві, які можна розглядати або як криві розподілу для різних температур (при однаковій масі), або криві розподілу для різних мас молекул (при однаковій температурі).
, не змінюється і залишається рівною одиниці. На рис. 5 представлені криві, які можна розглядати або як криві розподілу для різних температур (при однаковій масі), або криві розподілу для різних мас молекул (при однаковій температурі).







