1. Вычислить константу и степень гидролиза соли NH4Cl в растворе с С(NH4Cl) = 0,1 моль/л, если  (NH3×Н2О) = 1,8×10-5.
(NH3×Н2О) = 1,8×10-5.
Решение.
|
|


2. Вычислить константу и степень гидролиза Na2CO3 по первой ступени в растворе с С(Na2CO3) = 0,01 моль/л, если для H2CO3  = 4×10-7;
= 4×10-7;  = 5×10-11.
= 5×10-11.
Решение.
Гидролиз Na2CO3 протекает ступенчато:
Na2CO3 + H-OH ⇄ NaHCO3 + NaОН (1 ступень)
В сокращенном виде уравнение выглядит так:
|
|
NaHCO3 + H-OH ⇄ H2CO3 + NaОН (2 ступень)
|
|
Гидролиз Na2CO3 по первой ступени приводит к образованию гидрокарбонат-иона HCO3-, который является слабым электролитом:
HCO3- ⇄ H+ + СО32-
Данное уравнение соответствует диссоциации H2CO3 по второй ступени и характеризуется константой  (H2CO3) = 5×10-11.
(H2CO3) = 5×10-11.
Поэтому:
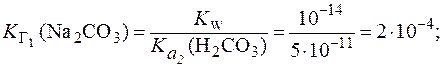

3. Сравнить степень гидролиза NaNO2 в растворах соли с концентрациями 0,1 и 0,001 моль/л, если  (HNO2) = 4×10-4.
(HNO2) = 4×10-4.
Решение.
Введем обозначения: С1 = 0,1 моль/л; С2 = 0,001 моль/л.
Тогда:  ;
;  .
.
Разделим одно выражение на другое и получим:

4. Рассчитать рН раствора соли NaCN с C(NaCN) = 0,01 моль/л, если  (HCN) = 8×10–10. Указать характер среды.
(HCN) = 8×10–10. Указать характер среды.
Решение.
|
|
1 способ:




pH > 7  среда щелочная.
среда щелочная.
2 способ:


5. Рассчитать рН раствора соли NH4CN с молярной концентрацией 0,002 моль/л, если  (HCN) = 8×10–10,
(HCN) = 8×10–10,  (NH3×Н2О) = 1,8×10–5. Указать характер среды.
(NH3×Н2О) = 1,8×10–5. Указать характер среды.
Решение.
|
|




pH > 7  среда слабощелочная.
среда слабощелочная.
6. Найти разность значений рН растворов Na2S и NaHS с одинако-выми концентрациями солей, если  (Н2S) = 7,
(Н2S) = 7,  (Н2S) = 13.
(Н2S) = 13.
Решение.


Вычтем из первого уравнения второе и получим:

Вопросы для самоконтроля
1. Какой процесс называется гидролизом соли?
2. Какова причина изменения рН раствора за счет гидролиза?
2. Какие типы солей подвергаются гидролизу в растворе? Приведите примеры.
3. Почему соли типа NaCl, KI, СаС12 не подвергаются гидролизу?
4. В каких случаях при гидролизе солей образуются кислые (основные) соли? Приведите примеры.
5. В каких случаях происходит необратимый гидролиз соли? Приведите примеры.
6. Какие продукты образуются при взаимодействии хлорида хрома (III) и сульфида аммония (NH4)2S в водном растворе?
7. Что называется константой гидролиза? От каких факторов зависит и от каких не зависит константа гидролиза?
8. Что называется степенью гидролиза? Как она связана с константой гидролиза различных типов солей?
9. Какие факторы влияют на величину степени гидролиза соли?
10. Почему степень гидролиза увеличивается при повышении температуры?
11. Для, каких солей разбавление раствора практически не влияет на степень гидролиза?
12. Каким способом можно гидролизовать FeCl3 до образования Fe(OH)3?
13. При гидролизе каких солей рН раствора близок к 7?
14. Почему раствор NaHCO3 имеет слабощелочную реакцию, а раствор NaHSO3 - слабокислую?  (H2CO3) = 4×10-7,
(H2CO3) = 4×10-7,  (H2SO3) = 1,7×10-2.
(H2SO3) = 1,7×10-2.
15. Необходимо приготовить раствор соли FeSO4, при гидролизе которой образуется малорастворимое соединение (раствор мутнеет). В какой среде (кислой или щелочной) следует готовить раствор, чтобы избежать его помутнения? Почему?
Варианты задач для самостоятельного решения
Вариант №1
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: Na2SO4, FeCl2, Na2S.
2. Рассчитать константу и степень гидролиза NH4NO3 в растворе с С(NH4NO3) = 0,001 моль/л, если  (NH3×Н2О) = 1,8×10-5.
(NH3×Н2О) = 1,8×10-5.
3. Вычислить значение pH раствора СН3СООК с C(СН3СООК) = 0,005 моль/л, если  (СН3СООН) = 1,8×10-5.
(СН3СООН) = 1,8×10-5.
4. Рассчитать константу и степень гидролиза Na2CO3 по второй ступени в растворе с С(Na2CO3) = 0,1 моль/л, если для H2CO3  = 4×10-7;
= 4×10-7;  = 5×10-11.
= 5×10-11.
Вариант №2
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: MnSO4, KI, Na2SiO3.
2. Рассчитать константу и степень гидролиза NaCN в растворе с С(NaCN) = 0,01 моль/л, если  (HCN) = 8×10-10.
(HCN) = 8×10-10.
3. Вычислить значение рН раствора NaNO2 с C(NaNO2) = 0,01 моль/л, если  (HNO2) = 4×10-4.
(HNO2) = 4×10-4.
4. Сравнить величины констант гидролиза Pb(NO3)2 по первой и по второй ступени, если для Pb(OH)2  = 9,6×10-4;
= 9,6×10-4;  = 3×10-8.
= 3×10-8.
Вариант №3
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: Ca(NO3)2, Na2SO3, Cu(NO3)2.
2. Вычислить константу и степень гидролиза КClO в растворе с C(КClO) = 0,1 моль/л, если  (НClO) = 5,6×10-8.
(НClO) = 5,6×10-8.
3. Вычислить значение рН раствора соли KCN с C(KCN) = 0,05 моль/л, если  (HCN) = 8×10-10.
(HCN) = 8×10-10.
4. Рассчитать константу и степень гидролиза Na3PO4 по первой ступени в растворе с С(Na3PO4) = 0,1 моль/л, если для H3PO4  = 7,6×10-3;
= 7,6×10-3;  = 5,9×10-8,
= 5,9×10-8,  = 3,3×10-13.
= 3,3×10-13.
Вариант №4
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: K3PO4, CaCl2, ZnCl2.
2. Сравнить степень гидролиза NaCN в растворах с молярной концентрацией эквивалента соли 0,1 и 0,001 моль/л если  (HCN) = 8×10-10.
(HCN) = 8×10-10.
3. Вычислить значение рН раствора NH4NO3 с C(NH4NO3) = 0,1 моль/л, если  (NH3×Н2О) = 1,8×10-5.
(NH3×Н2О) = 1,8×10-5.
4. Рассчитать степень гидролиза KHCO3 в растворе с С(KHCO3) = 0,05 моль/л, если для H2CO3  = 4×10-7;
= 4×10-7;  = 5×10-11.
= 5×10-11.
Вариант №5
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: CuSO4, Li2S, NaBr.
2. Рассчитать константу и степень гидролиза NaNO2 в растворе с С(NaNO2) = 0,01 моль/л, если  (HNO2) = 4×10-4.
(HNO2) = 4×10-4.
3. Вычислить значение рН раствора NH4I с концентрацией соли 0,02 моль/л, если  (NH3×Н2О) = 1,8×10-5.
(NH3×Н2О) = 1,8×10-5.
4. Сравнить величины констант гидролиза Na2SiO3 по первой и по второй ступени, если для H2SiO3  = 1,3×10-10;
= 1,3×10-10;  = 2×10-12.
= 2×10-12.
Вариант №6
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: SrCl2, Fe(NO3)3, K2S.
2. Сравнить величины степени гидролиза NaF в растворах с молярной концентрацией эквивалента соли 0,2 и 0,002 моль/л.  (HF) = 6,6×10-4.
(HF) = 6,6×10-4.
3. Вычислить значение pH раствора НСООNa с молярной концентрацией соли 0,05 моль/л, если  (НСООН) = 2,2×10-4.
(НСООН) = 2,2×10-4.
4. Рассчитать степень гидролиза NaHS в растворе с С(NaHS) = 0,05 моль/л, если для H2S  = 1×10-7;
= 1×10-7;  = 1×10-13.
= 1×10-13.
Вариант №7
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: NaNO3, ZnSO4, Ca(OCl)2.
2. Рассчитать константу гидролиза и степень гидролиза NH4NO2 в растворе с С(NH4NO2) = 0,05 моль/л, если  (HNO2) = 4×10-4,
(HNO2) = 4×10-4,  (NH3×Н2О) = 1,8×10-5.
(NH3×Н2О) = 1,8×10-5.
3. Вычислить значение рН раствора C6H5COONa с концентрацией соли 0,01 моль/л, если  (C6H5COOH) = 6,3×10-5.
(C6H5COOH) = 6,3×10-5.
4. Рассчитать степень гидролиза Na3PO4 по второй ступени в растворе с С(Na3PO4) = 0,01 моль/л, если для H3PO4  = 7,6×10-3;
= 7,6×10-3;  = 5,9×10-8,
= 5,9×10-8,  = 3,3×10-13.
= 3,3×10-13.
Вариант №8
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: Pb(NO3)2, CaS, KC1.
2. Сравнить величины констант и степеней гидролиза солей NaF и NaCN в растворах с одинаковыми концентрациями, если  (HF) = 6,6×10-4;
(HF) = 6,6×10-4;  (HCN) = 8×10-10.
(HCN) = 8×10-10.
3. Вычислить значение рН раствора CH3COONH4 с молярной концентрацией соли 0,05 моль/л, если  (CH3COOH) = 1,8×10-5;
(CH3COOH) = 1,8×10-5;  (NH3×H2O) = 1,8×10-5.
(NH3×H2O) = 1,8×10-5.
4. Рассчитать константу и степень гидролиза Na2C2O4 по первой ступени в растворе с концентрацией соли 0,05 моль/л, если для Н2C2O4  = 5,9×10-2,
= 5,9×10-2,  = 6,4×10-5.
= 6,4×10-5.
Вариант №9
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: Ba(NO3)2, NiCl2, K2SO3.
2. Pассчитать константу гидролиза и степень гидролиза CH3COONH4 в растворе с С(CH3COONH4) = 0,002 моль/л, если  (CH3COOH) = 1,8×10-5;
(CH3COOH) = 1,8×10-5;  (NH3×H2O) = 1,8×10-5.
(NH3×H2O) = 1,8×10-5.
3. Вычислить значение рН раствора соли KF с концентрацией 0,001 моль/л, если  (HF) = 6,6×10-4.
(HF) = 6,6×10-4.
4. Рассчитать константу и степень гидролиза тартрата натрия по первой ступени в растворе с концентрацией соли 0,05 моль/л, если винная кислота является двухосновной и имеет  = 9,1×10-4,
= 9,1×10-4,  = 4,3×10-5.
= 4,3×10-5.
Вариант №10
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: CoSO4, Na2C2O4, Sr(NO3)2.
2. Сравнить величины констант и степеней гидролиза NH4F в растворах с концентрациями 0,02 моль/л и 0,002 моль/л, если  (HF) = 6,6×10-4,
(HF) = 6,6×10-4,  (NH3×H2O) = 1,8×10-5.
(NH3×H2O) = 1,8×10-5.
3. Вычислить значение рН раствора NH4CN с концентрацией 0,01 моль/л, если  (HCN) = 8×10-10,
(HCN) = 8×10-10,  (NH3×Н2О) = 1,8×10-5.
(NH3×Н2О) = 1,8×10-5.
4. Сравнить величины констант гидролиза Na2S по первой и по второй ступени, если  (H2S) = 1×10-7;
(H2S) = 1×10-7;  (H2S) = 1×10-13.
(H2S) = 1×10-13.
Вариант №11
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: BaS, K2SO4, CrCl3.
2. Вычислить константу и степень гидролиза HCOONa в растворе с молярной концентрацией соли 0,001 моль/л, если  (HCOOH) = 2,2×10-4.
(HCOOH) = 2,2×10-4.
3. Вычислить значение рН раствора NH4F с концентрацией 0,02 моль/л, если  (NH3×Н2О) = 1,8×10-5,
(NH3×Н2О) = 1,8×10-5,  (HF) = 6,6×10-4.
(HF) = 6,6×10-4.
4. Рассчитать константу и степень гидролиза сукцината натрия по первой ступени в растворе с концентрацией соли 0,05 моль/л, если янтарная кислота является двухосновной и имеет  = 1,6×10-5,
= 1,6×10-5,  = 2,3×10-6.
= 2,3×10-6.
Вариант №12
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: Ni(NO3)2, K2CO3, ВаС12.
2. Сравнить величины констант и степеней гидролиза NH4NO3 в растворах с концентрациями соли 0,02 и 0,002 моль/л, если  (NH3×H2O) = 1,8×10-5.
(NH3×H2O) = 1,8×10-5.
3. Вычислить значение рН раствора KClO с концентрацией соли 0,04 моль/л, если  (HClO) = 5,6×10-8.
(HClO) = 5,6×10-8.
4. Рассчитать степень гидролиза Na3PO4 по третьей ступени в растворе с С(Na3PO4) = 0,001 моль/л, если для H3PO4  = 7,6×10-3;
= 7,6×10-3;  = 5,9×10-8,
= 5,9×10-8,  = 3,3×10-13.
= 3,3×10-13.
Вариант №13
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: NaI, K2SiO3, Fe2(SO4)3.
2. Вычислить константу и степень гидролиза C2H5COONa в растворе с С(C2H5COONa) = 0,l моль/л, если  (C2H5COOH) = 1,3×10-5.
(C2H5COOH) = 1,3×10-5.
3. Вычислить значение рН раствора NaHCO3 с концентрацией 0,1 моль/л, если  (Н2СО3) = 4×10-7,
(Н2СО3) = 4×10-7,  (H2CO3) = 5×10-11.
(H2CO3) = 5×10-11.
4. Рассчитать константу и степень гидролиза о-фталата натрия по первой ступени в растворе с концентрацией соли 0,05 моль/л, если о-фталевая кислота является двухосновной и имеет  = 10-3,
= 10-3,  = 6×10-6.
= 6×10-6.
Вариант №14
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: Na2HPO4, KNO3, Bi(NO3)3.
2. Вычислить степень гидролиза NH4F в растворе с С(NH4F) = 0,02 моль/л, если  (HF) = 6,6×10-4,
(HF) = 6,6×10-4,  (NH3×H2O) = 1,8×10-5.
(NH3×H2O) = 1,8×10-5.
3. Рассчитать значение рН раствора Na2C2O4 с С(Na2C2O4) = 0,01 моль/л, если  (Н2C2O4) = 5,9×10-2,
(Н2C2O4) = 5,9×10-2,  (Н2C2O4) = 6,4×10-5.
(Н2C2O4) = 6,4×10-5.
4. Рассчитать константу и степень гидролиза гидросукцината натрия в растворе с концентрацией соли 0,05 моль/л, если янтарная кислота является двухосновной и имеет  = 1,6×10-5,
= 1,6×10-5,  = 2,3×10-6.
= 2,3×10-6.
Вариант №15
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: NaClO4, Na2SeO3, FeCl3.
2. Вычислить константу и степень гидролиза лактата натрия в растворе с С(CH3CH(OH)COONa) = 0,02 моль/л, если  (CH3CH(OH)COOH) = 1,4×10-4.
(CH3CH(OH)COOH) = 1,4×10-4.
3. Вычислить значение рН раствора Na2CO3 с концентрацией 0,1 моль/л, если  (Н2СО3) = 4×10-7,
(Н2СО3) = 4×10-7,  (Н2СО3) = 4,7×10-11.
(Н2СО3) = 4,7×10-11.
4. Сравнить величины констант гидролиза ZnCl2 по первой и по второй ступени, если для Zn(OH)2  = 4×10-5;
= 4×10-5;  = 1,5×10-9.
= 1,5×10-9.
Вариант №16
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: NiSO4, Li2SO3, LiCl.
2. Сравнить величины констант и степеней гидролиза солей KNO2 и KCN в растворах с одинаковыми концентрациями, если  (HCN) = 8×10-10,
(HCN) = 8×10-10,  (HNO2) = 4×10-4.
(HNO2) = 4×10-4.
3. Вычислить значение рН раствора NH4NO2 с концентрацией соли 0,05 моль/л, если  (HNO2) = 4×10-4,
(HNO2) = 4×10-4,  (NH3×H2O) = 1,8×10-5.
(NH3×H2O) = 1,8×10-5.
4. Рассчитать константу и степень гидролиза селенита натрия по первой ступени в растворе с C(Na2SeO3) = 0,02 моль/л, если для H2SeO3  = 3,5×10-3,
= 3,5×10-3,  = 5×10-8.
= 5×10-8.
Вариант №17
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: Na2Te, MnCl2, KBr.
2. Рассчитать константу и степень гидролиза C6H5COONa в растворе с С(C6H5COONa) = 0,002 моль/л, если  (C6H5COOH) = 6,3×10-5.
(C6H5COOH) = 6,3×10-5.
3. Вычислить значение рН раствора KBrO с концентрацией соли 0,05 моль/л, если  (HBrO) = 2×10-8.
(HBrO) = 2×10-8.
4. Рассчитать константу и степень гидролиза селенида натрия в растворе с C(Na2Se) = 0,02 моль/л, если для H2Se  = 1,4×10-4,
= 1,4×10-4,  = 5×10-11.
= 5×10-11.
Вариант №18
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: Ca(CH3COO)2, Sb(NO3)3, BaBr2.
2. Вычислить константу и степень гидролиза NH4Br в растворе с С(NH4Br) = 0,05 моль/л, если  (NH3×Н2О) = 1,8×10-5.
(NH3×Н2О) = 1,8×10-5.
3. Сравнить значения рН растворов KF и KCN с одинаковыми концентрациями, если  (HF) = 6,6×10-4,
(HF) = 6,6×10-4,  (HCN) = 8×10-10.
(HCN) = 8×10-10.
4. Рассчитать константу и степень гидролиза цитрата натрия по первой ступени в растворе с концентрацией соли 0,02 моль/л, если лимонная кислота является трехосновной и имеет  = 1,2×10-3,
= 1,2×10-3, 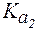 = 7,3×10-5,
= 7,3×10-5,  = 1,6×10-6.
= 1,6×10-6.
Вариант №19
1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: Na2Se, Sn(NO3)2, Li2SO4.
2. Вычислить степень гидролиза NH4CN в растворе с C(NH4CN) = 0,02 моль/л, если  (HCN) = 8×10-10,
(HCN) = 8×10-10,  (NH3×H2O) = 1,8×10-5.
(NH3×H2O) = 1,8×10-5.
3. Вычислить значение рН раствора Na3PO4 с концентрацией соли 0,01 моль/л, если для H3PO4  = 7,6×10-3;
= 7,6×10-3;  = 5,9×10-8,
= 5,9×10-8,  = 3,3×10-13.
= 3,3×10-13.
4. Рассчитать константу и степень гидролиза цитрата натрия по второй ступени в растворе с концентрацией соли 0,002 моль/л, если лимонная кислота является трехосновной и имеет  = 1,2×10-3,
= 1,2×10-3,  = 7,3×10-5,
= 7,3×10-5,  = 1,6×10-6.
= 1,6×10-6.
Вариант №20
1. 1. Написать уравнения гидролиза (в молекулярном и ионном виде) и определить реакцию среды водных растворов перечисленных солей: K2C2O4, Al2(SO4)3, LiNO3.
2. Сравнить величины констант и степеней гидролиза солей KF и CH3COOK в растворах с одинаковыми концентрациями, если  (HF) = 6,6×10-4,
(HF) = 6,6×10-4,  (CH3COOH) = 1,8×10-5.
(CH3COOH) = 1,8×10-5.
3. Вычислить значение рН раствора Na2HPO4 с концентрацией соли 0,01 моль/л, если для H3PO4  = 7,6×10-3;
= 7,6×10-3;  = 5,9×10-8,
= 5,9×10-8,  = 3,3×10-13.
= 3,3×10-13.
4. Сравнить величины констант гидролиза адипината натрия по первой и по второй ступени, если адипиновая кислота является двухосновной и имеет  = 3,9×10-5;
= 3,9×10-5;  = 3,9×10-6.
= 3,9×10-6.
БЛОК ИНФОРМАЦИИ






