«нать:
1.ќсновные термодинамические функции: теплоту, работу, внутреннюю энергию, энтальпию, энтропию, изобарно-изотермический и изохорно-изотермический потенциалы;
2. ¬иды термодинамических процессов;
3. —ущность первого закона термодинамики, его математическое выражение и применение к различным процессам;
4. ѕричины возникновени€ тепловых эффектов, сущность закона √есса и следствий из него, тепловые эффекты различных процессов;
5. —ущность и математические выражени€ второго закона термодинамики;
6. —ущность энтропии и ее статистическую природу;
7. ритерии самопроизвольного протекани€ процессов в различных системах;
8. ”равнение изотермы химической реакции и возможность его использовани€;
9. ”равнение изобары химической реакции и его применение.
”меть рассчитывать:
1. “епловые эффекты реакций при стандартных услови€х;
2. »зменение энтропии в результате химической реакции;
3. »зменение свободной энергии √иббса при заданной температуре;
4. онстанту химического равновеси€ при заданной температуре.
—осто€ние системы характеризуетс€ ее физическими и химическими свойствами (объем, давление, температура, химический состав и т.д.). —войства, выбранные в качестве независимых переменных, называютс€ параметрами состо€ни€. ¬еличина, определ€ема€ этими параметрами, однозначно характеризующа€ систему и независ€ща€ от пути ее перехода из одного состо€ни€ в другое, называетс€ функцией состо€ни€.
“ермодинамическими функци€ми состо€ни€ €вл€ютс€:
внутренн€€ энерги€ U характеризует общий запас энергии в системе, исключа€ кинетическую энергию системы как целого и ее потенциальную энергию в поле внешних сил ΔU = Uкон Ц Uисх > 0 внутренн€€ энерги€ системы возрастает;
энтальпи€ Ќ характеризует общее теплосодержание системы или тепловой эффект химической реакции при посто€нном давлении
ΔЌ > 0 тепло поглощаетс€, эндотермическа€ реакци€;
ΔЌ < 0 тепло выдел€етс€, экзотермическа€ реакци€;
энтропи€ S характеризует степень беспор€дочности частиц в системе
ΔS > 0 степень беспор€дка возрастает;
ΔS < 0 cтепень беспор€дка уменьшаетс€;
свободна€ энерги€ √иббса G или изобарно-изотермический потенциал характеризует часть энергии, идущую на совершение полезной работы при посто€нных давлении и температуре
ΔG > 0 энерги€ поглощаетс€, эндоэргоническа€ реакци€;
ΔG < 0 энерги€ выдел€етс€, экзоэргоническа€ реакци€;
свободна€ энерги€ √ельмгольца F или изохорно-изотермический потенциал характеризует часть энергии, идущую на совершение полезной работы при посто€нных объеме и температуре.
Δ F > 0 энерги€ поглощаетс€, Δ F < 0 энерги€ выдел€етс€.
¬ соответствии с законом √есса:
ΔG реакции = Σ(νΔG 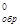 )продуктов Ц Σ(νΔG
)продуктов Ц Σ(νΔG 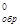 )исходных веществ
)исходных веществ
ΔH реакции = Σ(νΔH 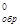 )продуктов Ц Σ(νΔH
)продуктов Ц Σ(νΔH 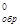 )исходных веществ
)исходных веществ
ΔS реакции = Σ(νS  )продуктов Ц Σ(ν S
)продуктов Ц Σ(ν S  )исходных веществ.
)исходных веществ.
ќбъединенный термодинамический закон
|
|
|
ΔG реакции = ΔH реакции - T ΔS реакции.
≈сли пренебречь зависимост€ми ΔH0 и ΔS0 от температуры, то дл€ термодинамических расчетов примен€ют уравнение ΔG 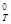 = ΔH
= ΔH 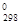 - TΔS
- TΔS 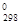 .
.
≈сли ΔG < 0, то такой процесс термодинамически возможен. „ем более отрицательно ΔG, тем в большей степени реакци€ протекает в направлении образовани€ продуктов реакции.
≈сли ΔG > 0, то процесс приводит к увеличению энергии √иббса и така€ реакци€ термодинамически невозможна.
≈сли ΔG = 0, то начальные услови€ в системе соответствуют равновесию.
ритери€ми самопроизвольного протекани€ процессов €вл€ютс€
1. в изолированной системе ΔS > 0;
2. в закрытой и открытой системах ΔG < 0 (дл€ изобарно-изотермических процессов);
3. в закрытой и открытой системах ΔF < 0 (дл€ изохорно-изотермических процессов).
ѕример 1. —колько теплоты выделитс€ при сжигании 920 г этанола? «апишите термохимическое уравнение данной реакции.
–ешение: ѕроцесс горени€ этанола можно представить следующим уравнением C2H5OH (ж) + 3O2 (г) = 2CO2 (г) + 3H2O(г). ѕо первому следствию из закона √есса ΔH 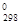 реакции =2ΔH
реакции =2ΔH 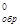 CO
CO 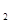 + 3ΔH
+ 3ΔH  H
H  O - ΔH
O - ΔH 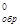 —
— 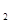 H
H 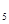 OH - 3ΔH
OH - 3ΔH 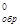 O
O 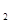 .
.
»спользу€ справочные данные, находим тепловой эффект горени€ 1 моль этанола C2H5OH.
ΔH 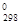 реакции = 2(-393,5) + 3(-285,8) Ц (-277,6) Ц 0 = - 1366,8 кƒж
реакции = 2(-393,5) + 3(-285,8) Ц (-277,6) Ц 0 = - 1366,8 кƒж
Ќаходим количество вещества C2H5OH в 920 г:
n (C2H5OH) = 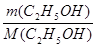 =
= 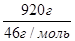 = 20 моль.
= 20 моль.
—ледовательно, количество теплоты, выдел€ющеес€ при сжигании 20 моль этанола, будет равно Q p = - ΔH 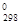 реакцииn (C2H5OH) = 1366,8∙20 = 27336 кƒж = 27,34 ћƒж. “ермохимическое уравнение можно записать следующим образом C2H5OH (ж) + 3O2 (г) = 2CO2 (г) + 3H2O(г), ΔH
реакцииn (C2H5OH) = 1366,8∙20 = 27336 кƒж = 27,34 ћƒж. “ермохимическое уравнение можно записать следующим образом C2H5OH (ж) + 3O2 (г) = 2CO2 (г) + 3H2O(г), ΔH 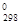 реакции = -1366,8 кƒж.
реакции = -1366,8 кƒж.
ќтвет: выделитс€ 27,34 ћƒж тепла.
ѕример 2. — помощью термодинамических расчетов на примере реакций
SnO2 (к) + Sn (к) = 2SnO(к) и PbO2(к) + Pb(к) = 2PbO(к) ответьте на вопрос об устойчивых степен€х окислени€ олова и свинца в закрытой системе при температуре 300 .
–ешение: –ассчитаем ΔG 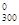 первой и второй реакции по уравнению ΔG
первой и второй реакции по уравнению ΔG  = ΔH
= ΔH 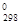 - TΔS
- TΔS 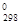 .
.
ƒл€ первой реакции:
1) ΔH 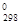 реакции =2ΔH
реакции =2ΔH 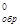 SnO - ΔH
SnO - ΔH 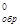 SnO
SnO  - ΔH
- ΔH 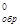 Sn
Sn
ΔH  реакции = 2(-286) - (-581) Ц 0 = 9 кƒж > 0 Ц тепло поглощаетс€, эндотермическа€ реакци€;
реакции = 2(-286) - (-581) Ц 0 = 9 кƒж > 0 Ц тепло поглощаетс€, эндотермическа€ реакци€;
2) ΔS 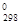 реакции = 2S
реакции = 2S 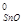 - S
- S 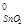 - S
- S 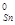
ΔS 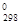 реакции =2∙56,5 Ц 52,3 Ц 51,6 = 9,1ƒж/ = 0,0091кƒж/ .
реакции =2∙56,5 Ц 52,3 Ц 51,6 = 9,1ƒж/ = 0,0091кƒж/ .
—тепень беспор€дка в системе возрастает, данна€ реакци€ будет протекать самопроизвольно в изолированной системе при стандартных услови€х.
ΔG 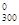 = 9 кƒж Ц 300 ∙ 0,0091 кƒж/ = 6,27 кƒж > 0 Ц энерги€ поглощаетс€ в ходе реакции; в закрытых и открытых системах термодинамически возможна обратна€ реакци€, т.е. в указанных услови€х более устойчив оксид олова (IV) SnO2.
= 9 кƒж Ц 300 ∙ 0,0091 кƒж/ = 6,27 кƒж > 0 Ц энерги€ поглощаетс€ в ходе реакции; в закрытых и открытых системах термодинамически возможна обратна€ реакци€, т.е. в указанных услови€х более устойчив оксид олова (IV) SnO2.
ƒл€ второй реакции расчеты провод€тс€ по такой же схеме:
1) ΔH 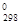 реакции =2ΔH
реакции =2ΔH 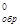 PbO - ΔH
PbO - ΔH 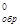 PbO
PbO  - ΔH
- ΔH 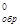 Pb
Pb
ΔH 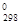 реакции =2(- 219) Ц (- 277) Ц 0 = -161кƒж < 0 Ц тепло выдел€етс€, экзотермическа€ реакци€;
реакции =2(- 219) Ц (- 277) Ц 0 = -161кƒж < 0 Ц тепло выдел€етс€, экзотермическа€ реакци€;
2) ΔS 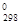 реакции = 2S
реакции = 2S 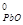 - S
- S 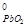 - S
- S 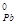
ΔS 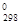 реакции =2∙66 Ц 72 Ц 65 = - 5 ƒж/ = - 0,005 кƒж/ Ц степень беспор€дка в системе уменьшаетс€, в изолированной системе данна€ реакци€ самопроизвольно протекать не будет.
реакции =2∙66 Ц 72 Ц 65 = - 5 ƒж/ = - 0,005 кƒж/ Ц степень беспор€дка в системе уменьшаетс€, в изолированной системе данна€ реакци€ самопроизвольно протекать не будет.
ΔG 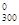 = - 161 кƒж Ц 300 (-0,005кƒж/ ) = - 159,5 кƒж < 0 Ц энерги€ выдел€етс€, в закрытых и открытых системах термодинамически возможен пр€мой процесс, т.е. в указанных услови€х более устойчив оксид свинца (II) PbO.
= - 161 кƒж Ц 300 (-0,005кƒж/ ) = - 159,5 кƒж < 0 Ц энерги€ выдел€етс€, в закрытых и открытых системах термодинамически возможен пр€мой процесс, т.е. в указанных услови€х более устойчив оксид свинца (II) PbO.
|
|
|
ќтвет: в указанных услови€х устойчивой степенью окислени€ дл€ олова €вл€етс€ степень окислени€ +4, дл€ свинца Ц +2.
ѕример 3. онстанты равновеси€ 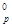 реакции 2SO2 (г) + O2 (г) = 2SO3 (г) при 727 и 9270— равны соответственно 3,34 и 0,079. –ассчитайте стандартную энергию √иббса ΔG
реакции 2SO2 (г) + O2 (г) = 2SO3 (г) при 727 и 9270— равны соответственно 3,34 и 0,079. –ассчитайте стандартную энергию √иббса ΔG 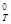 и определите направление самопроизвольного протекани€ реакции при указанных температурах, а также средний тепловой эффект (стандартную энтальпию) процесса в приведенном температурном интервале.
и определите направление самопроизвольного протекани€ реакции при указанных температурах, а также средний тепловой эффект (стандартную энтальпию) процесса в приведенном температурном интервале.
–ешение: ¬ абсолютной шкале температуры 727 и 9270— соответственно равны 1000 и 1200 . ¬еличину ΔG 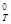 рассчитаем по стандартному уравнению ФизотермыФ химической реакции ΔG
рассчитаем по стандартному уравнению ФизотермыФ химической реакции ΔG 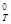 = - RT ln
= - RT ln 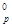 ;
;
ΔG 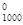 = -8,314 ∙1000 ln 3,34 = - 10026 ƒж/моль = - 10,026 кƒж/моль;
= -8,314 ∙1000 ln 3,34 = - 10026 ƒж/моль = - 10,026 кƒж/моль;
ΔG 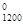 = -8,314 1200 ln 0,079 = 25324 ƒж/моль = 25,3 кƒж/моль.
= -8,314 1200 ln 0,079 = 25324 ƒж/моль = 25,3 кƒж/моль.
“аким образом, при 1000 реакци€ протекает в пр€мом направлении (ΔG 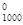 < 0), при 1200 Ц в обратном направлении (ΔG
< 0), при 1200 Ц в обратном направлении (ΔG 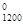 > 0).
> 0).
¬еличину  ΔH
ΔH 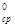 определим по уравнению изобары ¬ант √оффа в интегральном виде ln
определим по уравнению изобары ¬ант √оффа в интегральном виде ln 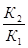 =
= 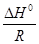 (
(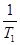 −
− 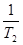 ). ¬ыражаем из уравнени€ ΔH
). ¬ыражаем из уравнени€ ΔH 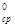 =
= 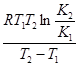 =
= 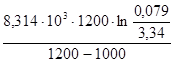 = - 186779,6 ƒж/моль = - 186,8 кƒж/моль.
= - 186779,6 ƒж/моль = - 186,8 кƒж/моль.
ƒл€ удобства расчетов обычно принимают “2 > “1.
ќтвет: ΔG 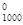 = - 10 кƒж/моль Ц в пр€мом направлении протекает реакци€, ΔG
= - 10 кƒж/моль Ц в пр€мом направлении протекает реакци€, ΔG 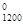 = 25,3 кƒж/моль Ц в обратном направлении протекает реакци€, реакци€ экзотермическа€ ΔH
= 25,3 кƒж/моль Ц в обратном направлении протекает реакци€, реакци€ экзотермическа€ ΔH 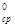 = - 186,8 кƒж/моль.
= - 186,8 кƒж/моль.
ѕример 4. –ассчитать энергию √иббса химической реакции синтеза аммиака
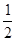 N2 (г) +
N2 (г) + 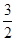 H2 (г) = NH3 (г) при 298 и относительных парциальных давлени€х –Ќ
H2 (г) = NH3 (г) при 298 и относительных парциальных давлени€х –Ќ 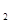 = 100, –N
= 100, –N 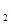 = 100 и PNH
= 100 и PNH 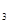 =1. ΔG
=1. ΔG 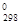 NH
NH 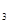 = - 16,66 кƒж/моль.
= - 16,66 кƒж/моль.
–ешение: »спользуем уравнение УизотермыФ химической реакции в нестандартных услови€х ΔG298 = ΔG 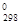 + RT ln
+ RT ln 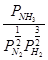
ΔG298 = - 16,66 + 8,314∙10-3 ∙298 ∙ 2,3∙ lg 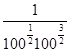 = -16,66 +5,698∙ lg
= -16,66 +5,698∙ lg 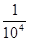 = - 16,66 + 5,698 ∙lg 10-4 = -16,66 + 5,698∙ (-4) = -16,66 Ц 22,792 = - 39,452 кƒж/моль.
= - 16,66 + 5,698 ∙lg 10-4 = -16,66 + 5,698∙ (-4) = -16,66 Ц 22,792 = - 39,452 кƒж/моль.
ΔG298 < 0, реакци€ идет самопроизвольно в пр€мом направлении в указанных услови€х.
ќтвет: ΔG298 = - 39,452 кƒж/моль
онтрольные вопросы:
1. акие из следующих термодинамических функций относ€тс€ к функци€м состо€ни€: теплота, энтропи€, свободна€ энерги€ √иббса, работа расширени€ газа, энтальпи€, изохорно-изотермический потенциал?
2. акой смысл имеют знаки ТТплюсФ или ФминусФ перед термодинамическими функци€ми: теплотой, энтальпией, свободной энергией √иббса?
3. акие выводы можно сделать о конкретной химической реакции, если изменение следующих термодинамических функций отрицательно: а) энтальпии; б) энтропии; в) свободной энергии √иббса?
4. ¬ каком случае дл€ оценки теплового эффекта реакции используетс€: а) первое следствие закона √есса; б) второе следствие закона √есса?
5. ак св€заны между собой тепловой эффект и изменение энтальпии процесса? ”кажите знак ΔH дл€ экзо- и эндотермической реакции.
6. ѕодтвердите физический смысл энтропии математическими формулами и примерами.
7. аким образом производ€т расчет свободной энергии √иббса: а) по величинам свободных энергий образовани€ веществ; б) по энтальпийному и энтропийному факторам; в) по величине электродвижущей силы процесса; г) по константе химического равновеси€ при заданной температуре?
8. ѕочему введены три критери€ направлени€ самопроизвольных процессов ΔS, ΔG, ΔF?
«адани€ дл€ самосто€тельного решени€:
ƒл€ предложенной реакции ответьте на следующие вопросы:
1) экзо- или эндотермической €вл€етс€ данна€ реакци€; определите тепловой эффект образовани€ 1 кг любого из продуктов реакции;
2) как мен€етс€ степень беспор€дка в ходе реакции;
3) возможна ли данна€ реакци€ в изолированной системе при стандартных услови€х;
4) возможна ли данна€ реакци€ в открытой системе при 250— и 1000 . ѕри какой температуре выдел€етс€ больше энергии;
|
|
|
5) какой фактор (энтропийный или энтальпийный) способствует протеканию процесса;
6) запишите выражени€ кинетической и термодинамической равновеси€, покажите взаимосв€зь между ними;
7) рассчитайте числовое значение равновеси€ при температуре 250— и 1000 . ѕри какой температуре полнота протекани€ реакции выше;
8) укажите оптимальные услови€ протекани€ реакции, использу€ принцип Ће Ўателье (услови€, при которых равновесие смещаетс€ в пр€мом направлении).
Ќе забудьте уравн€ть предложенную реакцию.
| Fe2O3 (т) + H2 (г) = FeO (т) + H2O (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | -822,2 | -264,9 | -241,8 | ||||||||||||||||||
| S0, ƒж/моль∙ | |||||||||||||||||||||
| CaC2 (т) + H2O (ж) = Ca(OH)2 (т) + C2H2 (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | -59,83 | -285,8 | -985,1 | 226,75 | |||||||||||||||||
| S0, ƒж/моль∙ | 69,96 | 69,95 | 83,39 | 200,82 | |||||||||||||||||
| NH3 (г) + Cl2 (г) = N2 (г) + HCl (г) | |||||||||||||||||||||
| ∆G0обр, кƒж/моль | -16,48 | -95,3 | |||||||||||||||||||
| S0, ƒж/моль∙ | 192,66 | 222,98 | 191,5 | 186,79 | |||||||||||||||||
| CH4 (г) + O2 (г) = CO2 (г) + H2O (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | -74,85 | -393,5 | -241,8 | ||||||||||||||||||
| S0, ƒж/моль∙ | 186,24 | 213,66 | 188,72 | ||||||||||||||||||
| SO2 (г) + H2S (г) = S (т) + H2O (ж) | |||||||||||||||||||||
| ∆G0обр, кƒж/моль | -300,2 | -33,5 | -237,2 | ||||||||||||||||||
| ∆H0обр, кƒж/моль | -296,9 | -20,6 | -285,8 | ||||||||||||||||||
| C2H2 (г) + O2 (г) = CO2 (г) + H2O (г) | |||||||||||||||||||||
| ∆G0обр, кƒж/моль | 209,2 | -394,4 | -228,6 | ||||||||||||||||||
| ∆H0обр, кƒж/моль | 226,75 | -393,5 | -241,8 | ||||||||||||||||||
| NO2 (г) = NO (г) + O2 (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | 34,19 | 91,26 | |||||||||||||||||||
| S0, ƒж/моль∙ | 240,06 | 210,64 | |||||||||||||||||||
| Fe2O3 (т) + CO (г) = Fe (т) + CO2 (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | -822,1 | -110,5 | -393,5 | ||||||||||||||||||
| S0, ƒж/моль∙ | 87,45 | 197,55 | 27,15 | 213,66 | |||||||||||||||||
| PbS (т) + O2 (г) = PbO (т) + SO2 (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | -100,4 | -219,3 | -296,9 | ||||||||||||||||||
| ∆G0обр, кƒж/моль | -98,77 | -189,1 | -300,2 | ||||||||||||||||||
| KClO3 (т) = KCl (т)+ O2 (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | -391,2 | -436,7 | |||||||||||||||||||
| S0, ƒж/моль∙ | 142,97 | 82,55 | |||||||||||||||||||
| FeS2 (т) + O2 (г) = Fe2O3 (т) + SO2 (г) | |||||||||||||||||||||
| ∆G0обр, кƒж/моль | -166,1 | -740,3 | -300,2 | ||||||||||||||||||
| S0, ƒж/моль∙ | 52,93 | 87,45 | 248,07 | ||||||||||||||||||
| C2H2 (г) + H2 (г) = C2H6 (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | 226,75 | -84,67 | |||||||||||||||||||
| S0, ƒж/моль∙ | 200,8 | 130,5 | 229,5 | ||||||||||||||||||
| CO2 (г) + NH3 (г) = CO(NH2)2 (т) + H2O (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | -393,5 | -45,94 | -333,7 | -241,8 | |||||||||||||||||
| S0, ƒж/моль∙ | 213,66 | 192,66 | 104,6 | 188,72 | |||||||||||||||||
| SiO2 (г) + NaOH (ж) = Na2SiO3 (т) + H2O (ж) | |||||||||||||||||||||
| ∆G0обр, кƒж/моль | -850,7 | -419,5 | -1468 | -237,2 | |||||||||||||||||
| S0, ƒж/моль∙ | 46,86 | 64,43 | 113,76 | 69,95 | |||||||||||||||||
| C2H5OH (ж) + O2 (г) = CO2 (г) + H2O (г) | |||||||||||||||||||||
| ∆H0обр, кƒж/моль | -276,98 | -393,5 | -241,8 | ||||||||||||||||||
| S0, ƒж/моль∙ | 160,7 | 213,7 | 188,7 | ||||||||||||||||||
|
|
|
’имическа€ кинетика
¬ыучитьпон€ти€:
1. скорость химической реакции: истинна€ и средн€€
2. константа скорости химической реакции
3. пор€док и молекул€рность реакции
4. температурный коэффициент скорости реакции
5. энерги€ активации
Ќеобходимо знать:
1. кинетические уравнени€ химических реакций разного пор€дка
2. зависимость константы скорости химической реакции от различных факторов
3. правило ¬ант-√оффа
4. уравнение јррениуса
5. св€зь между энтальпией реакции и энергией активации пр€мой и обратной реакций.
—корость химической реакции определ€етс€ изменением концентрации реагирующих веществ в единицу времени (τ, с).
ƒл€ гомогенной реакции v = 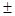
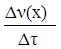 [
[ 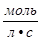 ]
]
ƒл€ гетерогенной реакции v = 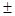
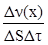 [
[ 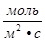 ]
]
¬ажнейшие факторы, вли€ющие на скорость химических реакций: природа и концентраци€ реагирующих веществ, температура процесса, наличие катализатора.
«ависимость скорости химической реакции от концентрации выражаетс€ законом действи€ масс: при посто€нной температуре скорость химической реакции пр€мо пропорциональна действующим массам Ц мол€рным концентраци€м реагирующих веществ, вз€тым в степени соответствующих стехиометрических коэффициентов (дл€ простых реакций) или в степени определ€емой опытным путем (дл€ сложных реакций).
Ќапример, дл€ простой реакции aA + bB = cC + dD
v = kC 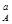 C
C 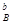 , n
, n 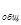 = a + b
= a + b
дл€ сложной реакции aA +bB = cC + dD
v = kC 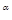 C
C 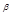 , n
, n 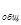 =
= 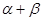
Cумма показателей степеней в кинетическом уравнении называетс€ общим пор€дком реакции (n).
„астный пор€док или пор€док по данному веществу определ€етс€ как показатель степени концентрации этого вещества:
дл€ простой реакции n 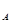 = a, n
= a, n 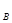 = b
= b
дл€ сложной реакции n 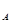 =
= 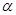 , n
, n 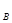 =
= 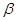
ѕор€док Ц эмпирический параметр, показывающий зависимость скорости реакции от концентрации реагентов. ќн может принимать любые значени€ (целые, дробные, ноль, положительные, отрицательные).
ћолекул€рность реакции Ц число молекул одновременно участвующих в элементарном акте реакции. ѕринимает значени€ 1,2, 3. ќпредел€етс€ по самой медленной стадии процесса, без знани€ механизма реакции молекул€рность определить невозможно.
¬ случае гетерогенных процессов в выражение закона действи€ масс не входит концентраци€ веществ, наход€щихс€ в конденсированной фазе, поскольку реакци€ протекает лишь на их поверхности.
онстанта скорости реакции k Ц фундаментальный кинетический параметр, не завис€щий от концентраций реагентов, а потому остающийс€ неизменным в течение реакции.
онстанта скорости численно равна скорости химической реакции при концентраци€х всех реагирующих веществ равных 1 моль/л.
онстанта скорости зависит от природы реагирующих веществ, температуры, наличи€ в реакционной среде катализатора. 
«ависимость скорости химической реакции от температуры выражаетс€ уравнением ¬ант-√оффа: v 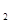 = v ∙
= v ∙ 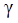
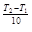
 ,
,
где v 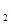 - cкорость реакции при температуре “
- cкорость реакции при температуре “ 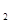 ;
;
v 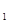 - cкорость реакции при температуре “
- cкорость реакции при температуре “ 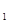 ;
;
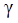 - температурный коэффициент скорости реакции, равный дл€
- температурный коэффициент скорости реакции, равный дл€
большинства гомогенных процессов 2 ~ 4.
”равнение ¬ант-√оффа показывает, что при повышении температуры на каждые 10  — скорость химической реакции возрастает в 2 ~ 4 раза.
— скорость химической реакции возрастает в 2 ~ 4 раза.
Ѕолее точную зависимость скорости химической реакции от температуры устанавливает уравнение јррениуса: k = k 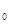 e
e 
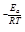 ,
,
где k Ц константа скорости реакции при температуре “; k 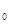 - предэкспоненциальный множитель, пропорциональный числу столкновений реагирующих частиц; ≈
- предэкспоненциальный множитель, пропорциональный числу столкновений реагирующих частиц; ≈ 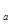 - энерги€ активации (кƒж/моль) реакции, то избыточное количество энергии которым должна обладать молекула в момент столкновени€, чтобы быть способной к химическому взаимодействию; R Ц универсальна€ газова€ посто€нна€, ее значение 8,314 ∙10-3
- энерги€ активации (кƒж/моль) реакции, то избыточное количество энергии которым должна обладать молекула в момент столкновени€, чтобы быть способной к химическому взаимодействию; R Ц универсальна€ газова€ посто€нна€, ее значение 8,314 ∙10-3 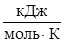 .
.
”равнение јррениуса дл€ температурного интервала от 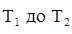 имеет следующий вид:
имеет следующий вид:
ln 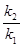 =
= 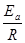 (
(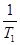 ―
― 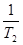 ) или lg
) или lg 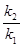 =
= 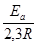 (
(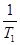 ―
― 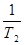 ),
),
где k 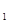 - константа скорости реакции при температуре “
- константа скорости реакции при температуре “ 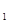 ; k
; k 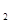 - константа скорости реакции при температуре “
- константа скорости реакции при температуре “ 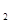 .
.
Ќа скорость химических реакций существенное вли€ние оказывают катализаторы Ц вещества, ускор€ющие данную реакцию за счет образовани€ промежуточных соединений с реагентами и выход€щие из химического процесса без изменени€. ”равнение јррениуса дл€ каталитического процесса имеет вид 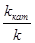 =
= 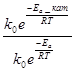 = е
= е 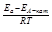 ,
,
где k 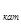 - константа скорости каталитической реакции с энергией активации ≈
- константа скорости каталитической реакции с энергией активации ≈ 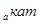 ; k Ц константа скорости некаталитической реакции с энергией активации ≈
; k Ц константа скорости некаталитической реакции с энергией активации ≈ 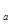 .
.
ѕример 1. ќпределить пор€док и молекул€рность реакции
S 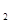 O
O 
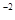 + 3I
+ 3I 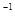 = 2SO
= 2SO 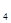
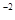 + I
+ I 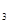
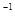 , если еЄ скорость описываетс€ уравнением v = k∙C
, если еЄ скорость описываетс€ уравнением v = k∙C 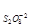 ∙—
∙— 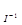 .
.
–ешение: «на€, что пор€док по веществу Ц это степень в которой находитс€ концентраци€ данного вещества в выражении закона действи€ масс, находим пор€док по каждому из участвующих в реакции веществ: n 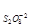 = 1, n
= 1, n 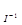 =1.
=1.
|
|
|
ќбщий пор€док реакции n 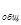 = n
= n 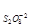 + n
+ n 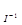 = 1 + 1 = 2.
= 1 + 1 = 2.
ћолекул€рность реакции определить невозможно, т.к. неизвестен механизм реакции.
ќтвет: n 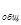 = 2, молекул€рность определить невозможно по данным задачи.
= 2, молекул€рность определить невозможно по данным задачи.
ѕример 2. –еакци€ взаимодействи€ оксида азота (II) с кислородом имеет второй пор€док по оксиду азота (II) и первый по кислороду. ”казать общий пор€док реакции и определить значение и размерность константы скорости, если при — 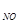 = 0,3 моль/л и —
= 0,3 моль/л и — 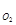 = 0,15 моль/л скорость реакции составл€ет 1,2∙10
= 0,15 моль/л скорость реакции составл€ет 1,2∙10 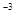 моль/л∙с.
моль/л∙с.
–ешение: »спользу€ условие, записываем выражение закона действи€ масс v = k∙— 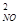 ∙—
∙— 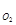 . ќбщий пор€док реакции равен 3 (n
. ќбщий пор€док реакции равен 3 (n 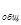 = n
= n 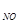 + n
+ n 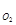 = 2 + 1 = 3). онстанту скорости реакции рассчитываем по уравнению
= 2 + 1 = 3). онстанту скорости реакции рассчитываем по уравнению
k = 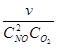 =
= 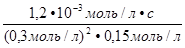 = 8,89∙10
= 8,89∙10 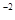
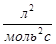 .
.
ќтвет: n  = 3, k = 8,89∙10
= 3, k = 8,89∙10 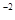
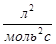
ѕример 3. ѕри 1500 — некотора€ реакци€ заканчиваетс€ за 16 мин. “емпературный коэффициент реакции равен 2,5. „ерез какое врем€ закончитс€ эта реакци€ при 80  —? ак изменитс€ скорость реакции?
—? ак изменитс€ скорость реакции?
–ешение: ¬оспользуемс€ уравнением ¬ант-√оффа
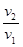 =
= 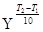 = 2,5
= 2,5 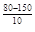 = 2,5
= 2,5 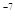 =
= 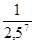 =
= 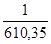 .
.
Cкорость реакции, при понижении температуры со 150 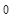 — до 80
— до 80 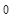 —, уменьшитс€ в 610, 35 раз. «на€, что скорость реакции и врем€ еЄ протекани€ обратно пропорциональны, замен€ем соотношение скоростей соотношением времен
—, уменьшитс€ в 610, 35 раз. «на€, что скорость реакции и врем€ еЄ протекани€ обратно пропорциональны, замен€ем соотношение скоростей соотношением времен 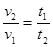 . ќтсюда,
. ќтсюда, 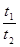 =
= 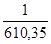 . t
. t 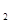 = 610,35∙ t
= 610,35∙ t 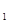 = 610,35 ∙16 мин =
= 610,35 ∙16 мин =
= 9765,6 мин = 162,76 ч = 6,78 сут.
ќтвет: при 80 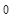 — реакци€ закончитс€ через 6,78 суток; скорость реакции уменьшитс€ в 610,35 раз.
— реакци€ закончитс€ через 6,78 суток; скорость реакции уменьшитс€ в 610,35 раз.
ѕример 4. ќпределить, как изменитс€ скорость пр€мой реакции
2—ќ 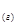 +ќ
+ќ 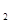
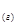 = 2—ќ
= 2—ќ 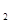
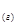 , если общее давление в системе увеличить в 4 раза.
, если общее давление в системе увеличить в 4 раза.
–ешение: ”величение давлени€ в системе в 4 раза вызовет уменьшение обьема системы в 4 раза, а концентрации реагирующих веществ возрастут в 4 раза. —огласно закону действи€ масс дл€ гомогенных реакций начальна€ скорость реакции равна v 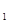 = k∙C
= k∙C 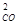 ∙C
∙C 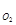 . ѕосле увеличени€ давлени€
. ѕосле увеличени€ давлени€
v 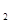 = k∙ (4C
= k∙ (4C 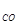 )
) 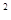 ∙4C
∙4C 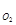 = k∙ 4
= k∙ 4 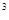 ∙C
∙C 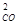 ∙C
∙C 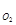
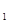 = 64 k ∙C
= 64 k ∙C 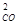 ∙C
∙C 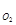 .
.
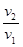 =
= 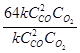 = 64.
= 64.
ќтвет: после увеличени€ давлени€ в 4 раза скорость реакции возросла в 64 раза.
онтрольные вопросы:
1. „то называют скоростью химической реакции? ¬ чем отличие пон€тий средней и истинной скоростей реакции? акова размерность скорости химической реакции?
2. акова формулировка основного закона химической кинетики Ц закона действи€ масс?
3. акие факторы вли€ют на скорость химической реакции? ¬ чем заключаетс€ различие кинетики гомогенных и гетерогенных химических реакций?
4. „то такое константа скорости химической реакции, от каких факторов она зависит?
5. „то такое пор€док и молекул€рность химической реакции? ак на основе этих пон€тий классифицируютс€ химические реакции? „то называетс€ общим и частным пор€дком реакции?
6. „то отражает кинетическое уравнение реакции? Ќаписать уравнени€ реакции I, II, III пор€дков.
7. акова зависимость скорости реакции от температуры? „то такое температурный коэффициент скорости реакции, в каких пределах он измен€етс€?
8. „то такое энерги€ активации реакции? Ќаписать выражение зависимости скорости реакции от температуры и энергии активации (уравнение јррениуса).
9. „то такое катализ? аковы представлени€ о механизме катализа? ¬ли€ет ли на энергию активации процесса введение катализатора?
«адани€ дл€ самосто€тельного решени€:
1. «аписать выражение закона действи€ масс дл€ данной реакции, указать общий пор€док реакции и пор€док по каждому, из участвующих в реакции, веществ. ак изменитс€ скорость реакции при условии а и б.
| уравнение реакции | а | б | |
| 2NO(г)+ —l2(г) = 2NOCl(г) | повысить P в 4 раза | понизить CNO в 50 раз | |
| 2CO(г) = CO2(г)+C(к) | понизить P в 5 раз | повысить C в 4 раза | |
| N2O4(г) = 2Nќ2(г) | повысить P в 8 раз | понизить C в 7 раз | |
| NO2(г)+CO(г) = NO(г)+CO2(г) | понизить P в 4 раза | повысить C в 80 раз | |
| Ќ2(г)+Cl(г) = HCl(г)+H(г) | повысить P в 2 раза | понизить C в 20 раз | |
| Cl2(г)+H(г) = HCl(г)+Cl(г) | понизить P в 7 раз | повысить C в 55 раз | |
| 2NO2(г) = N2O4(г) | повысить P в 10 раз | понизить C в 99 раз | |
| CaO(к)+—O2(г) = CаCO3(к) | понизить P в 6 раз | повысить C в 4 раза | |
| HCl(г) = Ќ(г)+Cl(г) | повысить P в 8 раз | понизить C в 12 раз | |
| NO(г)+ќ(г)= NO2(г) | понизить P в 9 раз | повысить C в 56 раз | |
| (CH3)2CO(г) = C2H6(г)+CO(г) | повысить P в 2 раза | понизить C в 98 раз | |
| 2H2O2(г)= 2H2O(г)+O2(г) | понизить P в 5 раз | повысить C в 65 раз | |
| 2NO(г)+O2(г) = 2NO2(г) | повысить P в 3 раза | понизить C в 2 раза | |
| —(графит)+O2(г) = CO2(г) | понизить P в 9 раз | повысить C в 9 раз | |
N2O5(г) = 2NO2(г)+ 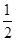 O2(г) O2(г)
| повысить P в 2 раза | понизить C в 5 раз |
2. “емпературный коэффициент скорости реакции равен 3,2. ак изменитс€ скорость реакции, если повысить температуру на 400?
3. ак следует изменить температуру, чтобы скорость реакции увеличилась в 8 раз (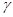 =2)?
=2)?
4. «а какое врем€ пройдет реакци€ при 600 —, если при 200 — она заканчиваетс€ за 40 с, а температурный коэффициент равен 2,3?
5. ¬ычислить температурный коэффициент скорости реакции, если понижение температуры на 40 вызывает уменьшение скорости реакции в 140 раз.
6. ѕри 1400 — реакци€ заканчиваетс€ за 30 с. —колько времени потребуетс€ дл€ данной реакции при 200 —, если 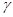 =2?
=2?
7. “емпературный коэффициент скорости реакции равен 3. ак изменитс€ скорость реакции при уменьшении температуры с 1250 до 550 —?
8. ѕри повышении температуры на 200 — скорость реакции возросла в 9 раз. „ему равен температурный коэффициент этой реакции и во сколько раз увеличитс€ ее скорость при повышении температуры с 200 до 1000 —?
9. “емпературный коэффициент скорости реакции равен 2,5. ак изменитс€ ее скорость: а) при охлаждении реакционной смеси от 500 до 300 —; б) при повышении температуры на 600 —?
10. ѕри повышении температуры от 200 до 400 — скорость реакции увеличилась в 6 раз. ¬ычислить температурный коэффициент и энергию активации реакции.
11. ¬ычислить температурный коэффициент скорости реакции гидролиза сахарозы в кислом водном растворе (100-500 —), ≈а = 107 кƒж/моль.
12. ак изменитс€ скорость реакции при повышении температуры с 600 до 650 , если энерги€ активации равна 26,6 кƒж/моль?
13. ак изменитс€ скорость реакции при повышении температуры с 307 до 377 , если энерги€ активации равна 186,8 кƒж/моль?
14. ¬ведением катализатора энерги€ активации реакции при 40 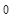 — снижена на 50 кƒж/моль. ак изменитс€ скорость реакции?
— снижена на 50 кƒж/моль. ак изменитс€ скорость реакции?
15. ѕри 45 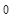 — реакци€ завершаетс€ за 150 с, а при 55
— реакци€ завершаетс€ за 150 с, а при 55 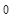 — Ц за 75 с. ¬ычислить энергию активации реакции.
— Ц за 75 с. ¬ычислить энергию активации реакции.
16. — выводом катализатора из системы, энерги€ активации реакции увеличилась на 30 кƒж/моль при температуре 20 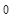 —. ак изменитс€ скорость химической реакции?
—. ак изменитс€ скорость химической реакции?
17. ѕри 37 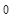 — реакци€ заканчиваетс€ за 150 с. —колько потребуетс€ времени дл€ проведени€ этой реакции при 47
— реакци€ заканчиваетс€ за 150 с. —колько потребуетс€ времени дл€ проведени€ этой реакции при 47 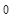 —, если энерги€ активации равна 57,2 кƒж/моль?
—, если энерги€ активации равна 57,2 кƒж/моль?
18. ¬ присутствии катализатора энерги€ активации некоторой реакции снижаетс€ с 80 до 55 кƒж/моль при температуре 20 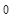 —. ак изменитс€ скорость реакции в этом случае?
—. ак изменитс€ скорость реакции в этом случае?
19. ак изменитс€ скорость реакции при понижении температуры с 50 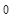 — до 20
— до 20 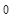 —, если энерги€ активации равна 28,8 кƒж/моль?
—, если энерги€ активации равна 28,8 кƒж/моль?
20. Ёнерги€ активации разложени€ пероксида водорода составл€ет 75 кƒж/моль. ¬ присутствии коллоидной платины она уменьшаетс€ до 49 кƒж/моль, а в присутствии каталазы до 23 кƒж/моль. ¬о сколько раз измен€ют скорость реакции обычный катализатор и фермент при 300 ?
21. ак изменитс€ скорость реакции при повышении температуру до 50 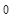 —, если энерги€ активации равна 125,5 кƒж/моль?
—, если энерги€ активации равна 125,5 кƒж/моль?
22. ѕосле удалени€ катализатора из системы, энерги€ активации реакции возросла на 40 кƒж/моль при температуре 37 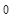 —. ак изменилась скорость реакции?
—. ак изменилась скорость реакции?
23. –еакци€ при 20 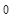 — завершаетс€ за 60 с. —колько дл€ этого потребуетс€ времени при 40
— завершаетс€ за 60 с. —колько дл€ этого потребуетс€ времени при 40 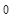 —, если энерги€ активации равна 33,4 кƒж/моль?
—, если энерги€ активации равна 33,4 кƒж/моль?
24. ¬ведением катализатора, энерги€ активации реакции при 29 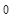 — снижена на 30 кƒж/моль. ак изменилась скорость реакции?
— снижена на 30 кƒж/моль. ак изменилась скорость реакции?
25. ѕри повышении температуры с 20 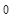 до 50
до 50 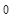 — скорость реакции возросла в 3 раза. „ему равна энерги€ активации реакции?
— скорость реакции возросла в 3 раза. „ему равна энерги€ активации реакции?
26. Ёнерги€ активации реакции разложени€ некоторого вещества равна 
 75 кƒж/моль, а обратной реакции Ц 265 кƒж/моль. –ассчитайте температурный коэффициент скорости пр€мой реакции в интервале 600 Ц 800— и стандартную энтальпию реакции.
75 кƒж/моль, а обратной реакции Ц 265 кƒж/моль. –ассчитайте температурный коэффициент скорости пр€мой реакции в интервале 600 Ц 800— и стандартную энтальпию реакции.
ћодуль 4. –астворы






