

 CH3 NO2 CH3 NH3 CH3
CH3 NO2 CH3 NH3 CH3





 O=N-CH3 HNO3 O= N-CH3 [H] O= N-CH3 +2CH3J
O=N-CH3 HNO3 O= N-CH3 [H] O= N-CH3 +2CH3J
-H2O -H2O -2HJ
N N N
C6H5 C6H5 C6H5
4-аминоантипирин
 N(CH3)2 CH3
N(CH3)2 CH3
 O= N-CH3
O= N-CH3
N
C6H5
Качеств.их можно различить с помощью азотистой к-ты и FeCl3 (см.практикум)
Тиазол
Производные
** Вход в состав вит.В1

 NH2 N+ CH3
NH2 N+ CH3

 N CH2 - CH2CH2OH
N CH2 - CH2CH2OH
H3C N S
Тиазольное кольцо
**2-аминотиазол исп-ся в произв-ве лек.средств.



 O N
O N


 H2N -S-NH-
H2N -S-NH-
 O
O
S
** Тиазолидин вход.в сост.пинициллина
 H2C N-H
H2C N-H
H2C CH2
S
Общая формула пинициллина.




 HOOC N O
HOOC N O

 H3C NH-C-R
H3C NH-C-R
 CH3 S
CH3 S
Β-лактамное кольцо
Тиазомидиновое
Кольцо
Шестичл.гетероциклы с 1-ми гетероатомом.
 | |||||
 |  | ||||



 N
N
N N
Пиридин хинолин изохинолин
Азины
Все яв-ся ароматич, но в отл.от 5-ти членных неподел.пара е- N не учавств.в сопряж.
Пиридин
Азот проявляет ЭА характер, это П-недостаточная система.
 4(б)
4(б)
(β’)5 3(β)
(α’)6 2(α)
N
..1
 Получение:
Получение:
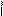 1) 2CHaCH+HCN –4000о®
1) 2CHaCH+HCN –4000о®
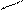
 2) 2CHaCH+NH3 4000о
2) 2CHaCH+NH3 4000о
Al2O3 N
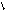
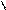 3) CH3-C=O + NH3 + H-C=O –to®
3) CH3-C=O + NH3 + H-C=O –to®
H H
По Чичибабину
Хим.св-ва:
** основные
Связаны с наличием свободной пары е- у атома N.
Основность пиридина меньше, им у алифат.аминов, в пиридине пара е- занимает sp2 гибр.орбиталь, а в аминах sp3 , т.к. ЭО N в sp2 > ЭО N в sp3 гибр.
- реаг.с водой


 +
+




 +Hб+OHб- OH- лакмус-синеет
+Hб+OHб- OH- лакмус-синеет
 ..N N
..N N
- реаг.как с мин.к-ами, так и с орг.-пикриновой к-ой, α-ая исп-ся для идентиф.пиридина.



 +
+


 + HBr Br-
+ HBr Br-
 |  |
N N
H

 OH
OH



 O2N NO2 + NO2
O2N NO2 + NO2
 + N-H O- - NO2
+ N-H O- - NO2
N NO2 NO2
Пикрат пиридинил
**реак.электрофильного замещения,т.к.N проявл.ЭА характер,поэтому пиридин, по сравн.с бензолом, яв-ся
П-недост.системой.
Реак. SE идут труднее, чем у C6H6.
Кроме того в кисл.среде, кольцо более дезактивируется, из-за обр-ия пока пиридиния.
 Br 300o Br реак SE идут в В-положении.
Br 300o Br реак SE идут в В-положении.


 Галоген -HBr
Галоген -HBr


 N
N
N

 KNO3+H2SO4; 300о NO2
KNO3+H2SO4; 300о NO2
 нитрировние
нитрировние
-K2SO4 -H2O
N


 H2SO3 SO3; 200o SO3H
H2SO3 SO3; 200o SO3H
 Сульфир B-пиридинсульфо к-та
Сульфир B-пиридинсульфо к-та
N
**реак. Sn
Если для C6H6 реак. SN вообще не идут, то у пиридина эти реак.идут в α-положении. Если это полож.занято, то в γ-полож.
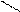
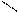




 NaNH2, to
NaNH2, to



 Аминиров. HOH
Аминиров. HOH
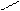
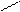
 б+ -Н2 NHNa -NaOH NH2
б+ -Н2 NHNa -NaOH NH2
N N N α-амигопиридин

 KOH, to
KOH, to


 Гидроксил.
Гидроксил.
 -Н2 OH HOH OH
-Н2 OH HOH OH
 N N
N N
Для гидроксипроизв.хар-на лактил-лактанная таутомерия.
 | |||||
 | |||||
 | |||||

 OH =O
OH =O
 ..N N
..N N
Лактимная форма лактамная форма
Преоблад.в р-ре, т.к:
1) средство к протоку у ат.N, больше чем к О.
2) цепь сопряж.длинее
**Nu св-ва.
Связана с налич.свобод.пары е- ат N.
1) алкилирование
 | |||
 | |||


 + CHб+3Jб-
+ CHб+3Jб-
 J- иодистый N-метилперединин
J- иодистый N-метилперединин
..N N+
CH3
2)ацилирование
 | |||||
 |  | ||||

 + CH3C=O N-C-CH3 Cl - исп-ся как хороший ацил.реагент.
+ CH3C=O N-C-CH3 Cl - исп-ся как хороший ацил.реагент.
 ..N Cl
..N Cl
 | |||
 | |||

 + SO3 N+ - SO3- пиридин сульфотриоксид.хороший сульфирующ.реагент.
+ SO3 N+ - SO3- пиридин сульфотриоксид.хороший сульфирующ.реагент.
 | |||
 | |||
..N
3) восстановление
В хим.повед, как со втор.амины.

 CH2
CH2
 [H] H2C CH2
[H] H2C CH2

 C2H5OH + Na H2C CH2 пипиридин
C2H5OH + Na H2C CH2 пипиридин
..N N
 H
H
 3H2/Pt
3H2/Pt
4H2/Pt, 70атм CH3-CH2-CH2-CH2 -CH2NH2
 Пентанамин -1
Пентанамин -1
- Окисление
При окисл.пироксикислотами идет окисл.по N.
 | |||
 | |||


 CH3COOH N-оксидпиридана легкор восст.до исх.пиридина.
CH3COOH N-оксидпиридана легкор восст.до исх.пиридина.
 | |||
 | |||
 ..N N
..N N
O
Производные пиридина



 CH3
CH3


 CH3
CH3
 CH3
CH3
N N N
Пиколины (гомологи пиридина)
α-пиколин
(2-метил-пиридин)
Α-метил-
Пиридин.
При их окисл.обр-ся к-ты.


 COOH
COOH



 COOH
COOH
 COOH
COOH
N N N
Пиколиновая к-та. Никотиновая к-та. Изоникот.к-та.
Произв.к-т
Никот.к-та и ее амид-витамин РР(антипилогрич.витам.)
В свою очередь никотин амид входит в состав коферментов: НАД + и НАДФ +, α-ые участв.в О-ВР, связанных с перкосом гидрид иона.


 C=O
C=O
 NH2
NH2
N




 [H-] H H
[H-] H H





 C=O + R-H C=O
C=O + R-H C=O
 NH2 H NH2 + R + H+
NH2 H NH2 + R + H+
N+ N
R R
НАД+ НАДН
Окисленная форма восстан.форма конфермента
Гидразит изоник.к-ты, под названием тубазид, исп.в мед.для лечения туюеркулеза.
При конденс.тубазида с ванилином получ.еще более преперата-фтевазид.
 С=O
С=O
 NH-NH2
NH-NH2
N












 N C=O O
N C=O O

 NH-NH2 + O= C OH N C-NH-N=CH OH
NH-NH2 + O= C OH N C-NH-N=CH OH
 H OCH3 -H2O OCH3
H OCH3 -H2O OCH3
ванилин
Хинолин
5 4(γ)



 6 3(B)
6 3(B)
 7 2(α)
7 2(α)
8 N1
Синтез по Скраупу
 NH2
NH2
 | |||
 | |||


 + CH2 CH2 CH2 C2H5NO2, to
+ CH2 CH2 CH2 C2H5NO2, to
 OH OH OH H2SO4 хинолин
OH OH OH H2SO4 хинолин
1) дегидрат.глицерина с обр.акрилового альдегида



 CH2CH CH2 H2SO4 CH2=CH-C=O
CH2CH CH2 H2SO4 CH2=CH-C=O
OH OH OH -H2O H







 2) O=C-H CH
2) O=C-H CH



 + CH б+2 = СР-С=O H CH2 -H2O OH
+ CH б+2 = СР-С=O H CH2 -H2O OH

 H N-CH2 OH2
H N-CH2 OH2
..NH2 N
H

 C6H5NO2
C6H5NO2
 C6H5NH2
C6H5NH2
N
Хим.св-ва:
**основные
Реак.те же, что и у пиридина (с H2O и H+) по атому N.
** SE
Протекают преимущ.в полож.5 и 8 – бензольного кольца.





 NO2
NO2




 + HNO3(k) H2SO4(k) +
+ HNO3(k) H2SO4(k) +
 -H2O
-H2O
N NO2 N N
** SN
Аминир.и гауроксил.идут в α-полож.бензольного кольца.
 |  |

 + 1) NaNH2
+ 1) NaNH2
 2) H2O NH2
2) H2O NH2
N N
** восстановление

 легко гидрируется
легко гидрируется
 |




 H2/Ni, t o 1.2.3.4-тетрагидрохенолин
H2/Ni, t o 1.2.3.4-тетрагидрохенолин
N

 H
H

 N
N
 H2/Ni, t o, P
H2/Ni, t o, P
Декагидрохинолин
N
H
** окисление
 | |||
 | |||
 + CH3COOH
+ CH3COOH
 N-оксидхинолин
N-оксидхинолин
 N N
N N
O



 KMnO4, to HOOC
KMnO4, to HOOC
 |
N HOOC хинолиновая к-та. (2,3-пиридинкарб.к-та)
N
Производные хинолина
8-гидроксихинолина(оксин)
Исп-ся как аналит.реагент, легко обр.компл.с Mg2+, Zn2+

OH N
На основе оксина известны противомикробные препараты бактерицидное действ.основано на связ.СО2+, необх.для жизнедеят.микроорган.

 NO2
NO2

 HNO3(k) 8-гидрокси-5-нитро-хинолин (5-НОК)
HNO3(k) 8-гидрокси-5-нитро-хинолин (5-НОК)

 -H2O
-H2O

 + OH N
+ OH N




 OH N
OH N
 H2SO4(k)
H2SO4(k)
 SO4 8-гидроксихиналиний сульфат(антисепт.ср)
SO4 8-гидроксихиналиний сульфат(антисепт.ср)
OH N
H 2

 Сl
Сl

 8-гидрокси-7-йод-5-хлор-хинолин
8-гидрокси-7-йод-5-хлор-хинолин

 J энтересептол
J энтересептол
OH N






