
Продолжение табл. 10.4

Окончание табл. 10.4 
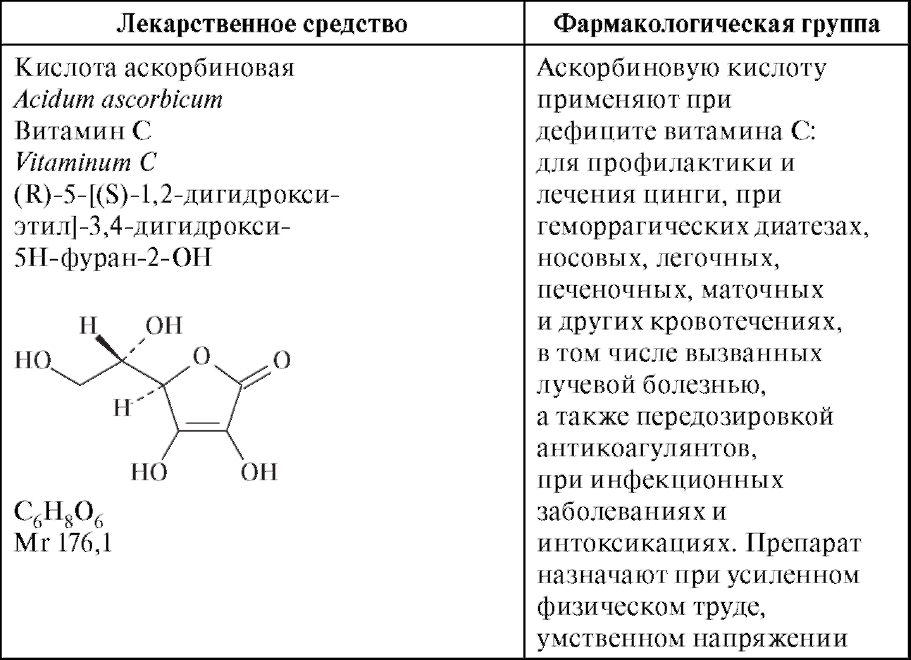
Гидроксикислотами называют соединения, в молекулах которых содержатся гидроксильная и карбоксильная группы.
Появление гидроксигруппы, обладающей положительным индуктивным эффектом, приводит к увеличению силы кислоты. Например, молочная кислота более сильная, чем пропионовая. Их константы ионизации равны 1,3х10-5 и 1,5х10-4 соответственно. Это связано с электронодонорными свойствами заместителя в молекуле молочной кислоты:

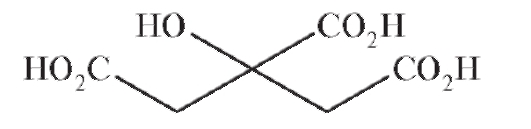
Гидрокситрикарбоновая кислота - лимонная - применяется в медицине в виде натриевой соли, натрия цитрата. В молекуле лимонной кислоты содержится 3 карбоксильных и 1 гидроксигруппа:
Гидроксикислоты могут подвергаться внутримолекулярной этерификации с образованием лактонов.
Лактоны - соединения, в которых сложноэфирная группировка -C(O)O включена в циклическую структуру. Примером лактона является аскорбиновая кислота (витамин С) (см. табл. 10.4).
Аминокислотами называют гетерофункциональные соединения, молекулы которых содержат одновременно амино- и карбоксильную группы.
В зависимости от местоположения аминогруппы по отношению к карбоксильной группе аминокислоты алифатического ряда делят на группы. Если аминогруппа находится в а-положении, то это а-аминокислоты (2-аминокислоты) общей формулы:

6-Аминогексановая (аминокапроновая) кислота, H2N-CH2-(CH2)4COOH, применяется как ЛС.
Аминокислоты как структурные единицы пептидов и белков играют важную роль в биологических процессах. Из белковых гидролизатов получено более 20 а-аминокислот.
Аминокислоты условно называют заменимыми, если они синтезируются в организме человека. «Незаменимые» аминокислоты не синтезируются в организме человека или синтезируются в недостаточном количестве («частично заменимые») и должны пополняться с пищей. Представителем подобных кислот является, например, метионин.
Все природные аминокислоты, кроме глицина (H2N-CH2- COOH) и ω-аминокислот, в которых аминогруппа находится на конце углеродной цепи, содержат хиральный центр и существуют в виде стереоизомеров (оптических, конфигурационных изомеров). Аминокислоты, входящие в состав белков животного происхождения, обычно являются L-изомерами. D-Аминокислоты входят в состав белка крайне редко. Так, D-глутаминовая кислота входит в состав белка клеточной стенки бактерии сибирской язвы. D-изомеры обнаружены также в некоторых природных антибиотиках (D-диметилцистеин в пенициллине, D-фенилаланин - в грамицидине).
Аминокислоты алифатического ряда представляют собой белые кристаллические вещества, как правило, растворимые в воде и нерастворимые в органических растворителях.
Все аминокислоты - амфолиты и способны реагировать как со щелочами, так и с минеральными кислотами.
В водных растворах аминокислоты могут существовать в форме диполярных ионов (цвиттер-ионов):
+nh3-chr-coo-
Значение рН, при котором существует диполярный ион, называется изоэлектрической точкой (р1). В зависимости от рН среды аминокислота может быть полностью протонирована (катионная форма) или полностью депротонирована (анионная форма):

Аминокислоты вступают в реакции этерификации (по карбоксильной группе), алкилирования и ацилирования (по аминогруппе), могут восстанавливаться, подвергаться декарбоксилированию, образовывать пептиды и т.д.
Для идентификации аминокислот используют их способность к образованию внутрикомплексных соединений с различными катионами (серебра, меди, ртути, свинца, цинка, кобальта и др.). Например, с катионом Си2+ образуется внутрикомплексное координационное соединение темно-синего цвета:

Для обнаружения аминокислот применяют и высокочувствительную нингидриновую реакцию, которая позволяет отличить аминокислоты от пептидов и белков. Она протекает при одновременном участии амино- и карбоксильной группы.
Хромогенные реакции с солями меди, нингидрином и другими реактивами используют для фотоколориметрического определения аминокислот.
Применение аминокислот в медицинской практике основано на их способности участвовать в азотистом обмене, синтезе необходимых для нормальной функции организма белков, пептидов, ферментов, гормонов.
В качестве ЛС наиболее часто применяют следующие аминокислоты и их синтетические аналоги: аминалон, кислоту аминокапроновую, кислоту глутаминовую, цистеин, ацетилцистеин, метионин.
Природные аминокислоты можно получить гидролизом белков в среде хлороводородной или серной кислоты при нагревании. Источником белков служат мясо, кожа, желатин, шерсть, волосы, перо, казеин творога.
Перечисленные химические свойства карбоновых кислот используют в фармацевтическом анализе для идентификации и количественного определения ЛС.
Ниже рассмотрим нормативные требования к контролю качества субстанции натрия цитрата, используемой для приготовления инъекционных препаратов, субстанции кальция глюконата, а также производных карбоновых кислот - аскорбиновой кислоты (лактон гидроксикарбоновой кислоты) и аминокислот - глутаминовой и аминокапроновой.






