Второе начало термодинамики имеет особый статус не только фундаментального закона физики, но и универсального принципа естествознания в целом.
Второе начало дает информацию о направлении процессов, которые могут происходить в действительности. Оно, совместно с первым началом, позволяет установить множество точных количественных соотношений между различными макроскопическими параметрами тел в состоянии термодинамического равновесия. Это оказывается возможным благодаря определению такой величины как энтропия через теплоту. Энтропия (греч. – поворот, превращение) служит мерой преобразования или эволюции системы.
Существует несколько десятков различных формулировок второго начала. В большинстве из них термин «энтропия» не используется (см. формулировки Кельвина, Клаузиуса и Оствальда).
| Второе начало термодинамики | ||
| Формулировка Кельвина: Невозможен циклический процесс, единственным результатом которого является производство работы А за счет уменьшения внутренней энергии U только одного теплового резервуара (рис.13) | Формулировка Клаузиуса: Невозможен циклический процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому (рис.14) | Формулировка Оствальда: Невозможно построить «вечный двигатель второго рода». |
Такие процессы невозможны. Они запрещены вторым началом.
|
|
|
Часть первая. Каждая термодинамическая система обладает функцией состояния, называемой энтропией. Энтропия вычисляется следующим образом. Система переводится из произвольно выбранного начального состояния в соответствующее конечное состояние через последовательность состояний равновесия. Вычисляются все подводимые при этом к системе порции тепла 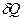 , делятся каждая на соответствующую ей абсолютную температуру Т и все полученные таким образом значения суммируются.
, делятся каждая на соответствующую ей абсолютную температуру Т и все полученные таким образом значения суммируются.
 (13)
(13)
Часть вторая. При реальных (не идеальных) процессах энтропия замкнутой системы возрастает.
Содержание второй части формулировки А.Зоммерфельда в большинстве учебников рассматривается как самодостаточная формулировка второго начала, или как закон возрастания энтропии:
 (14)
(14)
Энтропия не убывает только в процессах изолированной системы, в неизолированной системе энтропия может и возрастать, и убывать, и оставаться неизменной. Рост энтропии в изолированной системе означает приближение системы к состоянию термодинамического равновесия; в этом состоянии S – максимальна, а dS=0. 
Расчет изменения энтропии в различных процессах изучаемых систем зачастую является актуальной внутренней подзадачей разнообразных задач термодинамики, химии биологии, лингвистики. В частности, изменение энтропии служит мерой изменения качества энергии. Важнейшим условием для тепловых машин, работающих по произвольному циклу, является условие их максимально допустимой эффективности:
 (за цикл) (15)
(за цикл) (15)
Большинство процессов, происходящих в природе, необратимы, например: диффузия, расширение, растворение. Для таких процессов вычисление энтропии основывается на том, что S – функция состояния. Если система перешла из одного состояния в другое необратимым образом, то можно мысленно заменить необратимый процесс обратимым, причем начальное и конечное состояния этого процесса должны быть равновесны, рассчитанное в этом случае изменение энтропии будет равно изменению энтропии при реальном необратимом процессе.

Задачи
3.1. Произвольное рабочее вещество совершает цикл, в пределах которого абсолютная температура изменяется в α раз. Цикл имеет вид изображенный на рис.15: T – температура, S – энтропия. Найти КПД цикла.
|
3.3. Найти приращение энтропии алюминиевого бруска массы m=3.0кг при нагревании его от Т1=300˚К до Т2=600˚К, если в этом интервале температур удельная теплоемкость алюминия с=а+bТ, где а=0,77Дж/гК, b=0.46мДж/гК2.
3.4. Вычислить изменения внутренней энергии и энтропии одного моля идеального газа при расширении по политропе pVn=const от объема V1 до объема V2. рассмотреть частные случаи изотермического и адиабатического процессов.
3.5. Гелий массы m=1,7г адиабатически расширили в n=3 раза и затем изобарически сжали до первоначального объема. Найти приращение энтропии газа в этом процессе.
3.6. В двух сосудах одного и того же объема находятся различные идеальные газы. Масса газа в первом сосуде М1, во втором М2, давления газов и их температуры одинаковы. Сосуды соединили друг с другом и начался процесс диффузии. Определить суммарное изменение ∆S энтропии рассматриваемой системы, если относительная молекулярная масса первого газа μ1, а второго μ2.
 |
3.7. Идеальный одноатомный газ в количестве υ=10 молей, находящийся при температуре Т1=300˚К, расширяется без подвода и отдачи тепла в пустой сосуд через турбину, необратимым образом совершая работу (рис.16) После установления равновесия температура газа понижается до Т=200˚К.
|
|
3.8. Вычислить изменение энтропии при смешении одноатомного идеального газа массы m1, имеющего начальную температуру Т1 и давление p1, и двухатомного газа массы m2, имеющего начальные температуру Т2 и давление p2. Молярные массы смешиваемых газов М1 и М2.
Ответы
3.1. 
3.2. 
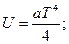
3.3. 
3.4. 

где k=const;
3.5. 
3.6. 
3.7. 
3.8. 
Семинар 4. Реальные газы
Уравнение состояния газа Клапейрона-Менделеева имеет ограниченную область применимости, поскольку не учитывает межмолекулярные взаимодействия. В реальных газах есть дальнодействующие силы притяжения и короткодействующие силы отталкивания. Взаимодействие в газах приводит к количественным и качественным отклонениям от поведения, предсказываемого уравнением Клапейрона-Менделеева.
 Существует множество уравнений реальных газов, адекватно описывающих их свойства, включая превращение в жидкость. Это уравнения Ван-дер-Ваальса, Дитеричи (16), Бертло (17), Клаузиуса (18). Наиболее популярные в современной научной практике уравнения Редлиха-Квонга, Пенга-Робинсона, Камерлинг-Оннеса, или вириальное уравнение (19).
Существует множество уравнений реальных газов, адекватно описывающих их свойства, включая превращение в жидкость. Это уравнения Ван-дер-Ваальса, Дитеричи (16), Бертло (17), Клаузиуса (18). Наиболее популярные в современной научной практике уравнения Редлиха-Квонга, Пенга-Робинсона, Камерлинг-Оннеса, или вириальное уравнение (19).
|
 , функцией расстояния r между центрами молекул (рис.17).
, функцией расстояния r между центрами молекул (рис.17).
| Уравнения состояния реальных газов |
 - уравнение Дитеричи (16), - уравнение Дитеричи (16),
 - уравнение Бертло (17), - уравнение Бертло (17),
 - уравнение Клаузиуса (18), - уравнение Клаузиуса (18),
 - уравнение Камерлинг-Онесса (19). - уравнение Камерлинг-Онесса (19).
|
Функция имеет минимум, в котором силы притяжения уравновешиваются силами отталкивания. Аналитический вид функции  на полуэмпирической основе представлен ниже:
на полуэмпирической основе представлен ниже:
 - потенциал Леннарда-Джонса (20)
- потенциал Леннарда-Джонса (20)
В теории Ван-дер-Ваальса используется упрощенная модель межмолекулярного взаимодействия, часть кривой  заменяется вертикальной прямой (пунктирная линия на рис.17). Если d – расстояние до этой прямой от начала координат, то центры взаимодействия частиц не могут сблизиться на расстояние, меньшее d, что соответствует модели твердых упругих шаров.
заменяется вертикальной прямой (пунктирная линия на рис.17). Если d – расстояние до этой прямой от начала координат, то центры взаимодействия частиц не могут сблизиться на расстояние, меньшее d, что соответствует модели твердых упругих шаров.
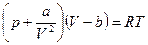 - уравнение Ван-дер-Ваальса (21)
- уравнение Ван-дер-Ваальса (21)
где 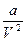 – поправка на давление, т.е. дополнительное «внутреннее» давление за счет взаимного притяжения; b – поправка на объем молекул, учитывающая силы отталкивания.
– поправка на давление, т.е. дополнительное «внутреннее» давление за счет взаимного притяжения; b – поправка на объем молекул, учитывающая силы отталкивания.
 Наиболее содержательные результаты получаются из уравнения Ван-дер-Ваальса путем анализа его изотерм. Если в уравнении (19) принять Т = const, то изотерма этого уравнения в плоскости p, V пересекается прямой линией p = const либо в одной точке, либо в трех точках (рис.18). При некоторой промежуточной температуре Ткр три корня V1, V2, V3 становятся равными.
Наиболее содержательные результаты получаются из уравнения Ван-дер-Ваальса путем анализа его изотерм. Если в уравнении (19) принять Т = const, то изотерма этого уравнения в плоскости p, V пересекается прямой линией p = const либо в одной точке, либо в трех точках (рис.18). При некоторой промежуточной температуре Ткр три корня V1, V2, V3 становятся равными.
Такая температура и соответствующая ей изотерма называются критическими. Критическая изотерма всюду монотонно опускается вниз, за исключением одной точки – критической.
Соответствующие этой точке давление pk, объем Vk и температура Tk также называются критическими.
|








