Общая схема метаболизма глутамата и глутамина:







 ЦТК а КГК а Кетоглутарамат
ЦТК а КГК а Кетоглутарамат
 |  | ||

 а- амино NH3 карбомаил кетокислоты
а- амино NH3 карбомаил кетокислоты


 бутират фосфат
бутират фосфат
аминокислоты










 N-ацетил
N-ацетил

 глутамат Глутамат Глутамин транспорт N2
глутамат Глутамат Глутамин транспорт N2







 ГАМК цис о-про карбомаил
ГАМК цис о-про карбомаил
 ГОМК фосфат
ГОМК фосфат
гамма-глу-амино фенилацетил


 гамма-глу-цис гли кислота глутамин
гамма-глу-цис гли кислота глутамин
 |
гамма-глу-цис-гли аминокислота
 |  | ||

 синтез из ГИС ПРОЛИН
синтез из ГИС ПРОЛИН
Глутаминовая кислота – сильное антитоксическое и антиоксидантное средство. Является центральным компонентом аминокислотного обмена, так как обеспечивает интеграцию белкового обмена с энергетическим (углеводным и липидным). Это осуществляется благодаря реакциям прямого и непрямого дезаминирования:
 ЦТК
ЦТК
 ЩУК аминокислота а КГК NH3 мочевина
ЩУК аминокислота а КГК NH3 мочевина


 АСП кетокислоты ГЛУ
АСП кетокислоты ГЛУ
 кетоновые тела
кетоновые тела
 фумарат глюкоза
фумарат глюкоза
мочевина
Глутамин играет роль антитоксического фактора. Это связано с тем, что при поступлении в клетку большого количества патологического материала, изменяется соотношение НАД и НАД*Н2, начинается конкуренция между субстратами за обладание НАД, в то время как концентрация НАД*Н2, возникает угроза энергетического голода тканей и дыхательная цепь переключается на ФАД-зависимое окисление именно благодаря глутамину, которая идёт на синтез эндогенного сукцинил-КоА.

 ГЛУ ГАМК янтарный полуальдегид сукцинилКоА ФАД-зависимый
ГЛУ ГАМК янтарный полуальдегид сукцинилКоА ФАД-зависимый
COOH вход ДЦ
|
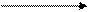 HOOC – CH2 – CH2 – CH – COOH CH2
HOOC – CH2 – CH2 – CH – COOH CH2
| - CO2 |
NH2 CH2
ГЛУ |
CH2 – NH2
ГАМК
 а КГК ГЛУ COOH COOH COOH
а КГК ГЛУ COOH COOH COOH
 . | HSKoA | |
. | HSKoA | |
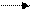

 CH2 CH2 CH2 ФАД (ДЦ)
CH2 CH2 CH2 ФАД (ДЦ)
| | |
CH2 CH2 CH2
| | |
H – C = O O = C – SKoA COOH
Янтарный полуальдегид сукцинилКоА сукцинат
Глутаминовая кислота является одним из немногих соединений в дополнение к глюкозе, которые служат энергетическим материалом для мозга (глутамин составляет 25% пула аминокислот мозга), поэтому в тканях мозга высока активность глутаматдекарбоксилазы:
HOOC – CH2 HOOC COOH COOH
| | | |
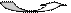 CH2 а -декарбоксили (CH2) а КГК ГЛУ CH2 CH2
CH2 а -декарбоксили (CH2) а КГК ГЛУ CH2 CH2




 | рование | | | ДЦ
| рование | | | ДЦ
CH – NH2 CH2 CH CH2
 | | | | НАД*Н2
| | | | НАД*Н2
COOH NH2 O = C – H COOH
Глутамин ГАМК янтарный полуальдегид
НАД
COOH
|
CH2
|
CH2
|
ГОМК CH2OH
ГАМК и ГОМК – медиаторы торможения. Они оказывают тормозной эффект на синаптическую передачу. В общих реакциях (декарбоксилирование глутамина и трансаминирование ГАМК принимает участие ПФ, поэтому судороги, наблюдаемые при гиповитаминозе В6, связаны со снижением образования ГАМК в глутаматкарбоксилазной реакции.
Антиоксидантная активность глутамина заключается в том, что она входит в состав глутатиона. Поэтому при отравлении тяжёлыми металлами принимают глутамин во внутрь. Но ввиду слабой усвояемости чистого глутамина, его используют в качестве лекарственного препарата в виде солей (калиевой соли глутамина). Глутамин имеет вкус куриного бульона.
Метаболизм аспарагина.
Синтез аспарагина осуществляется реакцией трансаминирования:
COOH COOH COOH COOH
| | | |
CH2 (CH2) АсАТ CH2 (CH2)

 | + | | + |
| + | | + |
C = O CH – NH2 CH – NH2 C = O
| | | |
COOH COOH COOH COOH
ЩУК глутамин аспарагин а КГК
Аспартат утилизируется:
1. В ГНГ (глюкогенная аминокислота)
2. Синтез мочевины
3. Синтез пуринов и пиримидинов
4. Образование в -аланина или а -аланина
COOH CH3 – CH – COOH

 | | COOH анзерин
| | COOH анзерин
CH2 NH2 |
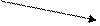
 | CH2
| CH2
CH – NH2 - CO2 | карнозин
| CH2 – NH2
COOH в -аланин
В -аланин входит в состав пантогеновой кислоты, идущей на синтез HS-KoA. Опухолевые ткани не способны воспроизводить аспарагин, поэтому введение аспарагиназы приводит к торможению роста опухоли.
5. Трансаминирование аспарагина даёт ЩУК
 ЩУК сукцинат, который наполняет эндогенный пул янтарной кислоты.
ЩУК сукцинат, который наполняет эндогенный пул янтарной кислоты.
6. Синтез аспарагина. Нужно отметить, что глицин и аспарагин в тканях подвергаются сочетанному трансаминированию и дезаминированию:
O O HOOC – C = O
|| || R |
 R – C – COOH + HOOC – CH – CH2 – C | + CH2
R – C – COOH + HOOC – CH – CH2 – C | + CH2
Кетокислота | | CH – NH2 |
NH2 NH2 | C = O
Аспсрагин COOH |
Аминокислота NH2
а -кетосукцинамовая
кислота
NH2 COOH
| |
C = O CH2
| + HOH | + NH3
 CH2 C = O
CH2 C = O
| СО-оксидаза |
C = O COOH
| ЩУК
COOH
а -кетосукцинамовая кислота
То же самое возможно и с глицином, при этом образуется а -кетоглутарамовая кислота.
7. Аспартат является нейротрансмиттером ЦНС (в виде препарата натриевой соли аспартата применяется для лечения заболеваний сердца).
Метаболизм гистидина.
Известны 3 пути метаболизма гистидина:
1.







 N N
N N
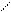
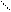
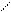




 CH2 – CH – COOH CH2 – CH2 – NH2
CH2 – CH – COOH CH2 – CH2 – NH2
| - CO2
NH NH2 NH гистамин
O

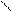






 N + HOH N //
N + HOH N //




 CH2 – CH2 – NH2 NH3 + CH2 – C + H2O2
CH2 – CH2 – NH2 NH3 + CH2 – C + H2O2
NH диаминооксидаза NH \
альдегид гистидина H




 2.
2.
N

 CH2 – CH – COOH + H2N – CH2 – CH2 – COOH
CH2 – CH – COOH + H2N – CH2 – CH2 – COOH
NH | в -аланин - НОН




 гистидин NH2
гистидин NH2


 N N
N N
 CH2 – CH – COOH CH2 – CH – COOH
CH2 – CH – COOH CH2 – CH – COOH




 | |
| |
NH NH N NH
| | |
H2N – CH2 – CH2 – C = O CH3 CO
карнозин |
анзерин (CH2)2 – NH2 Внутреннее дезаминирование:
3. 









 N гистидинаммиаклиаза N
N гистидинаммиаклиаза N





 CH2 – CH – COOH CH = CH – COOH
CH2 – CH – COOH CH = CH – COOH
NH | - NH3 NH
NH2

 имидазолилпропионат ГЛУ
имидазолилпропионат ГЛУ
Метаболизм пролина.
Пролин синтезируется из глутамата:
O
НАДФ*Н2 НАДФ //
 HOOC – CH2 – CH2 – CH – COOH HOOC – CH2 – (CH2) – C
HOOC – CH2 – CH2 – CH – COOH HOOC – CH2 – (CH2) – C
- НОН гамма-полуальдегид \




 H
H


 глутаматдегидрогеназа
глутаматдегидрогеназа





 COOH O = COOH
COOH O = COOH




 - НОН NH пролиноксидаза NH
- НОН NH пролиноксидаза NH
пролин 5-оксопролин
оксипролиназа COOH COOH


 O = COOH | | GSH
O = COOH | | GSH
 NH CH2 – CH2 – CH – NH2
NH CH2 – CH2 – CH – NH2
5-оксопролин АТФ АДФ+Фн глутамат






