Цикл трикарбоновых кислот связан с предшествующими стадиями энергетического обмена (гликолиз, окисление жирных кислот), поэтому механизмы регуляции этих процессов будут справедливы и для цикла Кребса.
Типы регуляции:
1) Ретроингибирование;
2) Путём изменения концентрации субстрата на выходе цикла;
3) Аллостерическая регуляция (с помощью НАД, НАД * Н2, АТФ).
4) Ионная (рН, концентрация Са)
 Так как цикл Кребса начинается со стадии ЩУК + ацетилКоА, то эти метаболиты управляют интенсивностью цикла. Первым регуляторным фактором является концентрация ЩУК, которая в основном образуется из ПВК. ПВК же образуется из углеводов (глюкозы), поэтому при диабете или углеводном голодании наблюдается недостаток ПВК, а значит и ЩУК и сам цикл блокируется. АцетилКоА не является лимитирующим субстратом, так как в основном образуется при окислении жирных кислот. Но в то же время ЩУК – конкурентный ингибитор сукцинатдегидрогеназы, поэтому при избытке ЩУК цикл трикарбоновых кислот блокируется на 6 – ой стадии. Это торможение можно убрать глутамином, который переаминирует ЩУК в аспарагин. Второй регуляторный центр – концентрация НАД и НАД * Н2. В живых системах концентрация НАД и НАД * Н2 = const. Любые факторы, ведущие к увеличению НАД * Н2 (алкогольная интоксикация) и дефекту НАД блокируют цикл Кребса. Следовательно, увеличение концентрации НАД стимулирует цикл трикарбоновых кислот.
Так как цикл Кребса начинается со стадии ЩУК + ацетилКоА, то эти метаболиты управляют интенсивностью цикла. Первым регуляторным фактором является концентрация ЩУК, которая в основном образуется из ПВК. ПВК же образуется из углеводов (глюкозы), поэтому при диабете или углеводном голодании наблюдается недостаток ПВК, а значит и ЩУК и сам цикл блокируется. АцетилКоА не является лимитирующим субстратом, так как в основном образуется при окислении жирных кислот. Но в то же время ЩУК – конкурентный ингибитор сукцинатдегидрогеназы, поэтому при избытке ЩУК цикл трикарбоновых кислот блокируется на 6 – ой стадии. Это торможение можно убрать глутамином, который переаминирует ЩУК в аспарагин. Второй регуляторный центр – концентрация НАД и НАД * Н2. В живых системах концентрация НАД и НАД * Н2 = const. Любые факторы, ведущие к увеличению НАД * Н2 (алкогольная интоксикация) и дефекту НАД блокируют цикл Кребса. Следовательно, увеличение концентрации НАД стимулирует цикл трикарбоновых кислот.
Так как АТФ является косвенно конечным продуктом, то её избыток блокирует реакции, а значит АДФ стимулирует цикл (АДФ рассматривается как аллостерический активатор изоцитратдегидрогеназы). Стимулятором цикла является также и кислород, так как стимулирует работу АТФ. При повышении концентрации Са в клетке активируются дегидрогеназные реакции. Цикл Кребса активируется при сердечной недостаточности. Это объясняется тем, что миокард не может самостоятельно убрать избыток Са и эту роль берут на себя митохондрии, возрастает потребность в кислороде.
ТКАНЕВОЕ ДЫХАНИЕ.
Тканевое дыхание – один из процессов диссимиляции, по сути это есть биологическое окисление в тканях и клетках организма. В организме существует три пути потребления и утилизации кислорода:
1 – й путь: 90 – 95 % кислорода идёт на митохондриальное окисление.
2 – й путь: 5 – 10 % идёт на микросомальное окисление (в печени при поступлении токсинов).
3 – й путь: 2 – 5 % - перекисное окисление.
ДЫХАТЕЛЬНАЯ ЦЕПЬ.
В процессе окисления ацетилКоА в цикле Кребса восстановленные формы НАД * Н2 и ФАД * Н2 поступают в дыхательную цепь, где энергия электрона и протона трансформируется в энергию макроэргических связей АТФ. Дыхательная цепь – это совокупность дегидрогеназ, которые транспортируют электроны и протон с субстрата на кислород. Принцип функционирования дыхательной цепи основан на 1 – ом и 2 – ом законах термодинамики (1 – й закон: закон сохранения энергии; 2 – й закон: все системы стремятся к минимальной энергии).
Дыхательная цепь локализуется во внутренней мембране митохондрий и имеет два пути введения электрона и протона или два входа; дегидрогеназная цепь образует четыре комплекса:
1 – й вход – НАД - зависимый (поступают электрон и протон со всех НАД - зависимых реакций)
2 – й вход – ФАД - зависимый (аналогично)
Кофермент Q или убихинон – это гидрофобное соединение, является компонентом клеточной мембраны (находится на наружной поверхности), содержится в большой концентрации, относится к группе витаминов.
О

 //
//
Н3СО СН3 СН3 СН3



 / /
/ /


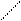
 Н3СО (СН2 – СН = С – СН2)9 – СН2 – СН = С – СН2
Н3СО (СН2 – СН = С – СН2)9 – СН2 – СН = С – СН2
\\
О
КОФЕРМЕНТ Q.
ЦИТОХРОМ.
СН2
//
СН СН3
/ /





 Н3С СН = СН2
Н3С СН = СН2



 N N
N N

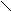

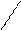


 Fe
Fe







 N N
N N




 Н3С СН3
Н3С СН3
 |
\ \
СН2 СН2 – СН2 – СО2
\
СН2
\
СО2
ЦИТОХРОМ aa3– (цитохромоксидаза)
CH3 CH3 CH3
| | |
СН2 – СН – (СН2) 3 – СН –(СН2) 3 – CH
| |
HO - СН CH3 CH3





 | |
| |



 H3C- - CH = CH2
H3C- - CH = CH2



 N N
N N
 |  |

 Fe
Fe
 |  |










 N N
N N
O = C -
|
H | |
CH2 CH2 – CH2 – CO2
| |
CH2
|
CO2
Цитохромоксидаза имеет высокую степень сродства к О2 и может работать при его низких концентрациях. аа3 состоит из шести субъедениц, каждая из которых содержит гем и атом Cu. Две субъеденицы составляют цитохром а, а остальные четыре относятся к цитохрому а3.
Дыхательная цепь активно реагирует на чрезмерные нагрузки, яды. Так, например, барбитураты ингибируют перенос электрона и протона в первый комплекс дыхательной цепи, в ответ на это возникает энергетический голод ткани. Это происходит потому, что возникает недогрузка дыхательной цепи протонами и электронами. В результате снижается синтез АТФ и в ткани активируется производство и окисление эндогенной янтарной кислоты. Такое же действие оказывает и алкоголь, так как этанол является НАД – зависимым субстратом. Этанол монополизирует основной фонд НАД и превращает его в НАД * Н2. Дыхательная цепь перегружается НАД * Н2 и ткань не получает энергии за счёт окисления естественных субстратов. Такие яды, как цианиды, СО, Н2S, блокируют четвёртый комплекс дыхательной цепи. Если ингибирование первого комплекса приводит к активации трёх оставшихся и за счёт этого дыхательная цепь компенсируется, то при блокировании четвёртого комплекса работа дыхательной цепи не состоится, что приводит к смерти. Четыре комплекса, входящие в состав дыхательной цепи, неравноценны: в 1,3 и 4 происходит синтез АТФ (АДФ + Фн).
Работа всей дыхательной цепи состоит из двух составляющих: 1) образование АТФ (50% энергии депонируется в виде АТФ); 2) рассеивание остальных 50 % энергии в виде тепла.
Для оценки эффективности работы дыхательной цепи и окислительного фосфорилирования в 1939 году введён коэффициент Р / О –показатель степени спряжения фосфорилирования и дыхания. Р / О – отношение количества поглощённых молекул фосфата (в процессе АДФ + Фн) к количеству поглощённого кислорода. Так, если окисляются НАД – зависимые субстраты, то электроны в этом случае проходят все три стадии фосфорилирования и на образование АТФ уходят три молекулы Фн и один атом О2, поэтому Р / О = 3. Если окисляются ФАД – зависимые субстраты, то электроны проходят только две стадии фосфорилирования и тратится две молекулы Фн на атом О2, поэтому Р / О = 2. При окислении витамина С и адреналина, электроны поставляются прямо на цитохром с, поэтому они проходят только одну стадию фосфорилирования и поэтому Р / О = 1.
В ряде случаев некоторые пункты фосфорилирования могут «выключаться» - такое состояние называется разобщением окислительного фосфорилирования. В этом случае Р / О снижается: для
НАД – зависимых субстратов – ниже трёх, для ФАД – зависимых субстратов – ниже двух.
Исходя из первого закона термодинамики, в разобщённых митохондриях увеличивается теплообразование. Это происходит за счёт того, что та энергия электронов, которая должна была быть использована для синтеза АТФ в «выключенной» стадии фосфорилирования, рассеивается в виде тепла. Процесс разобщения окислительного фосфорилирования лежит в основе лихорадки, вызванной бактериями, вирусами и другими агентами. Разобщение резко увеличивается при охлаждении организма. Работа митохондрий при всех «выключенных» стадиях фосфорилирования называется сопряжённой, в противном, выше описанном случае, разобщённой и дыхание при этом называется свободным. В качестве разобщителей окислительного фосфорилирования выступают слабые гидрофобные кислоты (жирные кислоты), тироидные гормоны, лекарства.
Дыхательная цепь имеет механизм шунтирования: сброс электрона и протона с НАД на цитохромы или с НАД на межмембранные дегидрогеназы, не нарушая мембрану и гладкую эндоплазматическую сеть. Такой перенос характерен для печени. При воздействии какого – либо блокатора, возникает блок в первом комплексе дыхательной цепи. Происходит накопление НАД * Н2, и становится реальной угроза гипоксии и печень может погибнуть. Чтобы этого не произошло, происходит сброс НАД * Н2 с митохондриальной дыхательной цепи на микросомальную.






