При работе с патологическим материалом, содержащим микробы, и особенно при культивировании патогенных микробов во избежание заражения персонала лаборатории необходимо соблюдать правила техники биологической безопасности. В зависимости от степени патогенности и контагиозности возбудителей принято выделять четыре уровня биологической опасности и соответствующих мероприятий, необходимых для предупреждения заражения в лаборатории.
Первый уровень (работа с непатогенными микроорганизмами). Необходимо соблюдение стандартных правил (см. тему 1.1).
Второй уровень (работа с низковирулентными микроорганизмами). К числу дополнительных правил и мероприятий относятся использование лабораторной одежды и защитных перчаток; обязательное обеззараживание всех загрязненных отходов; ограничение доступа в лабораторию. Для предотвращения попадания микробов в воздух рабочего помещения выполнение механических манипуляций, сопряженных с высокой вероятностью распыления микроорганизмов, необходимо осуществлять в специализированных закрытых легкодезинфици-руемых настольных боксах.
Третий уровень (работа с высоковирулентными микроорганизмами). К числу дополнительных правил и мероприятий относятся использование специальной защитной лабораторной одежды; контроль доступа в лабораторию. Все манипуляции с патологическим материалом необходимо осуществлять в специализированных боксах.
Четвертый уровень (работа с возбудителями ООИ). Работа с возбудителями особо опасных инфекций (ООИ) разрешена исключительно в специализированных режимных лабораториях,

 имеющих оборудование, необходимое для эффективной защиты от патогенных микробов, их контроля и уничтожения. К числу дополнительных правил и мероприятий относятся наличие отдельных помещений для смены лабораторной одежды и душевых, обязательное обеззараживание всех отходов лаборатории. Все манипуляции с патологическим материалом необходимо осуществлять в специализированных настольных боксах, снабженных системами стерилизации воздуха (см. тему 7.1).
имеющих оборудование, необходимое для эффективной защиты от патогенных микробов, их контроля и уничтожения. К числу дополнительных правил и мероприятий относятся наличие отдельных помещений для смены лабораторной одежды и душевых, обязательное обеззараживание всех отходов лаборатории. Все манипуляции с патологическим материалом необходимо осуществлять в специализированных настольных боксах, снабженных системами стерилизации воздуха (см. тему 7.1).
■ ОЦЕНКА РЕЗУЛЬТАТОВ КЛИНИКО-ДИАГНОСТИЧЕСКИХ МИКРОБИОЛОГИЧЕСКИХ ИССЛЕДОВАНИЙ
Обнаружение патогенных микроорганизмов, являющихся возбудителями заболеваний (например, микобактерии туберкулеза, гонококки и др.), имеет решающее значение для постановки диагноза.
Выявление роли условно-патогенных микроорганизмов в этиологии и патогенезе заболеваний должно быть основано на строгой аргументации. Обязательным условием является клиническое, эпидемиологическое, микробиологическое и серологическое исключение возбудителей инфекционных болезней (например, возбудителей кишечных инфекций, венерических болезней и др.). Для оценки роли условно-патогенных микроорганизмов в патологии могут быть использованы следующие критерии.
1. Выделение микроорганизмов из крови, спинномозговой жидкости или других жидкостей организма, которые в норме у здоровых людей являются стерильными.
2. Обнаружение в исследуемом материале, особенно при дисбактериозах, условно-патогенных микроорганизмов в достаточно больших количествах (например, 105—107 микробных клеток в 1 мл). Для этого проводят количественное определение микроорганизмов по числу КОЕ в 1 г или 1 мл испытуемого образца. Эти количественные показатели могут варьировать в зависимости от вида микроорганизмов, типа исследуемого материала, характера и стадии заболевания.
3. Повторное, многократное (в течение суток или через сутки) выделение одного и того же микроорганизма из одного и того же материала от больного (например, из крови при сепсисе и т.д.).
4. Обнаружение идентичных условно-патогенных микроорганизмов в разных образцах материала (например, при пищевых токсикоинфекциях — в промывных водах желудка, рвотных массах, испражнениях, пищевых продуктах).
5. Нарастание титра антител в 4 раза и более в парных сыворотках крови больного в отношении условно-патогенного микроорганизма, который предполагается как возбудитель дан-
ного патологического процесса. В ряде случаев рекомендуется использовать в качестве антигенов аутоштаммы микроорганизмов, выделенные от больных.
6. Положительные кожно-аллергические реакции у больных с аллергенами, приготовленными из условно-патогенных микроорганизмов.
7. В случае внутрибольничных (нозокомиальных) инфекций — выделение идентичных культур микроорганизмов от группы больных.
8. Совпадение данных лабораторного определения чувствительности микроорганизмов к антибиотикам с эффективностью антимикробной терапии в клинических условиях, подтверждаемое улучшением состояния больного и уменьшением количества или элиминацией соответствующих микроорганизмов.
9. Условно-патогенные микроорганизмы (синоним: оппортунистические) представляют собой большую группу микроорганизмов, занимающих различное систематическое положение. Они встречаются среди аэробных и анаэробных бактерий, грибов, простейших. В клинической микробиологии наиболее часто встречаются условно-патогенные микроорганизмы, относящиеся к родам Staphylococcus, Streptococcus, Escherichia, Klebsiella, Proteus, Entewbacter, Citrobacter, Serratia, Pseudomonas, Haemophilus, Bacteroides, Veillonella, Vibrio, Peptococcus, Peptostreptococ-cus, Mycobacterium, Mycoplasma, Candida и др.
■ ОФОРМЛЕНИЕ РЕЗУЛЬТАТОВ ЛАБОРАТОРНЫХ МИКРОБИОЛОГИЧЕСКИХ ИССЛЕДОВАНИЙ
Результаты лабораторных исследований оформляют на специальных бланках, которые передают лечащему врачу.
1. В ответе прежде всего указывают наличие патогенных, а также условно-патогенных микроорганизмов, обнаруженных при микробиологическом исследовании. Сообщают также данные лабораторного определения чувствительности микроорганизмов к антибиотикам.
2. При обнаружении микробных ассоциаций перечисляют все микроорганизмы, указывают доминирующие виды и количественные микробиологические показатели.
3. В соответствии с правилами международной номенклатуры в ответах приводят видовые названия микроорганизмов, например: Staphylococcus aureus, Pseudomonas aeruginosa и т.д.
4. С целью ускорения лабораторных исследований в ряде случаев при выделении условно-патогенных микроорганизмов вполне допустимо в ответе ограничиться указанием только родовой принадлежности обнаруженных микроорганизмов, например Proteus sp., Candida sp. и т.д.
 | |||
 |
| ВОЗБУДИТЕЛИ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ И РАНЕВЫХ ИНФЕКЦИЙ |
| Глава 12 |
| Раневые и гнойные инфекции часто встречаются в хирургической, акушерско-гинекологической, терапевтической, педиатрической практике, а также других отраслях медицины. Нередко они носят характер внутрибольничной (госпитальной) инфекции. Возбудителями раневой и гнойной инфекции являются бактерии, которые относятся к разным семействам, родам и видам. Среди них известны аэробные и анаэробные, грам-положительные и грамотрицательные бактерии. БАКТЕРИИ - ВОЗБУДИТЕЛИ РАНЕВОЙ И ГНОЙНОЙ ИНФЕКЦИИ |
Аэробные бактерии Грамположительные бактерии
Chryseobacterium indologenes Chryseobacterium meningosepticum Enterococcus faecalis и другие виды Enterococcus Erysipelothrix rhusiopathiae Staphylococcus aureus Staphylococcus epidermidis Staphylococcus saprophiticus и другие виды Staphylococcus Streptococcus pyogenes Streptococcus agalactiae
Грамотрицательные бактерии
Burkholderia cepacia Citrobacter koseri Edwardsiella tarda Eikenella corrodens Enterobacter spp. Escherichia coli Haemophilus influenzae Klebsiella spp. Listeria monocytogenes Moraxella catarrhalis Proteus vulgaris Proteus mirabilis Pseudomonas aeruginosa Pseudomonas putida Pseudomonas fluorescens Salmonella enterica
подвид enterica биовар typhimurium Serratia spp. Spirillum minus Streptobacillus moniliformis Vibrio vulnificus
Анаэробные бактерии
Неспорообразующие грамотрицательные анаэробы
Bacteroides fragilis
и другие виды рода Bacteroides
Prevotella melaninogenica
и другие виды рода Prevotella
Porphiromonas spp.
Fusobacterium spp.
Veilonella spp.
Неспорообразующие грамположительные анаэробы
Peptostreptococcus spp. Propionibacterium acnes
Спорообразующие грамположительные анаэробы
Clostridium perfringens Clostridium novyi Clostridium septicum Clostridium histolyticum Clostridium ramosum Clostridium sporogenes Clostridium tetani
Бактерии, перечисленные выше, вызывают гнойно-воспалительные процессы различной локализации, в том числе ангины, фурункулы, циститы и пиелиты, плевриты, перикардиты, сепсис и др. Многие из этих возбудителей встречаются в нормальной микрофлоре человека и проявляют свою патогенность только при нарушении нормальной экологии.
Стафилококки, стрептококки, протей, эшерихии и анаэробные бактерии нередко вызывают смешанную инфекцию как в разнообразных сочетаниях между собой, так и с другими микроорганизмами — вирусами, грибами.
Тема 12.1. АЭРОБНЫЕ БАКТЕРИИ -ВОЗБУДИТЕЛИ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ И РАНЕВЫХ ИНФЕКЦИЙ
▲ План
▲ Программа
1. Биологические свойства возбудителей гнойно-воспалительной и раневой инфекции, их патогенность, экология, особенности инфекции и эпидемиология вызываемых заболеваний.
2. Микробиологическая диагностика.
3. Диагностические препараты, профилактические и лечебные препараты.
А Демонстрация
1. Рост а- и р-гемолитических стрептококков на кровяном агаре.
2. Рост и образование пигмента P.aeruginosa на агаре.
3. Диагностические и лечебно-профилактические препараты.
ЗАНЯТИЕ 1
▲ Задание студентам
1. Микроскопировать и зарисовать мазки из чистых культур возбудителей гнойных инфекций: S.aureus, S.pyogenes, P.aeruginosa, E.coli, P.vulgaris. Окраска по методу Грама.
2. Микроскопировать и зарисовать мазки из гноя, содержащие возбудителей: стафилококков, стрептококков. Окраска по методу Грама.
3. Ознакомиться с питательными средами, применяемыми при микробиологической диагностике гнойных и раневых инфекций. Указать назначение отдельных питательных сред.
4. Микробиологическое исследование при раневых и гнойных инфекциях:
а) указать материал, подлежащий исследованию;

|

|
б) микроскопический метод: микроскопировать мазок
из гноя, окраска по методу Грама. Сделать вывод;
в) наметить план дальнейшего исследования.
ЗАНЯТИЕ 2
Задание студентам
1. Микробиологическое исследование гноя:
а) учесть результат посева гноя на кровяной агар в
чашке Петри, описать подозрительные колонии,
отметить наличие гемолиза, составить план даль
нейшего исследования;
б) учесть результаты определения лецитиназы и плаз-
мокоагулазы у выделенной культуры стафилококка.
Сделать вывод;
в) учесть результаты определения чувствительности
культуры стафилококка к антибиотикам. Сделать
вывод.
2. Микробиологическое исследование мочи. Определить количество бактерий в 1 мл мочи по результатам метода секторных посевов. Дать заключение.
3. Серодиагностика ревматизма. Ознакомиться с описанием стрептолизиновой реакции. Внести в протокол результаты определения анти-О-стрептолизина в сыворотке крови больного. Сделать вывод.
4. Дать краткую характеристику демонстрируемым антимикробным, диагностическим и лечебно-профилактическим препаратам.
Методические указания
Материал для исследования: раневое отделяемое, гной, экссудат, моча, мазки со слизистых оболочек (носоглотки, зева и др.), кровь при подозрении на сепсис.
• Микробиологическая диагностика стафилококковых инфекций МЕТОДЫ ДИАГНОСТИКИ:
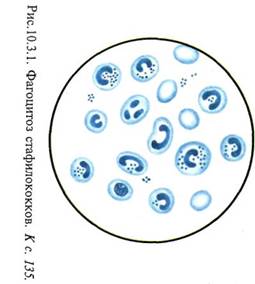
Бактериоскопическое исследование (схема 12.1.1). Из исследуемого материала (за исключением крови) готовят мазки для первичной бактериоскопии, окрашивают по методу Грама и микроскопируют. Наличие в препаратах грамположительных кокков, располагающихся в виде гроздевидных скоплений (рис. 12.1.1; на вклейке), позволяет поставить предварительный диагноз стафилококковой инфекции. Следует иметь в виду, что в патологическом материале стрептококки редко образуют типичные скопления, чаще располагаются поодиночке или небольшими группами по 2—3 бактерии.
Бактериологическое исследование. Испытуемый материал засевают петлей на чашки с кровяным и желточно-солевым агаром
Рис. 1.4. Культура дрожжей Sac--charomyces cerevisiae при разных методах микроскопии К с. 14. а — микроскопия мазка, окрашенного метиленовым синим; б - тем-нопольная микроскопия; в — фазо-во-контрастная микроскопия- г — люминесцентная микроскопия. Окраска корифосфином.
Рис.2.2.1. Смесь стафилококков и кишечных палочек. К с. 23. Окраска по методу Грама.
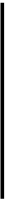 |

|
|
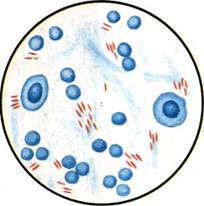
Рис.2.2.2. Возбудитель туберкулеза (Mycobacterium tuberculosis)
в мокроте. К с. 25. Окраска по методу Циля—Нильсена.
Рис.2.2.4. Возбудитель дифтерии (Corynebacterium diphtheriae). К с. 26.
Окраска по методу Нейссера. Видны зерна волютина.

|

|
Рис.2.2.3. Споры и вегетативные
клетки возбудителя сибирской
язвы (Bacillus anthracis). К с. 25.
Окраска по методу Ожешко.
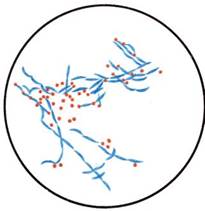
Рис.2.2.5. Капсула Klebsiellae pneumoniae. К с. 26. Окраска по методу Бурри—Гинса.
 |

|

|
Рис.3.2.1. "Пестрый ряд". К с. 46.
а — ферментация углевода до кислоты и газа; б — отсутствие ферментации;
в — образование индола; г — образование сероводорода.

Рис.6.2. Постановка опыта специфической трансдукции (схема).Я' с. 26
пп™ЬГ i dga'; б ~ реципиент E-coli 1ас"; в - Рост колоний реципиентного „» р п Т^- ВДо; г *" ^Раженная транслирующим фагом X dgal культура b.coli lac; д - рост колоний трансдуктантов (красного цвета), несущих ген gal, на среде Эндо.
Рис.6.1. Постановка опыта трансформации. К с. 68. контаетСпе?™г5НК' в™еленно? из B.subtilis; б - реципиент B.subtilis; в -
селенной с^ЛЫХ ба,СГерИЙ С ДНК; Г ~ рост колоний Рекомбинантов на штамма н L?™ сойС1Рептоми«ином; д - отсутствие роста реципиентного 1мма на селективной среде со стрептомицином; е - рост колоний реципиентного штамма на среде без стрептомицина.

|
Рис.6.3. Постановка опыта по конъюгации. К с. 70. а — рост колоний бактерий донора на минимальной среде без стрептомицина; б — рост колоний рекомбинантов на селективной среде со стрептомицином без лейцина; в — рост колоний бактерий реципиентов на полной среде со стрептомицином и лейцином; г — отсутствие роста бактерий донора на среде со стрептомицином; д — донор-культура E.coli F, lei, su5; е — контакт между бактериями донора и реципиента; ж — реципиент-культура E.coli F", lei", st/; з — отсутствие роста бактерий реципиента на селективной среде со стрептомицином без лейцина.
|

|
 |

|

|
Рис. 10.4.1. Кожно-аллергическая проба. К с. 144.
Рис. 12.1.2. Колонии стафилококка на кровяном агаре. А'с. 162.
 |

|

|
Рис. 12.1.1. Staphylococcus aureus и Streptococcus pyogenes в гное. Окраска по методу Грама. К с. 160.
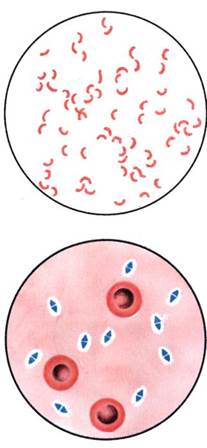
Рис. 12.2.1. Clostridium perfringens в отечной жидкости. К с. 174.


|
|

|
Рис. 13.2.1. Рост бактерий семейства Enterobacteriaceae на дифференциально-диагностических
средах. К с. 194. а — колонии Escherichia coli и Salmonella typhi на среде Эндо; б — колонии Salmonella typhi на висмут-сульфитном агаре.
Рис. 13.3.1. Vibrio cholerae. К с. 203 Окраска по методу Грама.
Рис. 14.1.1. Streptococcus pneumoniae в мокроте. К с. 214.


|

|
Рис. 14.2.1. Рост Corynebacteri-
um diphtheriae на кровяно-тел-
луритовой среде. К с. 231.
Рис. 14.3.2. Микрокультура Mycobacterium tuberculosis. К с. 240. Окраска по методу Циля — Нильсена.
 |

|

|
Рис. 14.3.1. Рост Mycobacterium
tuberculosis на среде Левенштей-
на — Йенсена. К с. 239.
Рис. 15.2.1. N. gonorrhoeae в гное
из мочеиспускательного канала.
К с. 253.
Окраска фуксином.


|

|
Рис. 16.1.1. Yersinia pestis в гное
из бубона. К с. 261.
Окраска метиленовым синим.
 Рис.16.1.3. Brucella melitensis (чистая культура). К с. 266.
Рис.16.1.3. Brucella melitensis (чистая культура). К с. 266.
Рис. 16.1.4. Bacillus anthracis (мазок из гноя). К с. 269.
 |

|

|
Рис. 16.1.2. Francisella tularensis
(чистая культура). К с. 263.
Окраска по методу Грама.
Рис. 17.1.1. Borrelia recurrentis в
крови больного. К с. 283.
Окраска по методу Романовского -
Гимзы.
 | ||
 |

|

Рис. 18.1.1. Титрование вируса гриппа в РТГА с куриными эритроцитами. К с. 292. Объяснение в тексте.

|
Рис.19.1.1. Тельца Бабеша —Нег-ри в нейронах гиппокампа. Срез головного мозга человека. К с. 305. Окраска по методу Романовского — Гимзы.
(ЖСА) для получения изолированных колоний. Посевы инкубируют при 37 °С в течение суток. На следующий день исследуют выросшие колонии на обеих средах. На кровяном агаре отмечают наличие или отсутствие гемолиза (рис. 12.1.2; на вклейке). На ЖСА S.aureus образует золотистые круглые выпуклые непрозрачные колонии. Вокруг колоний стафилококков, обладающих ле-цитиназной активностью, образуются зоны помутнения с перламутровым оттенком. Для окончательного установления вида стафилококка 2—3 колонии пересевают в пробирки со скошенным питательным агаром для получения чистых культур с последующим определением их дифференциальных признаков (табл. 12.1.1).
Таблица 12.1.1. Дифференциальные признаки стафилококков
| Вид |
| S.aureus |
| S.sapro-phyticus |
Признак
S.epider-midis
Образование:
плазмокоагулазы + — —
лецитиназы + — —
альфа-токсина + — —
Ферментация:
глюкозы + + —
маннита в анаэробных условиях + — +
Чувствительность к новобиоцину S S R
Условные обозначения:(+) — наличие признака; (—) — отсутствие признака; S — чувствительный; R — резистентный.
Для постановки реакции на плазмокоагулазу плазму крови, разведенную в 2 раза, разливают по 0,4 мл в пробирки, вносят туда по одной петле каждой исследуемой культуры стафилококка и помещают в термостат при 37 °С. Через 2, 4 и 24 ч отмечают результаты опыта. При наличии плазмокоагулазы образуется сгусток. В некоторых случаях наряду с плазмокоагу-лазой и лецитиназой определяют фибринолизин, гиалуронидазу, ДНКазу.
Для установления источника внутрибольничной инфекции выделяют чистые культуры стафилококка от больных и бактерионосителей, после чего проводят их фаготипирование с помощью набора типовых бактериофагов. Фаги разводят до титра, указанного на этикетке. Каждую из исследуемых культур засевают на питательный агар в чашку Петри газоном, высушивают, а затем петлей каплю соответствующего фага наносят на квадраты (по числу фагов, входящих в набор), предварительно размеченные карандашом на дне чашки Петри. Посевы инкубируют при 37 "С. Результаты оценивают на следующий день по наличию лизиса культуры (см. рис. 5.3.2).
Определение чувствительности стафилококка к антибиотикам — см. тему 7.2.
Экспресс-методы диагностики: иммунохимические, биохимические и молекулярно-биологические исследования.
Иммунохимические исследования. Основаны на обнаружении антигенов (токсинов и ферментов) возбудителя в материале от больного с помощью чувствительных серологических реакций.
Биохимические и молекулярно-биологические исследования. Исследуемый материал, полученный из очага инфекции, используют для обнаружения ДНК возбудителя с помощью ПЦР. В случае обнаружения соответствующих молекул можно поставить предварительный диагноз.
• Микробиологическая диагностика стрептококковых инфекций (схема 12.1.2)
МЕТОДЫ ДИАГНОСТИКИ:
Бактериоскопическое исследование. Мазки для первичной бактериоскопии готовят из патологического материала (за исключением крови), окрашивают по методу Грама и микроско-пируют. При положительном результате обнаруживают цепочки грамположительных кокков (см. рис. 12.1.1). Следует иметь в виду, что в патологическом материале стрептококки редко образуют типичные скопления, чаще располагаются поодиночке или небольшими группами по 2—3 бактерии.
Бактериологическое исследование. Исследуемый материал засевают на кровяной агар в чашку Петри. После инкубации при 37 "С в течение 24 ч отмечают характер колоний и наличие вокруг них зон гемолиза. Из части материала, взятого из колоний, готовят мазок, окрашивают по методу Грама и микро-скопируют. Для получения чистой культуры 1—3 подозрительные колонии пересевают в пробирки со скошенным кровяным агаром и сахарным бульоном. На кровяном агаре Streptococcus pyogenes образует мелкие, величиной с булавочную головку, мутноватые круглые колонии. В бульоне стрептококк в отличие от стафилококка дает придонно-пристеночный рост в виде хлопьев или зерен, оставляя среду прозрачной.
По характеру гемолиза на кровяном агаре стрептококки делятся на три группы: 1) негемолитические; 2) aj-гемолитические, или зеленящие, образующие зеленоватую зону частичного гемолиза; 3) р-гемолитические, образующие вокруг колонии полностью прозрачную зону гемолиза.
Заключительным этапом бактериологического исследования является идентификация выделенной культуры по антигенным свойствам (табл. 12.1.2). Серогруппу стрептококков определяют в реакции преципитации с экстрактом из исследуемой культуры (полисахаридным преципитиногеном С) и группоспецифи-


|
ческими сыворотками (обычно 4 наиболее распространенные серогруппы — А, В, С и D). Развернутое серологическое исследование и типирование стрептококков проводят главным образом для эпидемиологического обследования.
Таблица 12.1.2. Дифференциальные признаки стрептококков
| Вид | Рост при | Рост на средах, содержащих | желчь (40%) | ||
| 10'С | 45 °С | метиленовый синий (0,1 %) | хлорид натрия (6,5 %) | ||
S.pyogenes — — — — —
S.pneumoniae — + ± — —
S.sanguis — ± — — +
S.salivarius — + — — —
| Вид | Рост при рН 9,6 | Термоустойчивость при 60 °С в течение 30 мин | Образование растворимого гемолизина | Антигенная группа (серо-группа) | |
| О | S | ||||
S.pyogenes — — + + А
S.pneumoniae — — + — —
S.sanguis ± H(—)
S.salivarius — — — — —(К)
Условные обозначения: (+) — наличие признака; (—) — отсутствие признака; (+) — наличие признака у одних штаммов и отсутствие его у других штаммов данного вида.






