Существует несколько систем классификации комплексных соединений, которые основываются на различных принципах.
1. По знаку заряда комплекса:
1. Катионные комплексы образованы в результате координации вокруг положительного иона нейтральных молекул (H2O, NH3 и др.).
[Zn(NH3)4]Cl2 - хлорид тетраамминцинка (II)
[Co(NH3)6]Cl2 - хлорид гексаамминкобальта (II)
2. Анионные комплексы: в роли комплексообразователя выступает атом с положительной степенью окисления, а лигандами являются простые или сложные анионы.
K2[BeF4] – тетрафторобериллат (II) калия
Li[AlH4] – тетрадигдроалюминат (III) лития
K3[Fe(CN)6] – гексацианоферрат (III) калия
3. Нейтральные комплексы образуются при координации молекул вокруг нейтрального атома, а также при одновременной координации вокруг положительного иона - комплексообразователя отрицательных ионов и молекул.
[Ni(CO)4] – тетракарбонилникель
[Pt(NH3)2Cl2] – дихлородиамминплатина (II)
Комплексное соединение [Pt(NH3)2Cl2] внешней сферы не имеет и заряд комплекса равен 0.
2. По принадлежности комплексного соединения к определенному классу соединений:

Есть и вещества, не диссоциирующие на ионы, т.е. неэлектролиты
3. По природе лиганда:
- аквакомплексы (лигандом выступает вода: [Co(H2O)6]Cl2, [Al(H2O)6]Cl3 и др.),
- аммиакаты (лигандом выступает аммиак, например: [Cu(NH3)4]SO4, [Co(NH3)6]Cl3, [Pt(NH3)6]Cl4 и др.),
- ацидокомплексы (анионы - кислоты). К ним относятся комплексные соли: K2[PtCl4], комплексные кислоты: H2[CoCl4], H2[SiF6].
- гидроксокомплексы (ОН), например: Na2[Zn(OH)4], Na2[Sn(OH)6] и др.
- карбонилы - комплексные соединения, в которых лигандами являются молекулы оксида углерода (II): [Fe(CO)5], [Ni(CO)4].
- комплексы с макроциклическими лигандами, внутри которых размещается центральный атом (хлорофилл, гемоглобин, цианокобаламин).
4. По внутренней структуре комплекса:
- моноядерны е – если комплекс содержит только один атом металла --комплексообразователя (пример, PdCl4 – имеет один атом палладия);
- многоядерные или полиядерные – если он содержит два или более атомов металла (комплекс платины [Pt2(NH3)2Cl4] – содержащий два атома платины.
| Если полиядерные комплексы содержат атомы металла одинаковой химической природы, то они называются гомометаллическими: | 
|
| Если же в полиядерном комплексе имеются атомы металла-комплексообразователя разной химической природы, то такие комплексы называются гетерометаллическими. Так, из двух биядерных комплексов: | 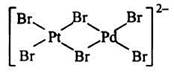
|
Для комплексных соединений, содержащих во внутренней сфере различные лиганды, характерна геометрическая изомерия, когда при одинаковом составе внутренней сферы лиганды в ней располагаются по-разному относительно друг друга.


Геометрические изомеры комплексных соединений отличаются не только по физическим и химическим свойствам, но и биологической активностью. Цис-изомер Pt(NH3)2Cl2 имеет ярко выраженную противоопухолевую активность, а транс-изомер – нет.






