Роль фактора EF1 і гідролізу GTP. Щоб аа-тРНК могла потрапити до рибосоми, рибосома має опинитися в певному – відкритому структурному стані з розширеним каналом між субодиницями з боку стебла L7/12 (див. рис. 9). Крім того, така відкрита форма рибосоми не допускає дуже міцної взаємодії з аа-тРНК, тобто сприяє її легкій дисоціації в разі невідповідності між кодоном і антикодоном. Однак зрозуміло, що відкрита форма рибосоми із частково порушеними контактами (енергетично вигідними взаємодіями) між субодиницями має характеризуватися підвищеною вільною енергією, тобто є малоймовірною. Інший важливий аспект полягає в тому, що на етапі первинного перебору аа-тРНК з різними антикодонами необхідно повністю виключити для акцепторної частини тРНК можливість випадково потрапити до пептидил-трансферазного центру. Узагалі, для такого великого ліганду, як тРНК, існує кінетичний бар’єр асоціації / дисоціації: велика кількість контактів з лігандом вимагає утворювати / руйнувати їх одночасно – проміжні стани з лімітованим набором контактів мають забезпечити прискорення обох процесів. Роль EF1 саме й полягає у вирішенні зазначених проблем:
• Взаємодія EF1 з акцепторною частиною аа-тРНК залишає тільки антикодонову частину вільною для взаємодій з рибосомою (і зв’язаною з нею мРНК).
• При зв’язуванні потрійного комплексу, EF1 (який при цьому зв’язаний з акцепторною частиною аа-тРНК) взаємодіє із сайтом у основі стебла L7/12, що виключає контакт акцепторного стебла тРНК з пептидил-трансферазним центром.
• EF1·GTP має підвищену спорідненість до відкритої форми рибосоми, тобто подібно до того, як GTP перемикає конформацію самого EF1, потрійний комплекс EF1·GTP-аа-тРНК фіксує відкриту форму рибосоми, яка стає енергетично вигідною за рахунок енергії взаємодій з EF1 (рис. 18).
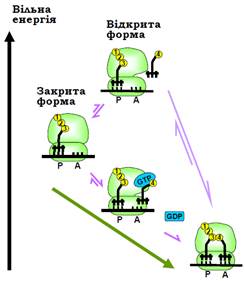
Рис. 18. Зв’язування з А-сайтом рибосоми аа-тРНК у вільному стані та в комплексі з EF1·GTP. Різні стани системи розміщені на різних рівнях відповідно до їхньої вільної енергії. Зелена стрілка вказує оптимальний шлях процесу. Показано тільки два сайти тРНК.
Отже, за умови присутності EF1·GTP здійснюється швидка й недуже міцна взаємодія аа-тРНК з рибосомою (головним чином завдяки взаємодії EF1 з основою стебла L7/12), яка також швидко змінюється дисоціацією: випробування, під час яких антикодонова частина тРНК намагається впізнати кодон. Якщо таке впізнання відбувається (див. нижче), спрацьовує GTP-азна активність EF1 – після гідролізу GTP-фактор дисоціює, що дозволяє акцепторній частині аа-тРНК остаточно розміститися в А-сайті.
Зв’язування аа-тРНК є внутрішньою властивістю рибосоми: in vitro зв’язування може відбуватися без участі будь-яких факторів, оскільки супроводжується зниженням вільної енергії. Проте позафакторне зв’язування є досить повільним через наявність на його шляху енергетичного бар’єра – високоенергетичного відкритого стану рибосоми (рис. 18). Таким чином, EF1 не зумовлює зв’язування аа-тРНК, а тільки суттєво прискорює цей процес. Можна сказати, що EF1 здійснює каталіз конформаційних перетворень рибосоми за рахунок спорідненості до проміжного інтермедіатного стану.
Щодо гідролізу GTP, то він потрібен лише для заміни ліганду з метою позбавитися цієї спорідненості й забезпечити дисоціацію EF1 і повернення рибосоми до закритого стану, необхідного для наступної стадії елонгаційного циклу. Але це має відбутися лише за умови впізнання кодона антикодоном аа-тРНК.
Упізнання кодона. Коли під час первинного зв’язування після кількох випробувань у межах А-сайта на маленькій субодиниці опиняється нарешті комплементарний антикодон, між ним і кодоном має утворитися коротка подвійна спіраль. Оскільки вона коротка (три пари основ), то досить нестабільна: кодон-антикодонова взаємодія за межами рибосоми є неефективною. При цьому рибосома (передусім маленька субодиниця) не тільки створює особливе середовище, яке стабілізує кодон-антикодонову спіраль, але й сприяє підвищенню специфічності – ефективно дискримінує споріднені та неспоріднені до даного кодону антикодони. При утворенні комплементарної подвійної спіралі, з її маленьким жолобком взаємодіють два консервативні аденозини рРНК 16S (з порядковими номерами 1492 і 1493 – розташовані у верхній частині спіралі 44, див рис. 13), утворюючи водневі зв’язки з 2′ОН-групами рибоз нуклеотидів кодона й антикодона (рис. 19). Така взаємодія, що реалізується лише за умови комплементарності, стабілізує перші дві (відносно позицій кодона) нуклеотидні пари. Друга нуклеотидна пара додатково стабілізується, також через маленький жолобок, взаємодією з консервативним G530 рРНК 16S. Третя пара кодон-антикодонової спіралі теж взаємодіє з певним цитидином рРНК 16S, але ця взаємодія менш специфічна й допускає неоднозначність спарювання (див. підрозділ, де йдеться про тРНК).
Взаємодії нуклеотидів рРНК 16S із кодон-антикодоновою спіраллю не тільки підвищують специфічність упізнання кодона, але й мають інший важливий наслідок. Як показано на рис. 19, для реалізаціїцих взаємодій А1492 і А1493 мають бути переорієнтованими відносно сусідніх нуклеотидів. Така локальна конформаційна перебудова запускає каскад конформаційних змін в інших частинах рРНК 16S за принципом доміно, що спричиняє глобальну конформаційну перебудову всієї маленької субодиниці. Зокрема, головка субодиниці переміщується в бік великої субодиниці (див. рис. 9), міцно замикаючи антикодонову частину аа-тРНК на кодоні мРНК. Оскільки субодиниці рибосоми взаємодіють між собою, структурна перебудова маленької субодиниці не залишається непомітною для великої: конформаційні зміни відбуваються і тут. Одним із результатів перебудови є зміна взаємодії між EF1 і відповідним сайтом його зв’язування в основі стебла L7/12, яка приводить до активації GTP-ази, – відбувається гідроліз GTP, конформаційна перебудова EF1 із втратою спорідненості до рибосоми та тРНК і дисоціація фактора.
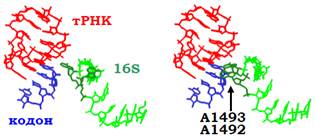
Рис. 19. Взаємодія в межах А-сайта на маленькій субодиниці між кодоном, антикодоновою петлею тРНК і частиною рРНК 16Sу випадку неспорідненого (ліворуч, 1N36 – друга кодон-антикодонова пара основ є не комплементарною) і спорідненого (праворуч, 1IBM) антикодонів.
Акомодація аа-тРНК завершує першу стадію елонгаційного циклу. Перед гідролізом GTP розміщення аа-тРНК на рибосомі суттєво відрізняється від кінцевої точки процесу зв’язування – локалізації в А-сайті. Оскільки сайти зв’язування тРНК формуються двома субодиницями (мають дві “половини”), остаточний А-сайт позначають як А/А. У складі комплексу з EF1 антикодонова частина розміщена в А-сайті на маленькій субодиниці, але акцепторна частина утримується в основі стебла L7/12 на великій – так зване А/Т положення (рис. 20).
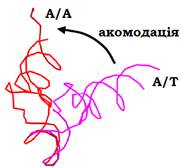
Рис. 20. А/Т (1QZA) і А/А (1QZB) положення аа-тРНК на рибосомі до й після акомодації відповідно.
При цьому антикодонове стебло суттєво вигинається – фіксація антикодона та акцепторного стебла підтримує напружену конформацію тРНК. Після гідролізу GTP, коли EF1 дисоціює, один із фіксаторів зникає – тРНК, ніби пружина, розпрямляється, її акцепторне стебло автоматично опиняється в А-сайті на великій субодиниці – у зоні пептидил-трансферазного центру. Ефективність цього процесу акомодації (рис. 20) залежить від жорсткості фіксації антикодонової петлі тРНК на маленькій субодиниці. Якщо взаємодія між кодоном і антикодоном не є повністю комплементарною, аа-тРНК просто дисоціює від рибосоми – це друга (після первинного зв’язування) можливість виправити помилку впізнання кодона.
Загальний сценарій зв’язування аа-тРНК з рибосомою зображено на рис. 21.
• На першому етапі початкового відбору аа-тРНК відбувається швидка асоціація / дисоціація потрійних комплексів EF1·GTP–аа-тРНК з відкритою формою рибосоми, яка фіксується за рахунок взаємодій з EF1. Відкрита форма сприяє також дисоціації деаміноацильованої тРНК з Е-сайта рибосоми (не показано на рис. 21).
• При утворенні комплементарної кодон-антикодонової подвійної спіралі, вона стабілізується за рахунок взаємодій з нуклеотидами рРНК 16S. Локальна конформаційна зміна 16S, яка є наслідком цих взаємодій, спрацьовує як тригер структурної перебудови спочатку маленької, потім великої субодиниць. Унаслідок перебудови антикодонова петля тРНК жорстко замикається на маленькій субодиниці, акцепторне стебло – на великій у основі пальця L7/12, і EF1 набуває GTP-азної активності.
• Гідроліз GTP розмикає ланцюг подій на дві частини, роблячи його необоротним. Після гідролізу EF1·GDP дисоціює, залишаючи аа-тРНК у напруженій конформації.
• Далі процес розгалужується: або, при недостатньо міцних кодон-антикодонових взаємодіях, відбувається дисоціація аа-тРНК, яка повертає систему до вихідного стану, або здійснюється акомодація – релаксація напруженої аа-тРНК, яка виводить її акцепторний кінець до пептидил-трансферазного центру.

Рис. 21. Схема основних подій при зв’язуванні аа-тРНКз А-сайтом рибосоми. Е-сайт тРНК не показано для спрощення.
Загальним наслідком процесу зв’язування, таким чином, є повна підготовка системи трансляції до наступного етапу елонгаційного циклу.
Транспептидація
Реакція перенесення пептидилу – транспептидація – полягає в руйнуванні ковалентного зв’язку між карбоксильною групою С-кінцевої амінокислоти пептидилу та 3′-кінцевою ОН-групою пептидил-тРНК і утворенні натомість пептидного зв’язку між звільненою карбоксильною групою та аміногрупою амінокислоти у складі аа-тРНК. Таким чином, при транспептидації пептидил переноситься з Р- до А-сайта рибосоми: в А-сайті опиняється пептидил-тРНК із подовженим на одну амінокислоту пептидилом, у Р-сайті залишається деаміноацильована тРНК (див. рис. 15).
Стандартна вільна енергія гідролізу зв’язку між пептидилом і тРНК оцінюється приблизно в –7,5 ккал/моль, енергія гідролізу пептидного зв’язку –0,5 ккал/моль. Отже, загальний енергетичний баланс транспептидації ~ –7,0 ккал/моль: це спонтанний процес, який не потребує джерел енергії – енергію було заощаджено при аміноацилюванні тРНК
Процес транспептидації, що відбувається безпосередньо після акомодації аа-тРНК, є найшвидчим етапом елонгаційного циклу. Каталіз реакції здійснюється пептидил-трансферазним центром великої субодиниці рибосоми, розташованим в основі центрального протуберанця (див. рис. 8) і формується пептидил-трансферазною петлею рРНК 23S. У радіусі ~18 Å від субстратів реакції немає жодної білкової хімічної групи, тобто рибосома – це рибозим. Слід, проте, ще раз зауважити, що вільна рРНК 23S не має каталітичної активності – активна конформація рРНК реалізується лише в комплекс із певним мінімальним набором білків.

Рис. 22. Процес перенесення пептидилу з Р-сайта на аа-тРНК в А-сайті через інтермедіатну сполуку, стабілізовану взаємодією з аденозином (А синього кольору) рРНК 23S. Амінокислотні бокові залишки R-пронумеровані в порядку приєднання їх до поліпептидного ланцюга.
Реакція транспептидації проходить через утворення інтермедіатної сполуки з формуванням зв’язку між N аміногрупи аа-тРНК і С, яким пептидил приєднаний до тРНК, атом оксигену набуває при цьому негативного заряду (рис. 22). Утворенню інтермедіату передує захоплення протона аміногрупи атомом N3 аденіну, що знаходиться в активному центрі. Легка іонізація N3 зумовлена його особливим мікрооточенням у складі рРНК 23S, протонований азот стабілізує негативно заряджений О. Далі протон переноситься на 3′ ОН-групу пептидил-тРНК, яка, відповідно, стає деаміноацильованою – втрачає зв’язок із С, замість якого остаточно формується пептидний зв’язок.
Механізм каталізу транспептидації є цілком аналогічним до такого білкових ферментів: рибосома здійснює жорстке взаємне орієнтування субстратів у активному центрі (і ця обставина – ентропійний каталіз – є головним фактором прискорення реакції транспептидації), а також завдяки створенню специфічного мікрооточення певної хімічної групи (аденіну) забезпечує стабілізацію проміжного високоенергетичного стану.
Транслокація
Результатом транспептидації є значне перегрупування лігандів, зв’язаних з рибосомою: пептидил-тРНК опиняється в А-сайті, деаміноацильована тРНК – у Р-сайті. Ураховуючи підвищену спорідненість акцепторної частини пептидил-тРНК до Р-сайта, рибосома має спонтанно пересунутися вздовж мРНК у напрямку до її 3′-кінця, і таке пересування – транслокація – має розпочатися з руху великої субодиниці (рис. 23). На проміжній стадії виникають гібридні сайти А/Р і Р/Е – стани, коли акцепторні частини тРНК уже знаходяться в Р (або Е) сайті на великій субодиниці, але антикодонові частини – ще в А (або Р) сайті. Зрозуміло, що рух субодиниць передбачає послаблення взаємодій між ними – певний розблокований після транспептидації, відкритий структурний стан рибосоми. Зрозуміло також, що послаблення взаємодій між субодиницями є енергетично невигідним. Відповідно, хоча транслокація є внутрішньою властивістю рибосоми і відбувається спонтанно (вільна енергія знижується в кінцевому стані за рахунок високої спорідненості пептидил-тРНК до Р-сайта), швидкість руху є дуже повільною в позафакторній системі in vitro, оскільки процес проходить через проміжний високоенергетичний стан. In vivo фактором прискорення процесу є білок EF2 (інше позначення – EFG).
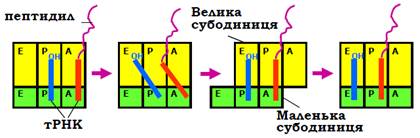
Рис. 23. Схема транслокації рибосоми через проміжну стадію гібридних сайтів.
Частина молекули EF2 є гомологічною білку EF1 – також має сайт зв’язування GTP/GDP і також взаємодіє з великою субодиницею рибосоми в основі пальця L7/12. Але у складі білка є ще один додатковий домен, який мімікрує під структуру антикодонової частини тРНК, структура білка в цілому нагадує комплекс EF1 – тРНК (рис. 24).
Фактор EF2 існує у принаймні чотирьох структурних станах залежно від типу зв’язаного ліганду: 1) EF2·GTP поза рибосомою – має високу спорідненість до рибосоми; 2) EF2·GTP на рибосомі – активна GTP-аза; 3) EF2·GDP·Pi – після гідролізу GTP (Pi – неорганічний фосфат); 4) EF2·GDP після дисоціації фосфату – має низьку спорідненість до рибосоми.

Рис. 24. Поверхня комплексу EF1-тРНК(структура з рис. 17) і білка EF2 (2EFG).
Вільний від будь-якого ліганду білок не має впливу на транслокацію, однак у комплексі з будь-яким гуаніновим нуклеотидом (включаючи також аналоги GTP, що не можуть бути гідролізовані) фактор прискорює транслокацію за рахунок своєї спорідненості до проміжного відкритого стану рибосоми. Проте у випадку гідролізу GTP (який передує остаточній транслокації) швидкість переміщення рибосоми підвищується ще в ~50 разів: найефективнішим стабілізатором відкритого стану рибосоми виявляється форма EF2·GDP·Pi.
Отже, сценарій транслокації можна уявити наступним чином (рис. 25).
• Після транспептидації рибосома перебуває в рівновазі між закритою та відкритою формою. Тільки друга форма здатна до транслокації, але вона у той самий час є більш високоенергетичною – рівновага зсунута в бік закритої форми.
• Взаємодія з EF2·GTP стабілізує відкриту форму рибосоми. Швидко після зв’язування, за рахунок взаємодії з сайтом G-білків у основі стебла L7/12, EF2 набуває GTP-азної активності – відбувається гідроліз GTP і перехід EF2 у структурну форму, що найефективніше сприяє розблокуванню рибосоми.
• У розблокованій формі рибосома рухається вздовж мРНК (зв’язок мРНК з молекулами тРНК зберігається, тобто вона переміщується також відносно тРНК). Цей рух є броунівським (одномірна дифузія під дією теплових флуктуацій), але спорідненість пептидил-тРНК до Р-сайта робить напрямок до 3′-кінця мРНК більш імовірним. Крім того, тРНК-подібний”структурний домен EF2 взаємодіє з маленькою субодиницею в межах А-сайта, сприяючи витісненню звідти антикодонової частини пептидил-тРНК.
• Одночасно з переміщенням, і незалежно від нього, відбувається дисоціація неорганічного фосфату. EF2, який залишається в комплексі з GDP, втрачаючи спорідненість, дисоціює від рибосоми, яка, у свою чергу, повертається до закритого структурного стану.
У результаті система є готовою до наступного елонгаційного циклу: новий кодон опинився в А-сайті, сам А-сайт є вільним від тРНК. Деаміноацильована тРНК, яка в результаті транслокації опинилася в Е-сайті рибосоми, може дисоціювати звідти відразу, або залишитися до етапу зв’язування наступної аа-тРНК.

Рис. 25. Послідовність основних подій при транслокації рибосоми.
Описані механізми функціонування рибосоми під час елонгаційного циклу дозволяють стверджувати, що рибосома працює за принципами молекулярної машини – пристрою, який з високою швидкістю (у середньому 10 – 15 елонгаційних циклів за секунду) і точністю (частота помилок ~10–4) здійснює білковий синтез. Під час елонгаційного циклу рибосома осцилує між закритим структурним станом, який забезпечує каталіз реакції нарощування амінокислотного ланцюга, і відкритими станами, в яких здійснюється специфічний відбір амінокислот згідно з генетичним кодом та переміщення рибосоми вздовж матриці. Перемикання конформацій залежить від взаємодій з факторами елонгації, які фіксують проміжні відкриті стани рибосоми, забезпечуючи прискорення перебудов. Гідроліз двох молекул GTP під час елонгаційного циклу використовується для звільнення факторів і повернення рибосоми до закритої жорсткої конформації.
Рушійною силою для переміщення рибосоми та її частин є хаотичний тепловий рух, але молекулярна конструкція рибосоми, її взаємоді їз тРНК, матрицею та факторами елонгації, і зміни цих взаємодій унаслідок хімічних реакцій (транспептидація, гідроліз GTP) задають певну траєкторію рухів і каталізують їх у певних напрямах. Аналогічні механізми використовуються й при ініціації та термінації трансляції.
Ініціація трансляції
Розпочинатися процес елонгації трансляції має зі стартового кодона мРНК, і в першому елонгаційному циклі, коли немає пептидил-тРНК у Р-сайті, якась стартова – ініціаторна – аа-тРНК має виконувати цю роль. Отже, сутність ініціації полягає в:
1) упізнанні стартового кодону, який задає початок і рамку зчитування інформації;
2) збиранні рибосоми з двох субодиниць на мРНК у зоні стартового кодону;
3) завантаженні ініціаторної аа-тРНК на стартовий кодон і водночас у Р-сайт рибосоми. Стартовим кодоном виступає здебільшого метіоніновий кодон AUG, відповідно, ініціаторною є завжди Met-тРНКіMet (індекс – і – вказує на те, що це – саме ініціаторна метіонінова тРНК, тобто вона відрізняється за своєю структурою від звичайної тРНКMet, яка використовується при елонгації). У прокаріотів, на відміну від еукаріотів, аміногрупа метіоніну ініціаторної тРНК є формільованою (N-формілметіонін, fMet – рис. 26).

Рис. 26. Метіонін і N-формілметіонін.
Механізми ініціації трансляції суттєво відрізняються у про- та еукаріотів. Еукаріотична мРНК після синтезу транспортується з ядра до цитоплазми, де й відбувається ініціація. Кожна молекула мРНК містить тільки одну рамку зчитування (один стартовий кодон), елементи системи ініціації взаємодіють спочатку з кепом на 5′-кінці молекули, після чого відбувається сканування матриці з метою пошуку стартового кодону ініціація відбувається за так званим скануючим механізмом.
Прокаріотична трансляція тісно узгоджена з транскрипцією і відбувається під час синтезу мРНК. При цьому мРНК, що синтезується на оперонах, часто містить кілька послідовних рамок зчитування і кілька стартових кодонів. Ініціація трансляції відбувається окремо на кожному з них усередині мРНК, і впізнання цих стартових кодонів не залежить від їхнього розташування відносно 5′-кінця матриці – внутрішня ініціація.






